Clear Sky Science · es
CISH, un punto de control intracelular clave, en comparación y en combinación con puntos de control inmunitarios contra el cáncer existentes y emergentes
Soltando los frenos de las células que combaten el cáncer
Las inmunoterapias contra el cáncer han cambiado el pronóstico de muchos pacientes, pero una gran parte de las personas aún obtiene poco o ningún beneficio. Este estudio explora una nueva forma de potenciar las propias células T del organismo —los asesinos del sistema inmunitario— desactivando un “freno” interno llamado CISH. A diferencia de los fármacos actuales que actúan sobre interruptores en la superficie celular, esta estrategia se dirige a un sistema de control enterrado dentro de la célula, con el objetivo de hacer que las células T diseñadas sean mucho mejores en localizar y destruir tumores, incluso cuando los cánceres intentan ocultarse.
Un nuevo tipo de freno inmunitario
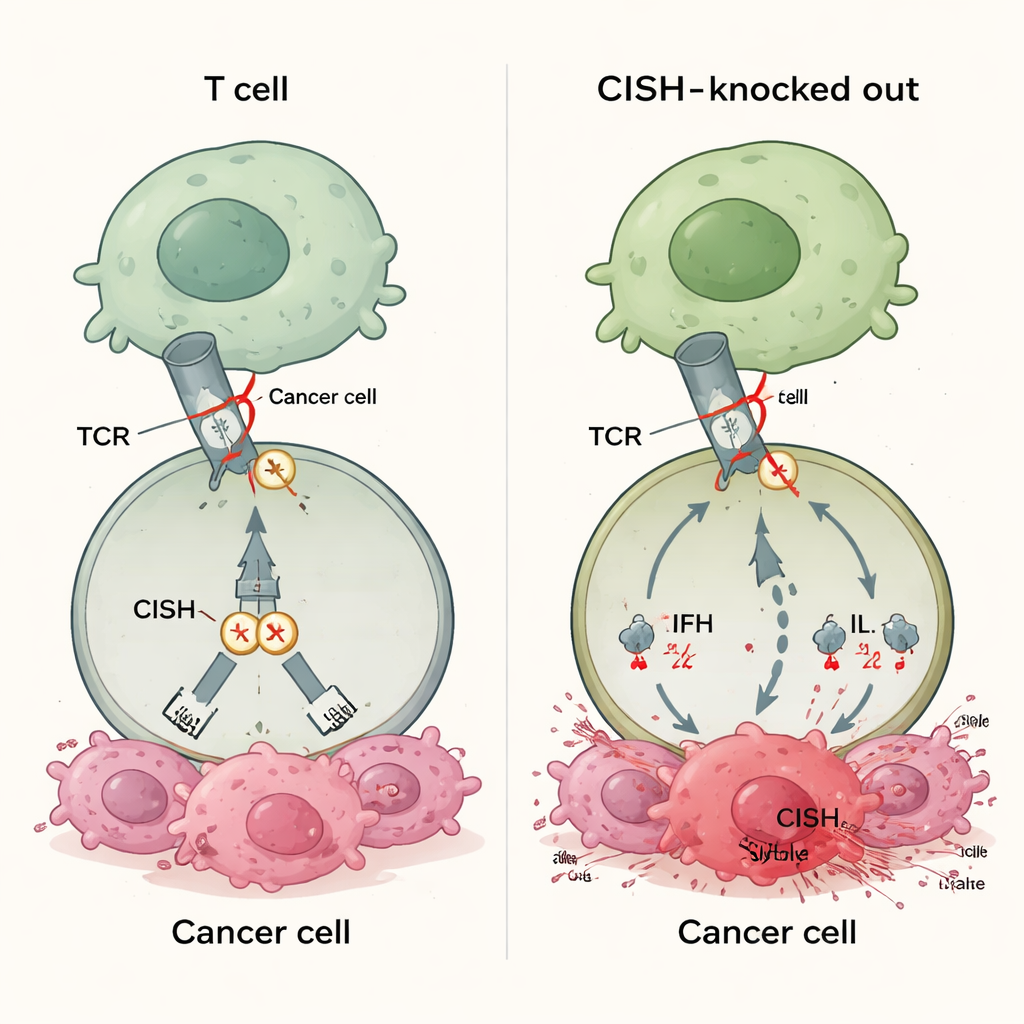
La mayoría de los fármacos de inmunoterapia aprobados bloquean proteínas como PD-1 en la superficie de las células T. Estos fármacos funcionan solo cuando los tumores muestran moléculas compañeras coincidentes como PD-L1, y muchos cánceres o bien nunca expresan suficientes de estas compañeras o las pierden con el tiempo. Eso ayuda a explicar por qué el 30–60% de los pacientes no responden a las terapias de puntos de control actuales. CISH pertenece a una clase diferente de frenos que se sitúan dentro de la célula T. Se activa cuando el receptor de la célula T detecta un objetivo y luego atenúa la señal promoviendo la destrucción de una proteína clave de señalización. Dado que esta acción no depende de ligandos expresados por el tumor, apagar CISH podría, en principio, potenciar las respuestas de las células T en muchos tipos de cáncer, independientemente del estado de PD-L1 u otros biomarcadores.
De tú a tú con los puntos de control existentes
Los investigadores usaron edición genética CRISPR para eliminar CISH y compararon las células T resultantes con células que carecían de PD-1 u otros frenos intracelulares. Cuando estimularon las células T de manera débil —una situación pensada para imitar tumores que muestran solo pequeñas cantidades de antígeno— las células con CISH eliminado produjeron muchas más señales inmunitarias clave, incluyendo interferón gamma, TNF-alfa e IL-2. Estas células también fueron más “polifuncionales”, lo que significa que células T individuales podían realizar varias tareas a la vez, un rasgo distintivo de la potente actividad antitumoral. En contraste, simplemente eliminar PD-1 no ayudó en condiciones de señal baja. En múltiples pruebas, la pérdida de CISH aumentó con mayor intensidad la activación, la capacidad de matar y la formación de células T con memoria duradera en comparación con la eliminación de otros puntos de control internos candidatos como RASA2, CBLB, SOCS1, REGNASE1, HPK1 o PTPN1/2.
Trabajando junto con otros interruptores internos
Dado que la señalización de las células T está controlada por muchas vías superpuestas, el equipo preguntó si combinar la eliminación de CISH con la supresión de otros frenos podría producir beneficios aditivos. Usando edición CRISPR múltiple, encontraron que eliminar CISH junto con SOCS1, HPK1 o RASA2 aumentaba aún más la producción de citocinas útiles bajo estimulación débil. En un modelo tumoral basado en una mutación frecuente de KRAS, las células T diseñadas con un receptor específico para KRAS fueron mejores matando células cancerosas cuando CISH se eliminó, y este efecto se intensificó cuando la pérdida de CISH se combinó con la eliminación de SOCS1 o RASA2. Estos hallazgos sugieren que CISH controla un nodo no redundante en la biología de las células T y puede cooperar con socios selectos para afilar la citotoxicidad específica contra el tumor.
Haciendo las células CAR-T más resistentes frente a tumores escurridizos
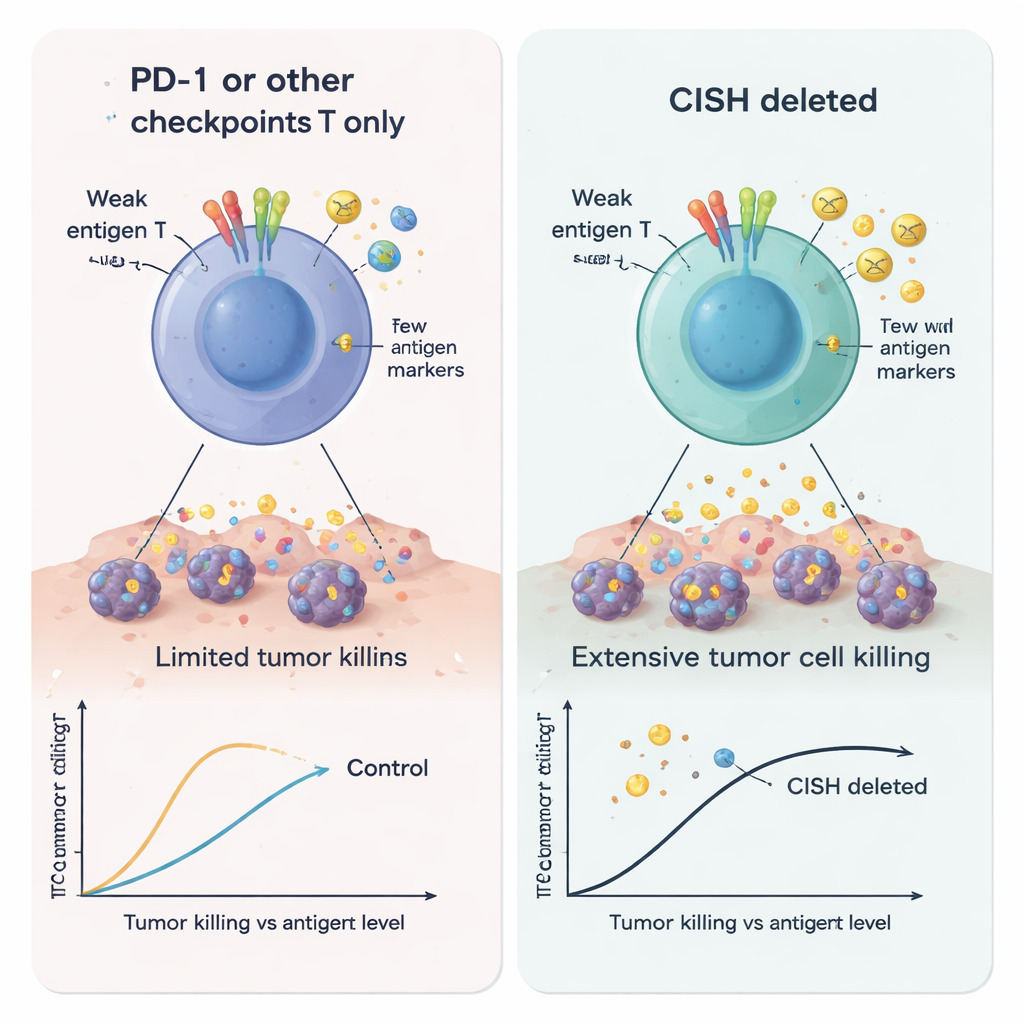
Los autores pasaron luego a un entorno clínicamente relevante: células CAR-T dirigidas contra el marcador de células B CD19. Crearon células leucémicas que expresaban distintos niveles de CD19 para imitar tumores que pierden o reducen sus objetivos para escapar de la terapia. Las CAR-T sin CISH fueron notablemente mejores destruyendo células cancerosas, incluso cuando CD19 era escaso, y secretaron más señales de activación y reclutamiento. Al mismo tiempo, liberaron menores cantidades de moléculas conocidas por debilitar las células T o promover el crecimiento tumoral, como Galectina-1, Galectina-3, 4-1BB soluble, IL-1α y la glicoproteína EMMPRIN/CD147. En conjunto, estos cambios apuntan a una célula CAR-T más agresiva y menos fácilmente suprimible, particularmente adecuada para entornos tumorales hostiles con bajo antígeno.
Del banco de laboratorio a los pacientes
Más allá de tubos de ensayo y placas de cultivo, la idea de dirigirse a CISH ya ha llegado a pacientes. Un ensayo primero en humanos que utilizó linfocitos infiltrantes tumorales editados para eliminar CISH en una persona con cáncer colorrectal avanzado produjo una respuesta completa que ha durado más de dos años, a pesar de la resistencia del cáncer a múltiples tratamientos previos. Al demostrar que CISH es un potente punto de control interno farmacológicamente abordable que aumenta la sensibilidad de las células T incluso a señales tumorales débiles, este estudio ayuda a explicar ese resultado clínico notable y respalda los esfuerzos para desarrollar terapias futuras —ya sean células editadas genéticamente o fármacos— que aflojen con seguridad este freno interno y amplíen el alcance de la inmunoterapia contra el cáncer.
Cita: Cano, F., Bravo-Blas, A., Colombe, M. et al. CISH, a key intracellular checkpoint, in comparison and combination to existing and emerging cancer immune checkpoints. Commun Biol 9, 319 (2026). https://doi.org/10.1038/s42003-026-09579-x
Palabras clave: inmunoterapia contra el cáncer, células T, terapia CAR-T, puntos de control inmunitarios, edición genética CRISPR