Clear Sky Science · es
Una mutación patógena en α‑SNAP impide la unión a lípidos de membrana al ocultar un bucle hidrofóbico crítico
Cómo un pequeño cambio en una proteína puede alterar el desarrollo cerebral
Las células cerebrales transportan constantemente carga en pequeñas burbujas llamadas vesículas, y una proteína ayudante llamada alpha‑SNAP es central para que esas entregas se realicen. Una mutación rara en alpha‑SNAP, conocida por una línea de ratones llamada “hyh”, provoca graves problemas en la formación del cerebro y en el equilibrio de fluidos. Este estudio plantea una pregunta aparentemente simple con grandes consecuencias: ¿esa sustitución de una sola letra en alpha‑SNAP impide que se adhiera a las membranas celulares, y podría ello ser una razón clave por la que el cerebro se desarrolla mal?
Un trabajador del muelle celular con muchas funciones
Alpha‑SNAP suele actuar como una especie de peón del muelle para las vesículas, ayudándolas a fusionarse con las membranas celulares para que la carga pueda liberarse o reciclarse. Coopera con un conjunto de proteínas llamadas SNARE y con una máquina consumidora de energía llamada NSF para acercar las membranas y, después, restablecer el sistema para la siguiente ronda. Más allá de este papel clásico, alpha‑SNAP también contribuye a controlar procesos como la autofagia, la muerte celular, la entrada de calcio y la detección del estado energético. Todas estas funciones dependen, de una u otra manera, de la capacidad de alpha‑SNAP para tocar e insertar parcialmente sus regiones en la superficie oleosa de las membranas.
Un bucle oculto y una mutación problemática
Trabajos previos habían mostrado que alpha‑SNAP usa un corto “bucle” grasiento cerca de un extremo de la proteína para engancharse a las membranas. En la proteína sana, este bucle sobresale y puede introducirse en la capa externa de la membrana. En el ratón hyh, un único aminoácido en la posición 105 se sustituye, dando lugar a la mutación M105I. Los autores utilizaron simulaciones por ordenador para ver cómo cambia la forma de la proteína. Encontraron que la proteína mutante se vuelve ligeramente más compacta y se retuerce de manera que repliega el bucle hidrofóbico hacia el interior, alejándolo del agua y de las membranas. Como resultado, la proteína mutante se aproxima a las membranas con un ángulo más plano y tiende a presionarlas con una región menos adhesiva, lo que reduce tanto el tiempo de contacto como la profundidad de inserción. Los cálculos de energía de unión respaldaron esto: la proteína de tipo salvaje se estabilizaba en un estado de baja energía y fuerte unión, mientras que la mutante prefería contactos más débiles y superficiales.
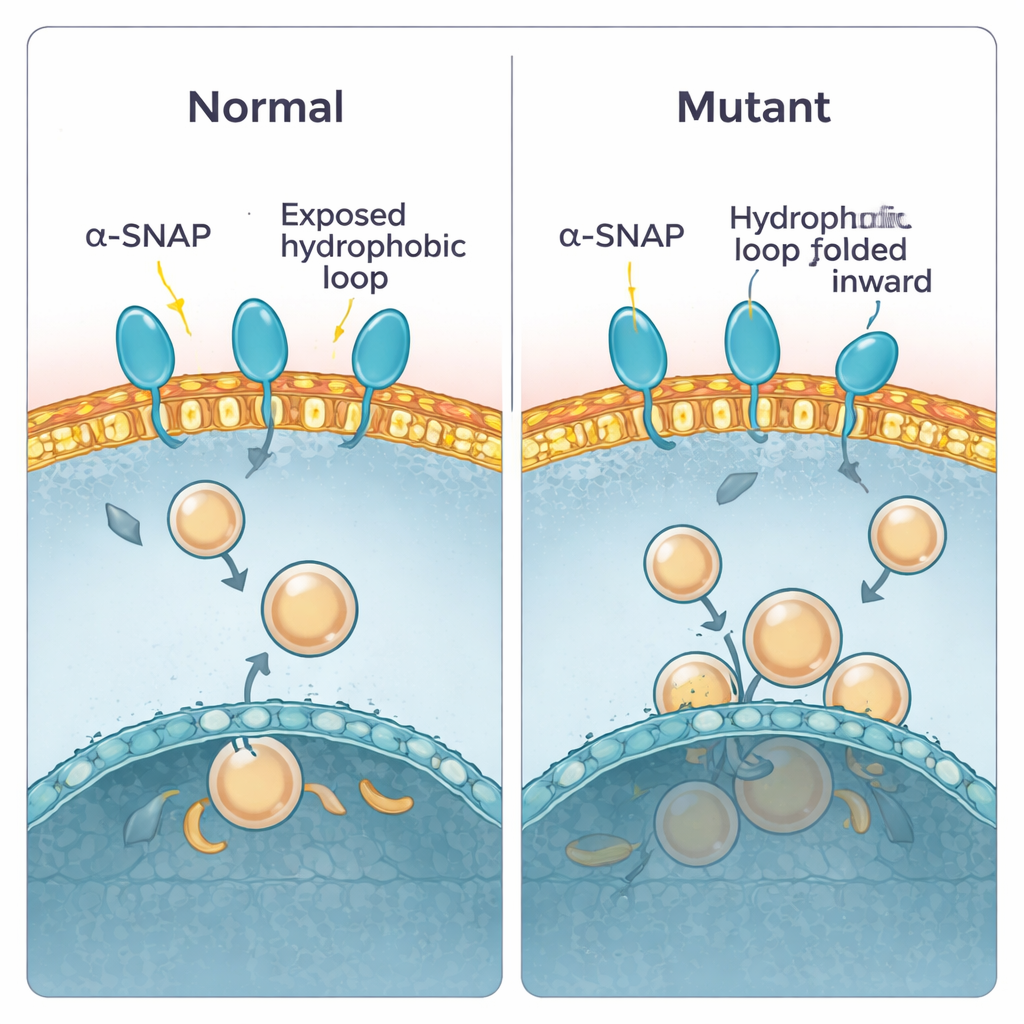
Poniendo la predicción a prueba en el laboratorio
Para comprobar estas predicciones, el equipo purificó tanto alpha‑SNAP normal como la mutante y evaluó su comportamiento en distintos ensayos experimentales. Primero, usaron un disolvente detergente que se separa en fases acuosa y oleosa, emulando la elección entre agua y membrana. Alpha‑SNAP normal se repartió de forma equilibrada, consistente con una superficie parcialmente oleosa. La versión mutante mostró menos disposición a entrar en la fase oleosa, sugiriendo que sus partes grasas están efectivamente más enterradas. A continuación, dejaron que las proteínas interaccionaran con “láminas” planas de membrana plasmática preparadas a partir de células e imaginaron cuántos puntos de unión aparecían. De nuevo, alpha‑SNAP normal salpicaba la membrana, mientras que la mutante se unía mucho menos. Finalmente, hicieron flotar burbujas de membrana artificiales (liposomas) compuestas por lípidos cerebrales a través de gradientes de sacarosa. Alpha‑SNAP de tipo salvaje ascendía con las vesículas ricas en lípidos de membrana plasmática, mientras que la mutante quedaba rezagada, uniéndose pobremente a menos que las vesículas se prepararan con una mezcla de membrana más interna.
Consecuencias en el cerebro en desarrollo
Los investigadores se fijaron luego en cerebros de embriones de ratón en desarrollo, centrándose en una etapa en la que nacen nuevas neuronas. Separando el contenido celular en fracciones soluble y unida a membrana, mostraron que los niveles totales de alpha‑SNAP ya estaban reducidos en los cerebros hyh, pero, más importante, la fracción adherida a las membranas era desproporcionadamente baja en comparación con ratones normales. Al separar además distintos tipos de membrana, encontraron que la mayor pérdida se producía en la membrana plasmática, la superficie externa de la célula, mientras que las membranas internas se veían mucho menos afectadas. La microscopía contó la misma historia: en tejido normal, alpha‑SNAP delineaba las células con un patrón en panal que coincidía con un marcador de superficie conocido. En cerebros hyh, ese tinción de borde nítida se desvanecía hasta convertirse en un brillo más difuso e interno, indicando que la proteína mutante no se mantiene anclada en el borde celular donde la fusión de vesículas y la señalización son más activas.
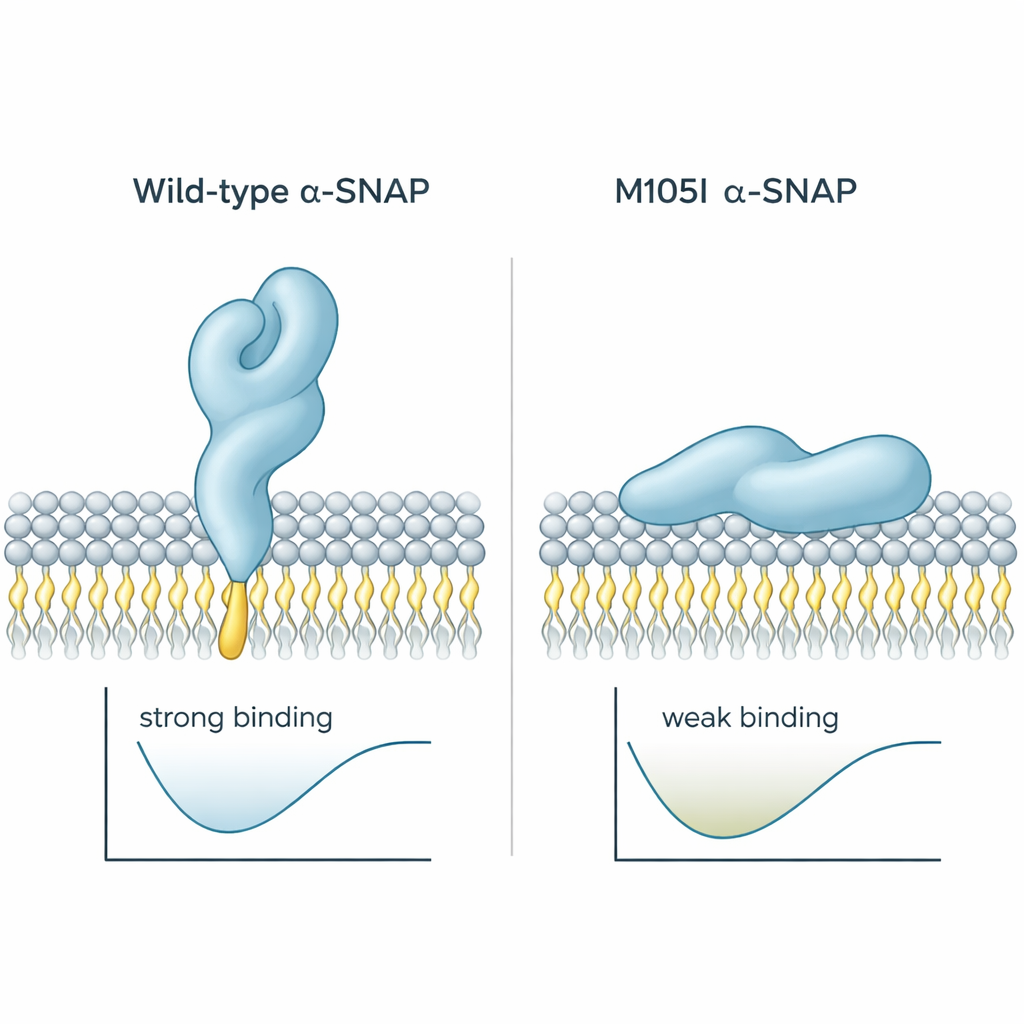
Por qué esto importa para la enfermedad
En conjunto, el trabajo muestra que la mutación M105I hace más que simplemente reducir la cantidad de alpha‑SNAP; altera el plegamiento de la proteína de modo que su bucle clave para captar membranas queda oculto. Esto dificulta que alpha‑SNAP agarre la membrana plasmática y adopte la orientación adecuada para organizar la maquinaria de fusión. En un cerebro en desarrollo, donde la entrega precisa de señales y materiales de construcción en la superficie celular es esencial, este sutil defecto estructural probablemente contribuye a la hidrocefalia, la corteza mal cableada y otros defectos observados en ratones hyh. Para el público no especialista, el mensaje es claro: incluso un cambio diminuto en la forma de una sola proteína puede remodelar cómo las células se comunican y, en consecuencia, cómo se construye un cerebro.
Cita: Méndez-Ruette, M., Bedoya, M., Hinrichsen, B. et al. A pathogenic mutation in α-SNAP impairs membrane lipid binding by concealing a critical hydrophobic loop. Commun Biol 9, 294 (2026). https://doi.org/10.1038/s42003-026-09578-y
Palabras clave: alpha-SNAP, unión a membrana, mutación proteica, desarrollo cerebral, fusión de vesículas