Clear Sky Science · es
ZFP42 mantiene la capacidad de autorrenovación y la transcripción rítmica en células madre y progenitoras epidérmicas humanas a través de CRY1
Por qué importa el reloj interno de tu piel
Cada noche, mientras duermes, tu piel no descansa: repara, renueva y se prepara para el siguiente día de exposición al sol y desgaste. Este estudio explora cómo pequeños relojes biológicos dentro de las células madre de la piel mantienen ese proceso de renovación en horario, y cómo un factor poco conocido llamado ZFP42 se asocia con una proteína del reloj, CRY1, para conservar esas células madre jóvenes y funcionales. Comprender este vínculo entre la cronobiología y la renovación cutánea podría, en el futuro, ayudar a desarrollar mejores tratamientos para el envejecimiento de la piel, la cicatrización y las enfermedades cutáneas.
Los relojes de la piel
Al igual que el reloj maestro del cerebro que responde a la luz, casi todos los tejidos del cuerpo tienen su propio reloj “periférico”. En la capa externa de la piel, la epidermis, las células madre y progenitoras en la base se dividen constantemente, ascienden y forman la barrera protectora de la que dependemos. Los autores estudiaron estas células madre y progenitoras epidérmicas (EPSC) procedentes de fetos humanos y de adultos para ver cuántos genes se activan y desactivan con un ritmo aproximado de 24 horas. Encontraron que alrededor de uno de cada diez genes activos en estas células muestra oscilación diaria, y que los patrones temporales de muchos genes clave cambian entre la piel fetal y la adulta, lo que sugiere que los relojes celulares de la piel envejecen con nosotros.
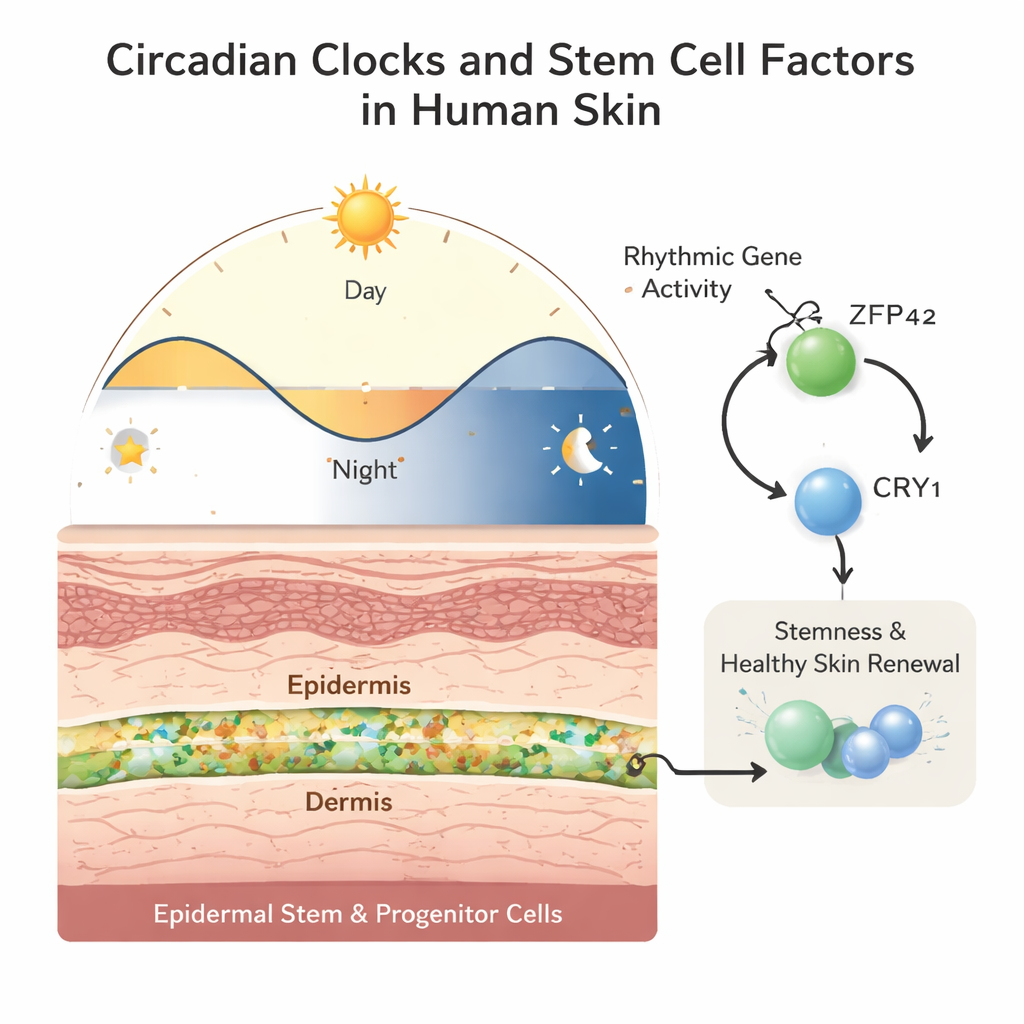
Piel fetal frente a adulta: ritmos más fuertes en la juventud
Al sincronizar EPSC en placas de laboratorio y medir la actividad génica cada tres horas, el equipo descubrió que los genes centrales del reloj —como BMAL1, PER1 y CRY1— oscilan de forma robusta tanto en células fetales como adultas. Sin embargo, la “intensidad” general de la actividad génica rítmica, conocida como amplitud, fue mayor en las células fetales y atenuada en las adultas. Muchos de los genes rítmicos compartidos estaban relacionados con la replicación del ADN, la división celular y la reparación, procesos centrales para mantener sanas a las células madre. El momento de los picos génicos también cambió: las células adultas mostraron ritmos retrasados y alterados, especialmente en genes relacionados con la defensa antiviral, el envejecimiento celular y la muerte celular programada, lo que sugiere que el programa diario de protección y renovación se reajusta a medida que la piel madura y envejece.
La temporalidad diaria del crecimiento y la maduración
Cuando los investigadores analizaron los genes que eran rítmicos solo en fetos o solo en adultos, observaron diferencias llamativas. En las EPSC fetales, las oleadas de genes implicados en la respuesta a heridas, el metabolismo y la intensa división celular tendían a alcanzar su pico antes en el ciclo diario, acorde con su rápido crecimiento y capacidad regenerativa. En las EPSC adultas, los genes vinculados a la construcción de la barrera cutánea y al impulso de la diferenciación celular completa a menudo alcanzaban su pico antes que los genes que controlan la replicación del ADN y la división. Esta separación sugiere que las células madre de la piel adulta pueden utilizar la hora del día para alternar entre preparar células para convertirse en una superficie protectora y alimentar la proliferación celular más tarde, quizá para equilibrar el mantenimiento de la barrera con la protección frente al estrés diurno como la radiación ultravioleta.
ZFP42 y CRY1: mantener las células madre juveniles
Ahondando más, el equipo buscó moléculas regulatorias que pudieran estar por encima de estos genes rítmicos. Identificaron a ZFP42, más conocido como marcador de células madre muy tempranas, como altamente activo en las EPSC fetales y fuertemente asociado a promotores de genes rítmicos fetales. Cuando se redujeron los niveles de ZFP42 en EPSC jóvenes, las células se dividieron menos, se acumularon en una fase temprana del ciclo celular y mostraron más señales de diferenciación y muerte celular. Lo contrario también fue cierto: aumentar ZFP42 en EPSC de adultos mayores mejoró su capacidad de formar colonias, haciéndolas comportarse más como células madre jóvenes. De forma crucial, ZFP42 activó directamente al gen reloj CRY1 y era necesario para su comportamiento rítmico normal. Reducir CRY1 por sí solo imitó muchos efectos de la pérdida de ZFP42 —proliferación más lenta y mayor diferenciación— mientras que restaurar CRY1 rescató en parte los defectos de crecimiento, lo que indica que un eje ZFP42–CRY1 es central para mantener el comportamiento parecido al de células madre.
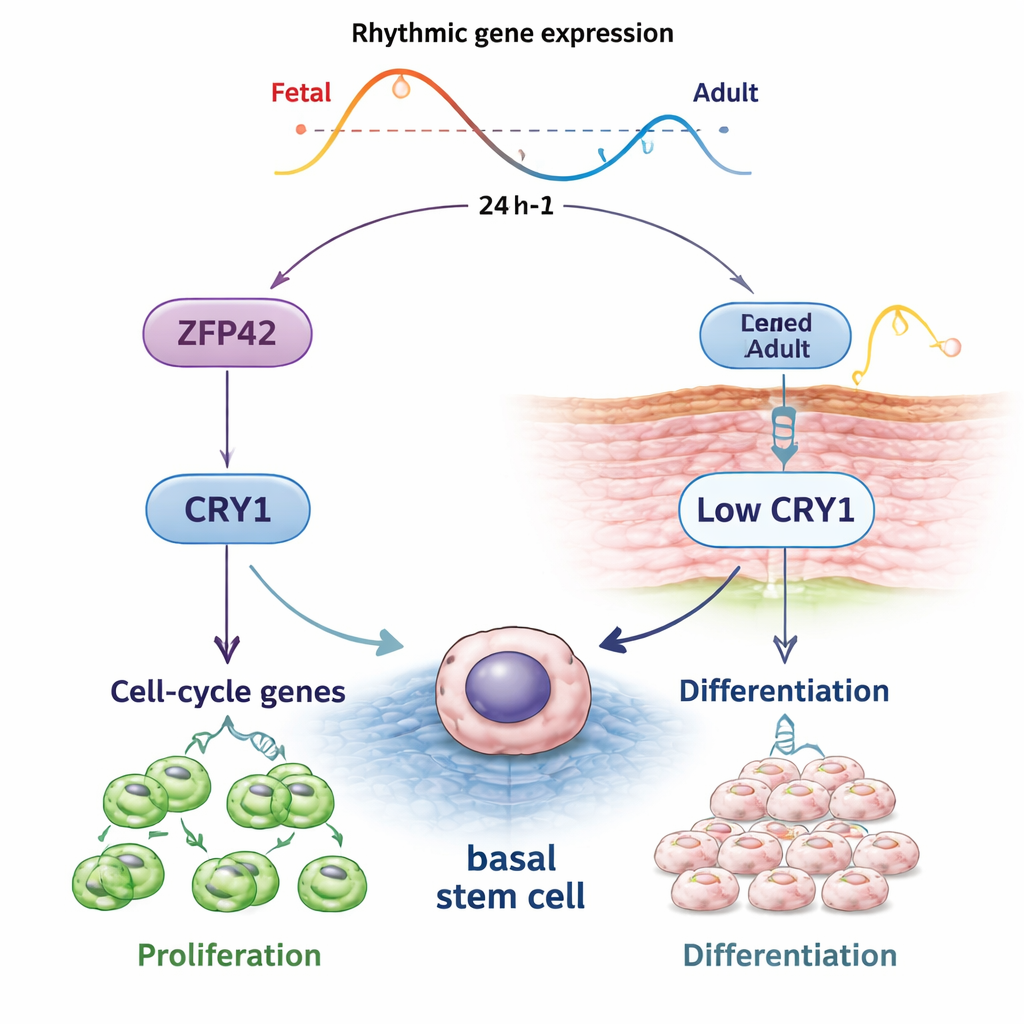
Qué significa esto para la salud de la piel
Para el público general, la conclusión es que las células madre de la piel no solo responden al daño y al envejecimiento de forma pasiva: siguen un horario diario coreografiado por relojes moleculares, y ese horario cambia a lo largo de la vida. ZFP42 actúa como un interruptor asociado a la juventud que mantiene al gen reloj CRY1 activo y rítmico, ayudando a las células madre epidérmicas a renovarse mientras previene una maduración prematura. A medida que los programas vinculados a ZFP42 se debilitan con la edad, los ciclos de renovación controlados por el reloj en la piel parecen desvanecerse. Aunque este trabajo se realizó en células en cultivo y necesita confirmación en tejido vivo, apunta a la posibilidad de que sintonizar la vía ZFP42–CRY1 o alinear los tratamientos con el tiempo interno de la piel pueda algún día mejorar las terapias para la piel envejecida, las heridas crónicas y otros trastornos del órgano más grande del cuerpo.
Cita: Gao, S., Tan, H., Xu, S. et al. ZFP42 maintains stemness and rhythmic transcription in human epidermal stem and progenitor cells via CRY1. Commun Biol 9, 291 (2026). https://doi.org/10.1038/s42003-026-09576-0
Palabras clave: ritmo circadiano, células madre de la piel, epidermis, CRY1, ZFP42