Clear Sky Science · es
Desarrollo de ligandos derivados de capsaicina para prohibitina para modular la interacción Aurora quinasa A/PHB2 y la mitofagia en células cancerosas
Por qué importa un compuesto de guindilla para el cáncer
Las guindillas deben su picor a la capsaicina, una pequeña molécula que se une a proteínas en nuestras células. Este estudio explora un giro sorprendente de esa especia conocida: los investigadores rediseñaron la capsaicina para crear nuevas moléculas con características farmacológicas que se dirigen a las “centrales eléctricas” de las células cancerosas —las mitocondrias— y modulan un proceso que esas células usan para mantener sus fábricas de energía en buen estado. Dado que las células cancerosas dependen en gran medida de mitocondrias eficientes para impulsar su crecimiento descontrolado, poder interrumpir selectivamente este sistema de soporte podría abrir una nueva vía para terapias anticancerígenas.
Las centrales energéticas celulares y su equipo de limpieza interno
Las mitocondrias equilibran constantemente la construcción de unidades nuevas con el reciclaje de las dañadas. El lado del reciclaje, llamado mitofagia, actúa como un sistema de control de calidad: las mitocondrias deterioradas se marcan y se degradan, mientras que las más sanas permanecen. Muchas células cancerosas secuestran este equilibrio, usando la mitofagia para eliminar mitocondrias débiles y enriquecer las “superrendidoras” que producen grandes cantidades de ATP, la moneda energética de la célula. Una proteína llamada Aurora quinasa A (AURKA), a menudo sobreproducida en tumores, se halló recientemente dentro de las mitocondrias donde se asocia con otra proteína, Prohibitina‑2 (PHB2), y con el adaptador de autofagia LC3. Juntas forman un complejo que promueve la mitofagia y sostiene una alta producción de energía en células cancerosas.
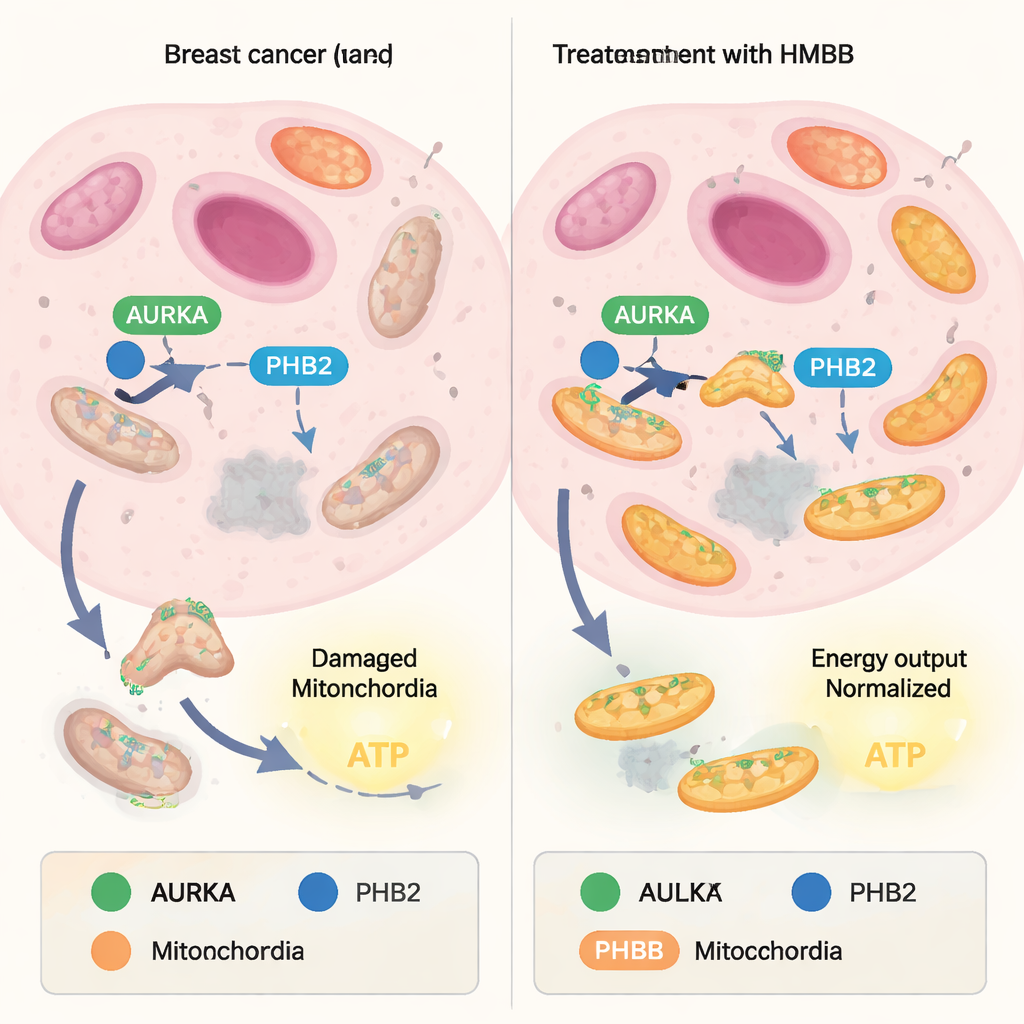
De la capsaicina picante a herramientas moleculares a medida
Trabajos anteriores habían mostrado que un compuesto natural llamado xantohumol puede unirse a PHB2 y desbaratar el complejo AURKA–PHB2–LC3, bloqueando la mitofagia y reduciendo la producción mitocondrial de ATP. No obstante, la estructura química del xantohumol no es ideal para el desarrollo de fármacos. En este estudio, los autores recurrieron a la capsaicina, otro ligando natural de PHB, y se preguntaron si podía remodelarse en herramientas más prácticas. Primero confirmaron que la capsaicina debilita ligeramente la interacción entre AURKA y PHB2 en células de cáncer de mama vivas, usando una técnica de imagen (FRET/FLIM) que mide cuán cerca están dos proteínas etiquetadas. Luego sintetizaron 16 moléculas inspiradas en la capsaicina modificando la “cola” y la “cabeza” aromática de la estructura original y probaron sistemáticamente cómo cada versión afectaba la asociación AURKA–PHB2 dentro de las mitocondrias.
Descubriendo un “pegamento” molecular que une proteínas
Las moléculas modificadas tuvieron efectos notablemente distintos. Algunas, como la propia capsaicina o un derivado llamado compuesto 5, facilitaron que AURKA y PHB2 se separaran. Otras apenas hicieron nada. Sin embargo, un subconjunto —especialmente una molécula denominada compuesto 13, más tarde llamada HMBB— tuvo el efecto opuesto y estrechó de forma significativa el vínculo entre AURKA y PHB2. Simulaciones de acoplamiento por ordenador ayudaron a explicar este comportamiento. La capsaicina y el compuesto 5 tendían a alojarse en el sitio activo de AURKA de maneras que generaban choques físicos con PHB2, empujando a las dos proteínas a separarse. En contraste, los compuestos 12 y 13 se acomodaban en el sitio activo de AURKA y simultáneamente contactaban un bolsillo inhibidor conocido en PHB2 sin causar un conflicto. En su lugar, sus formas les permitían actuar como un “pegamento molecular”, puenteando AURKA y PHB2 y estabilizando el complejo.
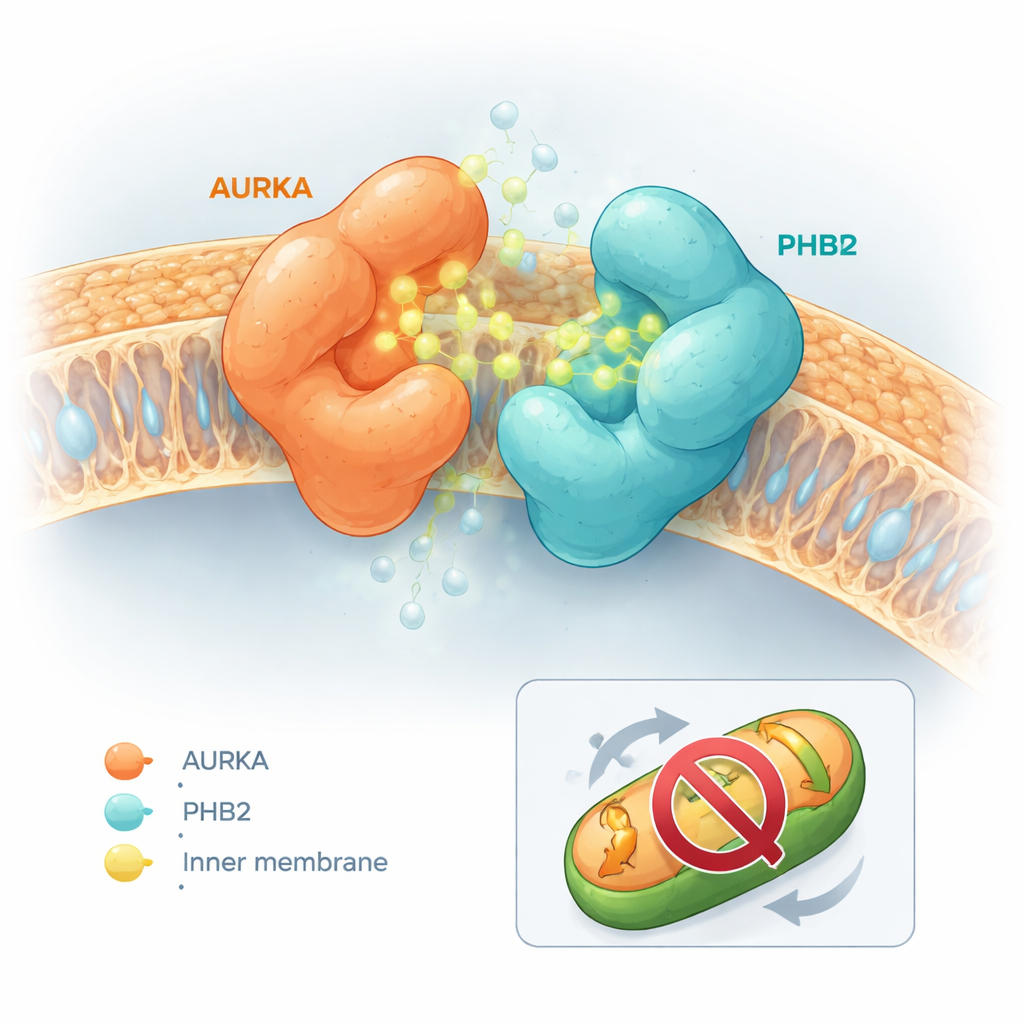
Bloquear la limpieza mitocondrial sin apagar el centro de control celular
Una cuestión crucial era si este comportamiento de pegamento molecular simplemente inhabilitaba AURKA en toda la célula, lo que implicaría un riesgo de efectos secundarios generalizados, o si actuaba de forma más selectiva. Usando un biosensor fluorescente distinto que informa sobre la activación de AURKA en los centrosomas —las estructuras que organizan la maquinaria de división celular— el equipo observó que HMBB no atenuó la actividad de AURKA en estos sitios. Sin embargo, en ensayos mitocondriales, HMBB revirtió la pérdida de masa mitocondrial que normalmente causa la sobreexpresión de AURKA en células de cáncer de mama. En células que producen de forma natural altos niveles de AURKA, HMBB aumentó el contenido mitocondrial, indicando que la mitofagia impulsada por AURKA fue bloqueada. En células con niveles bajos de AURKA, HMBB tuvo poco impacto, lo que subraya su dependencia de la vía AURKA–PHB2.
Qué podría significar esto para futuros tratamientos contra el cáncer
En conjunto, los hallazgos muestran que derivados de capsaicina cuidadosamente diseñados pueden afinar la interacción entre AURKA y PHB2 en las mitocondrias. Al actuar como pegamento molecular, HMBB y compuestos relacionados bloquean AURKA y PHB2 en una configuración que impide que el programa habitual de mitofagia progrese, sin eliminar las funciones esenciales de AURKA en otras partes de la célula. Para un lector no especializado, la idea clave es que los autores han creado moléculas prototipo que interfieren selectivamente con la manera en que las células cancerosas mantienen sus centrales energéticas en óptimas condiciones, potencialmente debilitando su suministro de energía mientras se preservan funciones celulares normales. Aunque estos compuestos aún están en una etapa temprana de laboratorio, ilustran una estrategia prometedora: usar pequeñas moléculas con características farmacológicas para dirigirse a asociaciones proteicas específicas dentro de las mitocondrias y, así, socavar las ventajas metabólicas de las que dependen muchos tumores.
Cita: Djehal, A., Caron, C., Giordano, D. et al. Development of capsaicin-derived prohibitin ligands to modulate the Aurora kinase A/PHB2 interaction and mitophagy in cancer cells. Commun Biol 9, 320 (2026). https://doi.org/10.1038/s42003-026-09573-3
Palabras clave: mitocondrias, mitofagia, Aurora quinasa A, derivados de capsaicina, metabolismo del cáncer