Clear Sky Science · es
MHC1-TIP permite el perfil multimodal del inmunopeptidoma en un solo tubo y revela heterogeneidad intratumoral en la presentación de antígenos
Mirando las tarjetas de identificación del cáncer
Cada célula lleva diminutas "tarjetas de identificación" moleculares en su superficie que ayudan al sistema inmunitario a decidir si esa célula es sana o peligrosa. En el cáncer, estas tarjetas—fragmentos proteicos cortos llamados antígenos—pueden revelar qué hace que una célula tumoral sea anómala y marcarla para su destrucción por células inmunitarias. Este estudio presenta un nuevo método de laboratorio, MHC1-TIP, que facilita y abarata la lectura de estas tarjetas a partir de cantidades muy pequeñas de tejido de pacientes, abriendo la puerta a inmunoterapias contra el cáncer más precisas.
Por qué importan las señales en la superficie celular
Nuestro sistema inmunitario inspecciona constantemente las células comprobando los antígenos que se muestran en moléculas especiales llamadas MHC clase I. Las células tumorales con frecuencia muestran antígenos inusuales que, en principio, pueden ser reconocidos por células T y ser diana de terapias como vacunas personalizadas. Sin embargo, medir realmente qué antígenos están presentes en muestras de pacientes ha sido técnicamente exigente. Los métodos tradicionales requieren un gran número de células, muchos pasos de procesamiento y anticuerpos caros, lo que los hace poco adecuados para biopsias diminutas o muestras clínicas escasas. Al mismo tiempo, los tumores no son uniformes: distintas regiones pueden expresar proteínas diferentes, lo que plantea la posibilidad de que la presentación de antígenos también varíe de un lugar a otro dentro de un mismo tumor.
Un atajo en un solo tubo hacia los antígenos tumorales
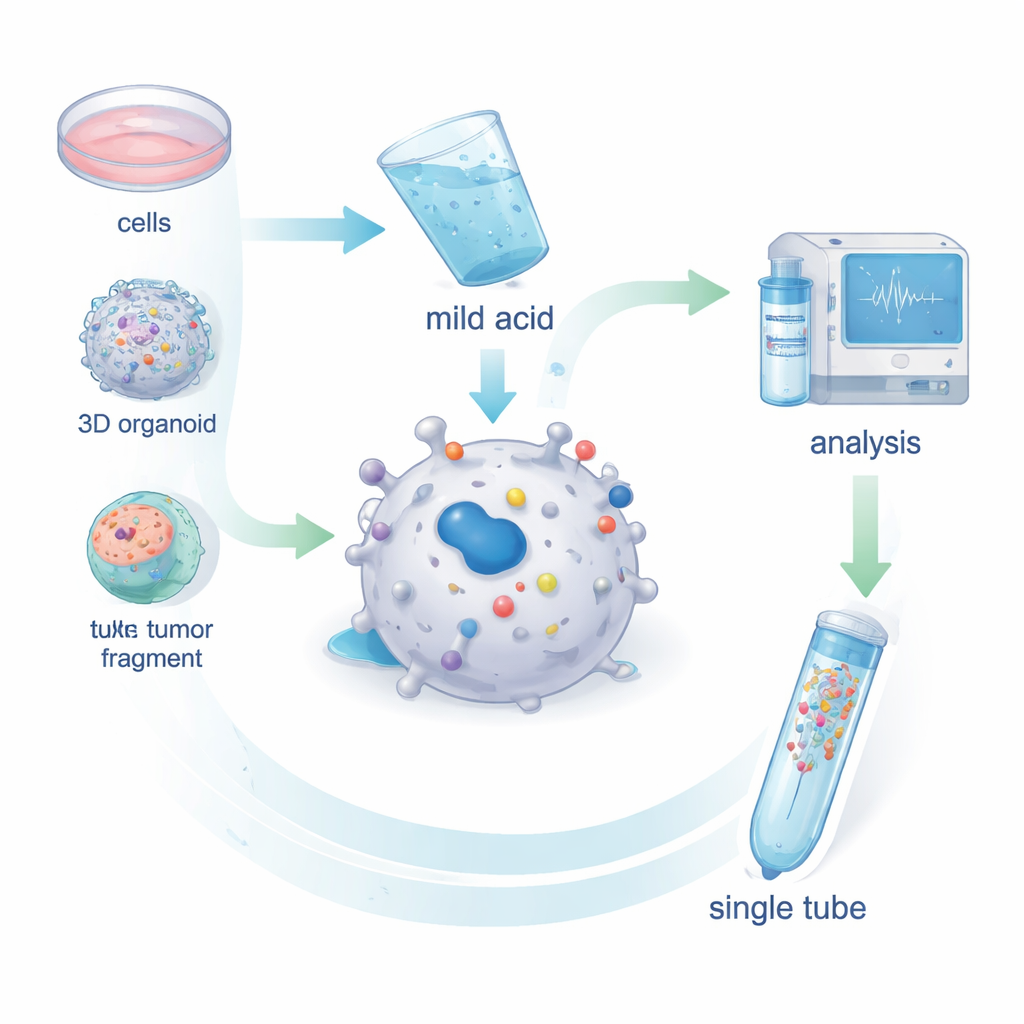
Los investigadores desarrollaron MHC1-TIP (MHC-I 1-Tube Immunopeptidomics) como una forma simplificada de recoger antígenos de células vivas. En lugar de romper las células y extraer las moléculas MHC con anticuerpos, lavan brevemente las células intactas—o pequeños fragmentos tumorales—con una solución ácida suave. Este tratamiento suave hace que los antígenos alojados en la hendidura del MHC se desprendan sin matar las células. Los péptidos liberados pasan entonces por un pequeño filtro que elimina los desechos mayores y quedan atrapados en una columna diminuta dentro de un solo tubo. Desde ahí, van directamente a un espectrómetro de masas, que identifica las secuencias peptídicas. Pruebas en células de melanoma mostraron que este paso de ácido suave elimina casi todos los complejos MHC–antígeno de la superficie y que los péptidos recuperados se parecen a los antígenos realmente unidos a MHC en cuanto a longitud y patrones de secuencia.
Más datos con menos muestra
MHC1-TIP fue diseñado para funcionar con muy pocas células y aun así entregar numerosos antígenos identificables. Al combinar el nuevo flujo de trabajo con un modo moderno de espectrometría de masas llamado adquisición independiente de datos, el equipo detectó cientos de antígenos a partir de solo 100.000 células y miles a partir de unos pocos millones de células—profundidad similar al método estándar de oro basado en anticuerpos, pero con menos material y menor coste. El método también funcionó en organoides derivados de pacientes, que son mini-tumores 3D cultivados en el laboratorio, y en diminutos fragmentos tumorales ex vivo más pequeños que un milímetro cúbico. Es importante destacar que, dado que el lavado ácido deja las células mayormente intactas, el material restante puede usarse para un perfil proteico a gran escala a partir de la misma muestra, permitiendo la comparación directa entre cuánto de una proteína dada está presente y cuánto de ella se presenta realmente como antígeno.
Diferencias ocultas dentro de un mismo tumor
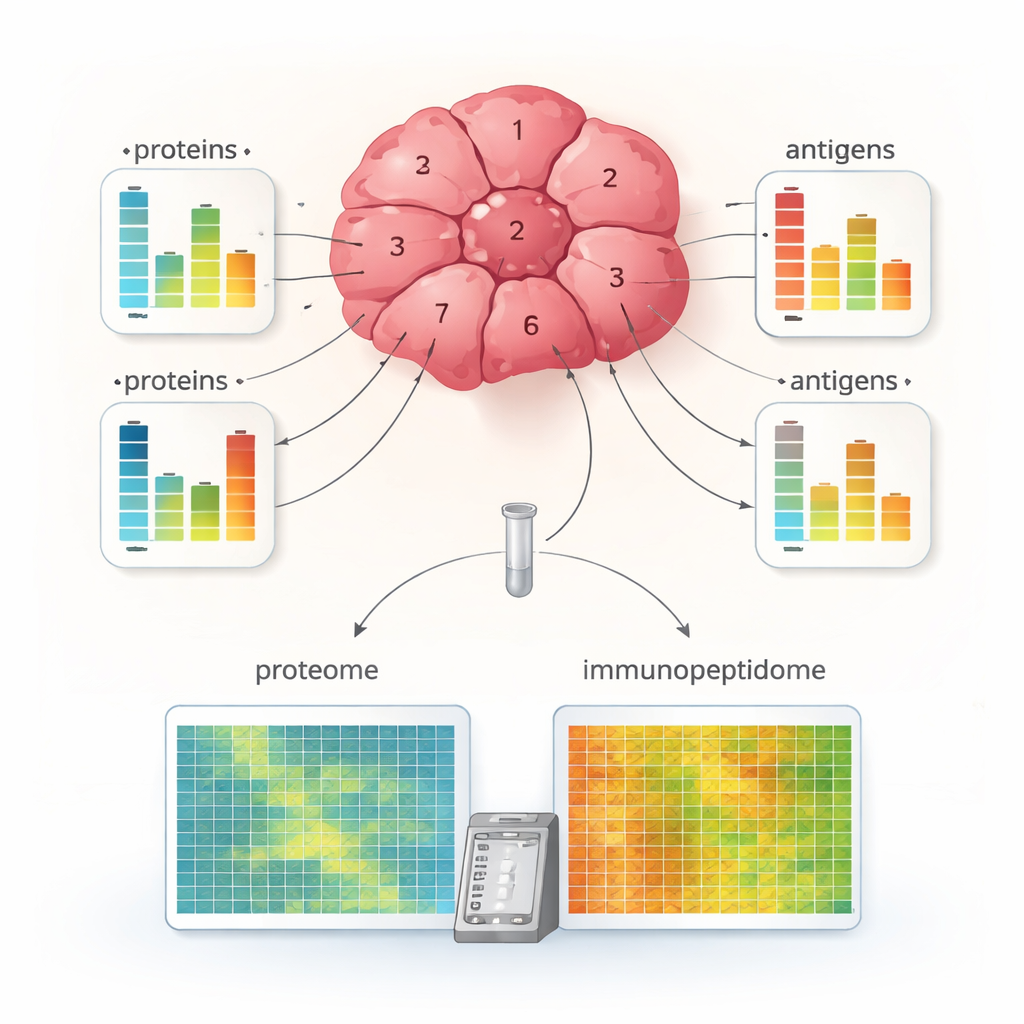
Aplicar MHC1-TIP a múltiples pequeños fragmentos tomados de diferentes regiones de un carcinoma de células renales reveló una marcada diversidad interna. Algunos fragmentos mostraron una rica presentación de antígenos, mientras que otros exhibieron muy pocos antígenos, aunque su contenido proteico global pudiera ser similar. Para muchas proteínas, los cambios en los niveles de antígenos no coincidieron con los cambios en su abundancia proteica, lo que sugiere que el procesamiento de antígenos y su carga sobre las moléculas MHC se regulan de forma independiente de cuánto de la proteína madre esté presente. El equipo también combinó los datos de antígenos con marcadores de células inmunitarias y de la maquinaria MHC, identificando regiones tumorales “calientes” inmunológicamente, con alta exhibición de antígenos y signos de células T activas, y regiones “frías”, con menos antígenos y menor evidencia de ataque inmune. Este nivel de detalle rara vez ha sido posible a partir de piezas tisulares tan pequeñas.
Qué significa esto para la atención oncológica futura
Para un no especialista, el mensaje principal es que medir simplemente qué proteínas produce un tumor no basta para saber lo que el sistema inmunitario puede ver. El nuevo método MHC1-TIP ofrece una manera práctica de leer la verdadera exhibición de antígenos a partir de muestras clínicamente realistas y muy pequeñas, al mismo tiempo que mide el panorama proteico más amplio. El descubrimiento de que la presentación de antígenos puede variar mucho entre distintas partes de un mismo tumor, y que no siempre sigue los niveles proteicos, advierte sobre elegir dianas para vacunas o células T basándose solo en la expresión génica o proteica. En el futuro, enfoques como MHC1-TIP podrían ayudar a diseñar inmunoterapias más efectivas y personalizadas al centrarse en antígenos que realmente se muestran en la superficie y se presentan de forma más consistente a lo largo del tumor.
Cita: Bathini, M., Bocaniciu, D., Johnson, F.D. et al. MHC1-TIP enables single-tube multimodal immunopeptidome profiling and uncovers intratumoral heterogeneity in antigen presentation. Commun Biol 9, 296 (2026). https://doi.org/10.1038/s42003-026-09570-6
Palabras clave: presentación de antígenos, inmunopeptidómica, inmunoterapia contra el cáncer, heterogeneidad tumoral, espectrometría de masas