Clear Sky Science · es
Reevaluación de la especificidad entre proteínas Gα y elementos de respuesta en la señalización GPCR
Por qué los pequeños interruptores celulares importan para la medicina
Muchos de los fármacos actuales actúan cambiando el estado de “interruptores” moleculares en la superficie de nuestras células denominados receptores acoplados a proteínas G, o GPCR. Estos interruptores transmiten mensajes al interior celular mediante proteínas ayudantes conocidas como proteínas G y, finalmente, activan o reprimen genes. Durante décadas, los investigadores han empleado pruebas sencillas que producen luz para ver qué proteínas G utiliza un fármaco o receptor dado. Este estudio plantea una pregunta básica pero crucial: ¿realmente nos están diciendo esas pruebas lo que creemos—y podemos seguir confiando en ellas al diseñar la próxima generación de medicamentos de precisión?
Cómo suelen interpretarse las señales GPCR
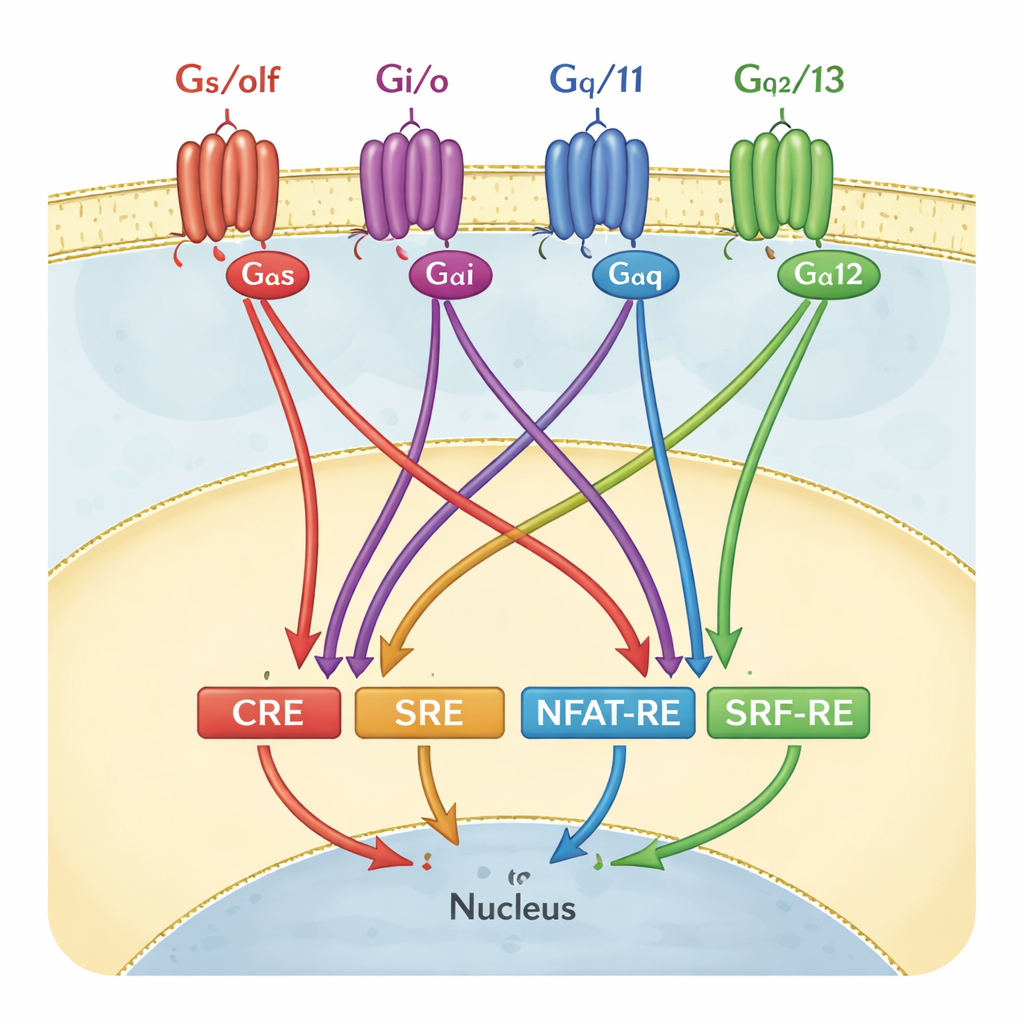
Para seguir la actividad de los GPCR, muchos laboratorios usan ensayos de genes reporteros. En estas pruebas, las células se modifican para que, cuando se activa un interruptor génico particular, o “elemento de respuesta”, las células emitan luz. Cuatro de esos interruptores son especialmente populares: CRE, SRE, NFAT‑RE y SRF‑RE. A cada uno se le ha considerado durante mucho tiempo representativo de una rama de la señalización por proteínas G—por ejemplo, CRE para la familia Gαs/olf, o SRF‑RE para Gα12/13. En manuales y en procesos de cribado, estos emparejamientos a menudo se dibujan casi como diagramas de cableado uno a uno: activas una proteína G específica y solo un reportero se enciende.
Poner a prueba el viejo diagrama de cableado
Los autores desafiaron sistemáticamente esta imagen usando células humanas HEK293 en las que se eliminaron con edición genética familias específicas de proteínas G—o incluso todas las proteínas G. Luego reintrodujeron tipos individuales de proteínas G una a una. En estas células expresaron nueve GPCR distintos, elegidos para representar receptores que señalizan de forma muy selectiva o a través de muchos socios de proteínas G. Midiendo la intensidad con la que cada uno de los cuatro reporteros brillaba a lo largo de múltiples concentraciones de fármaco, pudieron ver qué proteínas G eran realmente necesarias para cada elemento de respuesta y cuáles podían contribuir de forma indirecta.
Vías superpuestas en lugar de canales limpios
Los resultados derriban el modelo limpio de un receptor‑un reportero. Aunque CRE siguió dependiendo principalmente de las proteínas Gαs/olf—la clásica vía que eleva cAMP—otras familias de proteínas G pudieron influir notablemente en la actividad de CRE, pero solo cuando Gαs/olf estaba presente. Para los otros tres reporteros, SRE, NFAT‑RE y SRF‑RE, la familia Gαq/11 emergió como el principal impulsor, pese a que SRE y SRF‑RE se habían vinculado tradicionalmente a otras ramas de proteínas G. SRE y SRF‑RE se comportaron de manera especialmente similar, lo que sugiere que se alimentan de maquinaria downstream compartida en lugar de rutas distintas e aisladas. En muchos casos, proteínas G adicionales como Gα12/13 y Gαi/o aportaron empuje extra o actividad de fondo, poniendo de relieve una red de comunicación cruzada en lugar de canales separados.
Por qué la red celular difumina nuestras lecturas
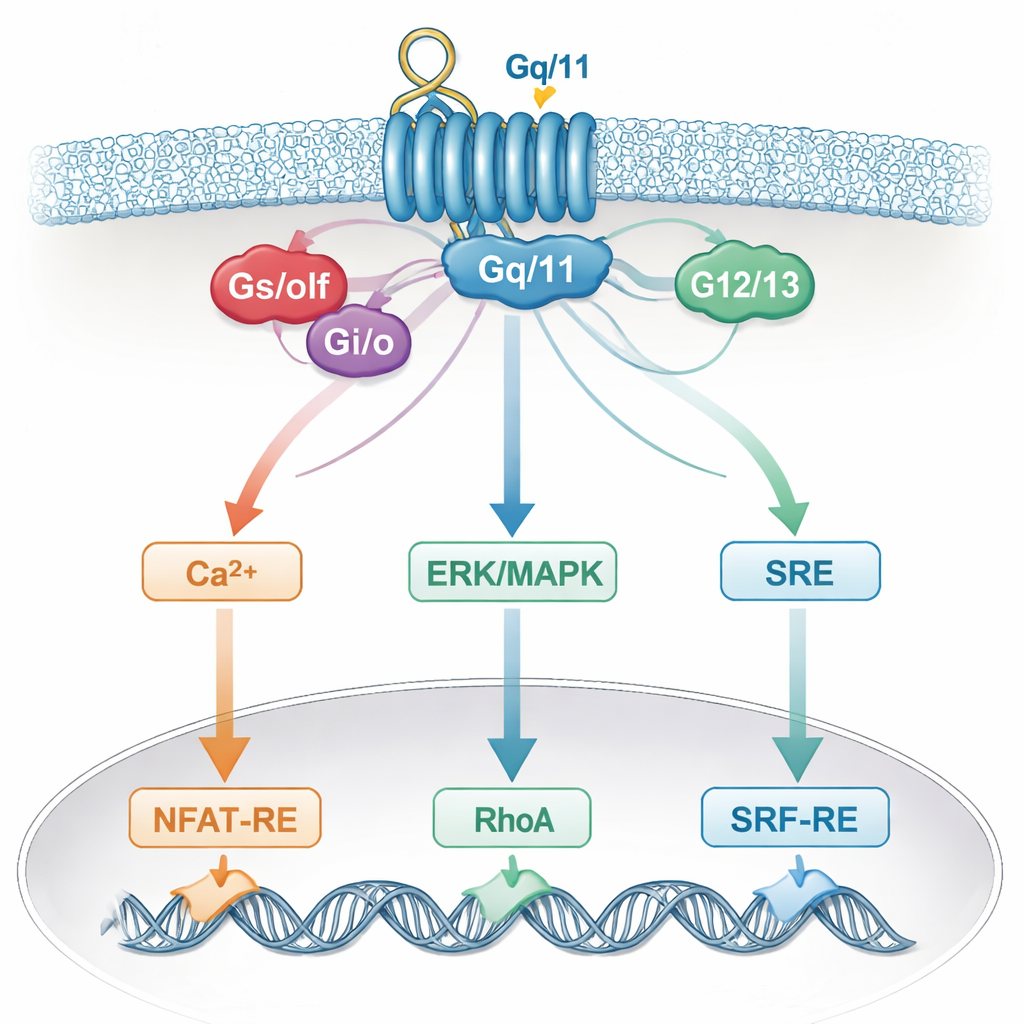
Esta especificidad difusa probablemente refleja cómo las células reales integran señales. Un único receptor puede activar múltiples proteínas G, que luego convergen en mensajeros comunes como el calcio, ERK/MAPK, RhoA o el cAMP, y en ayudantes compartidos como las subunidades Gβγ. Estas vías compartidas, a su vez, alimentan los mismos interruptores genéticos en el núcleo. Como resultado, un reportero que se pensaba que respondía a una familia de proteínas G en realidad “escucha” a varias. Factores específicos del tipo celular y el conjunto exacto de receptores presentes añaden aún más complejidad, lo que significa que las conclusiones extraídas de un sistema celular pueden no mantenerse en otro.
Qué implica esto para el descubrimiento de fármacos
Para los no especialistas, la idea clave es que muchas pruebas GPCR basadas en emisión de luz ampliamente usadas son menos específicas de lo que sus etiquetas sugieren. Aún pueden indicar que un receptor está activo y, de forma aproximada, qué vías generales están implicadas, pero no son una prueba fiable de que una familia concreta de proteínas G—y solo esa familia—esté involucrada. Los autores sostienen que los investigadores y desarrolladores de fármacos deberían tratar estos reporteros como indicadores groseros y combinarlos con métodos más directos que observen interacciones proteicas en tiempo real. Hacerlo ofrecerá una imagen más veraz de cómo los posibles medicamentos dirigen la señalización celular y ayudará a evitar atajos engañosos en la búsqueda de terapias más seguras y específicas.
Cita: Saito, A., Kise, R., Yamaguchi, S. et al. Re-evaluating Gα protein–response element specificity in GPCR signaling. Commun Biol 9, 288 (2026). https://doi.org/10.1038/s42003-026-09569-z
Palabras clave: Señalización GPCR, Proteínas G, ensayos reporteros, redes de señalización celular, descubrimiento de fármacos