Clear Sky Science · es
Ensayos celulares e isoforma-selectivos de quinasas acopladas a proteínas G para una evaluación integral de inhibidores
Por qué importa bajar los “volúmenes” celulares
Muchos de nuestros medicamentos actúan modulando al alza o a la baja la actividad de receptores en la superficie celular que detectan hormonas, neurotransmisores y fármacos. Es crucial apagar esos receptores con precisión para evitar la sobreestimulación celular; ese apagado está controlado en parte por enzimas llamadas GRK. Cuando las GRK están demasiado activas, como ocurre en la insuficiencia cardíaca y algunos cánceres, la señalización se altera. Este estudio desarrolla ensayos prácticos en células para medir cuánto pueden bloquear las moléculas experimentales GRK específicas, ayudando a los científicos a diseñar medicamentos más inteligentes que regulen con finura estos importantes “volúmenes” celulares.
Guardianes en la superficie celular
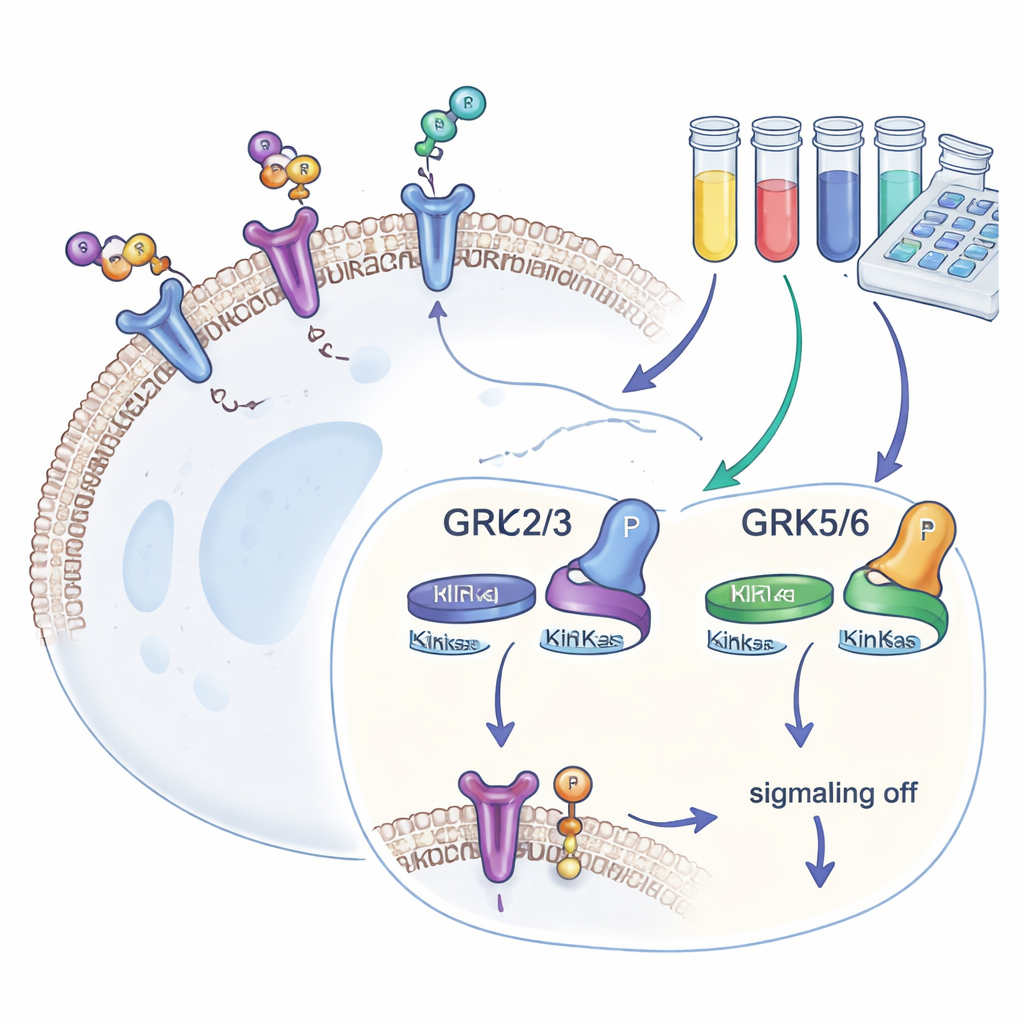
Nuestras células tienen cientos de tipos de receptores acoplados a proteínas G (GPCR), que detectan señales externas y las traducen en respuestas internas. Tras la activación de un GPCR, las GRK añaden pequeñas “banderas” de fosfato a su cola. Esas señales atraen a otra proteína, la beta-arrestina, que detiene la señalización y con frecuencia internaliza el receptor. Cuatro isoformas de GRK—GRK2, GRK3, GRK5 y GRK6—se encuentran en muchos tejidos. Debido a que influyen en la intensidad de la respuesta de los GPCR y porque sus niveles cambian en enfermedades como insuficiencia cardíaca, cáncer y adicción, los desarrolladores de fármacos buscan inhibidores de GRK que sean potentes y selectivos.
Construir un banco de pruebas limpio dentro de células
La mayoría de estudios previos sobre GRK se basaron en modelado por ordenador o en química de tubo de ensayo, que muestran con qué afinidad se une un inhibidor pero no cómo funciona dentro del denso interior de una célula viva. Para salvar esa brecha, los autores diseñaron células humanas HEK293 que carecen de las cuatro GRK comunes y reintrodujeron una sola isoforma de GRK a la vez. Cada línea celular también llevaba un receptor bien estudiado, el receptor beta-2 adrenérgico, etiquetado de modo que su fosforilación en un sitio específico de la cola (llamado T360/S364) pudiera leerse mediante un ensayo sensible basado en anticuerpos. Como este sitio es modificado solo por las GRK, la cantidad de fosfato presente sirve como una medida directa y cuantitativa de la actividad de cada isoforma de GRK dentro de células vivas.
Separando lo bueno, lo débil y lo inespecífico
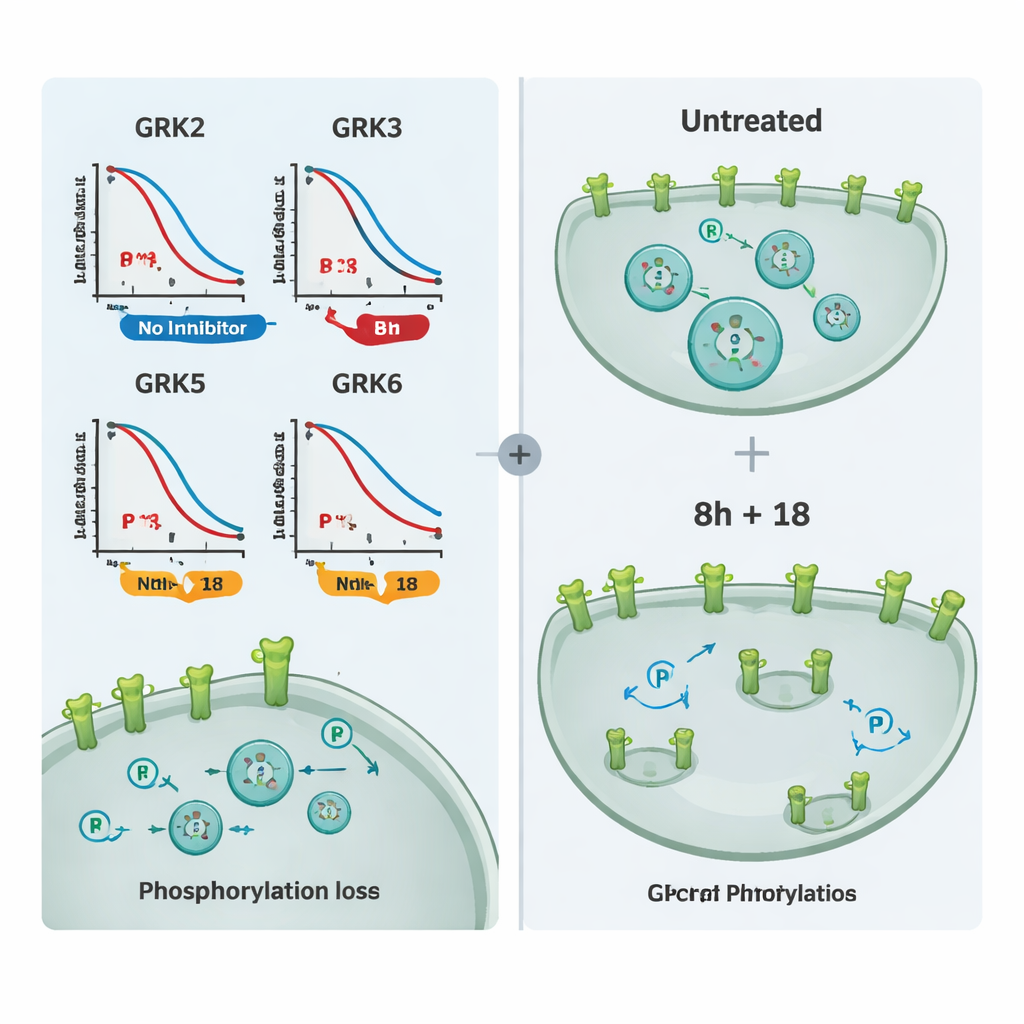
Con este conjunto de herramientas, el equipo probó un panel de inhibidores de GRK comercialmente disponibles. Primero agruparon compuestos que atacan principalmente GRK2 y GRK3, y otro grupo dirigido a GRK5 y GRK6. Al comparar cuánto reducía cada molécula la fosforilación del receptor en células que expresaban solo una subclase de GRK, pudieron trazar la selectividad en condiciones reales. Un compuesto, llamado 8h, surgió como el inhibidor más potente de GRK2/3, mientras que el compuesto 18 destacó por inhibir selectivamente GRK5/6. Algunas moléculas de uso frecuente mostraron poco efecto a las dosis probadas, probablemente porque no penetran bien en las células, y un inhibidor covalente muy potente perjudicó la salud celular, por lo que no fue adecuado para experimentos de imagen.
De las huellas químicas al comportamiento del receptor
Para demostrar que estos inhibidores afectan no solo a un receptor de prueba sino a la biología de los GPCR en general, los autores examinaron varios receptores de importancia médica, incluidos el receptor mu-opioide y el receptor de vasopresina V2. Midieron tanto la fosforilación como la internalización de receptores mediante microscopía. El compuesto 8h o el 18 por sí solos redujeron parcialmente la fosforilación y el movimiento hacia el interior de receptores de muchos objetivos, pero la combinación de 8h y 18 impidió casi por completo estos cambios y mantuvo los receptores en la superficie celular. Experimentos adicionales que rastrearon la reclutación de beta-arrestina confirmaron que los mismos compuestos pueden modular la señalización en otros receptores regulados por conjuntos solapados de GRK.
Qué significa esto para futuros medicamentos
Para no especialistas, el mensaje clave es que el estudio entrega un conjunto fiable de ensayos celulares—y dos compuestos herramienta especialmente útiles, 8h y 18—que permiten a los investigadores ver, en células vivas, cómo se atenúa exactamente cada isoforma de GRK. En lugar de deducirlo a partir de datos simplificados de tubo de ensayo, los científicos pueden ahora comparar candidatos lado a lado y decidir si afectan principalmente a GRK2/3, a GRK5/6 o a las cuatro a la vez. Esta claridad debería acelerar el desarrollo de fármacos que modulen con mayor precisión la señalización GPCR, con posibles beneficios para el tratamiento de enfermedades cardíacas, cáncer, trastornos del dolor y otras condiciones en las que el equilibrio de la señalización se ha descompensado.
Cita: Blum, N.K., Kiefer, M.C., Decker, A. et al. Cell-based and isoform-selective G protein-coupled receptor kinase assays for comprehensive inhibitor evaluation. Commun Biol 9, 287 (2026). https://doi.org/10.1038/s42003-026-09568-0
Palabras clave: Señalización GPCR, Inhibidores de GRK, Receptor beta-adrenérgico, Ensayo celular, Descubrimiento de fármacos