Clear Sky Science · es
HBP1 potencia la actividad del receptor de progesterona y la expresión de IGFBP1 impulsando la decidualización endometrial
Por qué esto importa para la fertilidad
Cuando comienza un embarazo, el embrión sólo puede implantarse en el útero si el revestimiento uterino ha sufrido una remodelación crucial llamada decidualización. Muchos casos de infertilidad y de fracaso repetido en la transferencia de embriones permanecen sin explicación, y evidencia creciente sugiere que el problema reside en esta remodelación más que en el embrión. Este estudio revela un «interruptor» molecular hasta ahora poco valorado, un factor de transcripción llamado HBP1, que ayuda a preparar el endometrio para la implantación y podría ofrecer nuevas vías para diagnosticar y tratar problemas de implantación.
Un interruptor oculto en el revestimiento uterino
El revestimiento interno del útero, el endometrio, cambia de forma rítmica con cada ciclo menstrual. Bajo la influencia del estrógeno crece, y bajo la progesterona madura hasta convertirse en una cama receptiva para el embrión. En este trabajo, los investigadores se centraron en las células del estroma endometrial humano, las células estructurales que se transforman en células deciduales más grandes y secretoras en el momento de la implantación. Al analizar datos de actividad génica existentes y realizar nuevos experimentos, encontraron que los niveles de HBP1 aumentan bruscamente cuando estas células estromales comienzan a decidualizar, lo que sugiere que HBP1 forma parte del sistema de temporización incorporado que prepara el útero.
Ayudando a las células a cambiar de forma y desacelerar
Para probar si HBP1 está simplemente presente o si es realmente necesario, el equipo moduló sus niveles al alza y a la baja en células del estroma endometrial humano cultivadas. Cuando HBP1 se redujo, marcadores clásicos de decidualización como IGFBP1, FOXO1 y prolactina cayeron tanto a nivel de ARN como de proteína. Las células tampoco sufrieron el cambio morfológico típico, de células delgadas y fusiformes a otras más anchas y poliédricas, y en su lugar siguieron proliferando. Cuando HBP1 se incrementó, los niveles de IGFBP1 aumentaron y la división celular se ralentizó. En conjunto, estos hallazgos muestran que HBP1 ayuda a las células a salir del modo de crecimiento y entrar en el estado decidual especializado que sostiene el inicio del embarazo.
Ajustando con precisión las señales hormonales dentro de la célula
La progesterona y su receptor son centrales para preparar el útero, pero no todos los tejidos responden igual a la hormona. Los investigadores descubrieron que la propia señalización de la progesterona aumenta los niveles de HBP1, creando un bucle de retroalimentación positiva. De forma llamativa, reducir HBP1 no cambió cuánto receptor de progesterona producían las células, pero sí atenuó la actividad de genes importantes sensibles a la progesterona, incluidos FKBP4, FKBP5, FOSL2 y el coactivador SRC1. Mediante enfoques genómicos, mostraron que HBP1 se une cerca de muchos de estos genes y se asocia con un aumento de una marca de histona específica, H3K4me3, que señala que el ADN está activo. En esencia, HBP1 no enciende ni apaga el receptor; facilita la lectura de los genes diana del receptor.
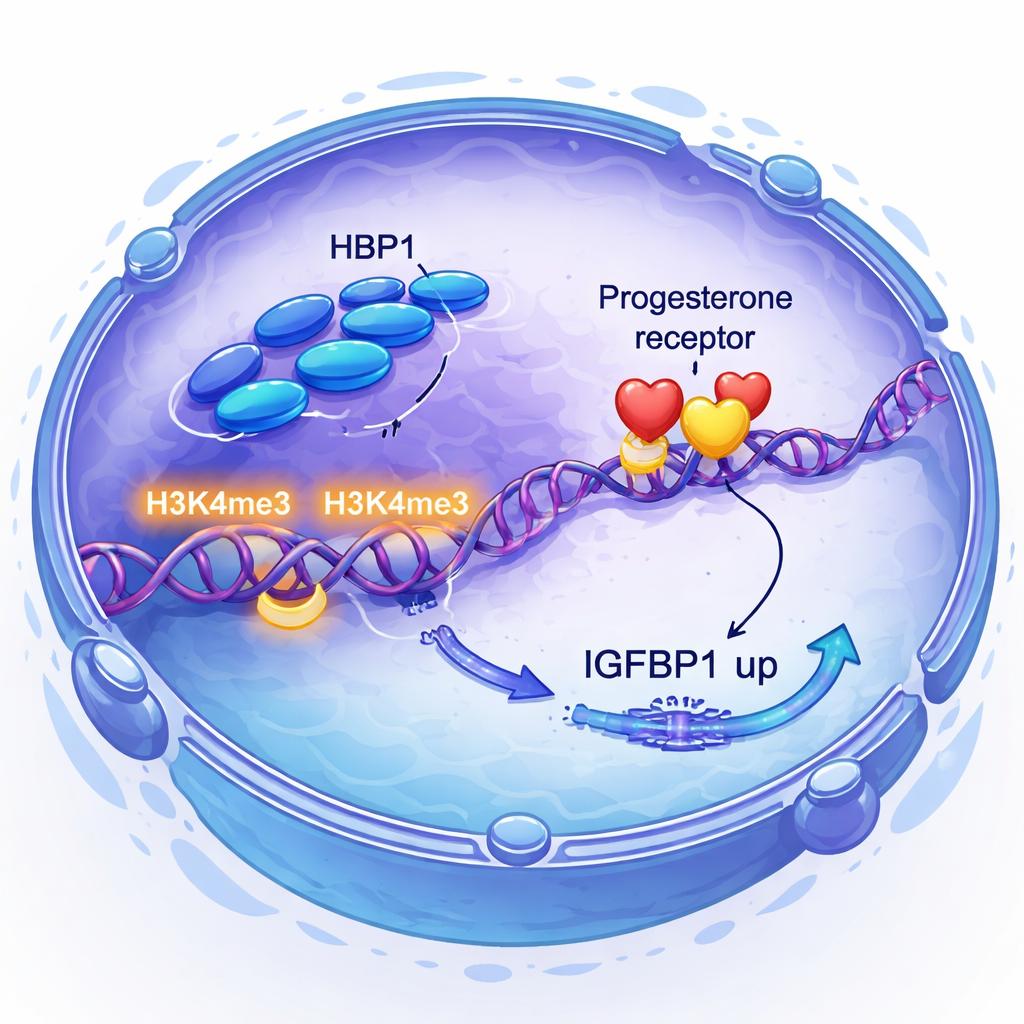
Control directo de una señal clave para la implantación
El equipo preguntó luego cómo conecta HBP1 con IGFBP1, una proteína utilizada desde hace tiempo como marcador de decidualización sana y conocida por influir en la comunicación embrión–útero. Al combinar secuenciación de ARN con secuenciación de inmunoprecipitación de cromatina, demostraron que HBP1 se sitúa directamente en la región promotora de IGFBP1 y aumenta allí H3K4me3, impulsando una mayor producción de IGFBP1. También encontraron que reducir HBP1 activó la vía PI3K–AKT, una señal relacionada con el crecimiento que, cuando está sobreactivada, suprime IGFBP1. Bloquear esta vía rescató los niveles de IGFBP1. Así, HBP1 apoya la decidualización de dos maneras: activando directamente IGFBP1 y amortiguando una señal de crecimiento que de otro modo frenaría los genes deciduales.
Vinculando un defecto molecular con la implantación fallida
Finalmente, los investigadores analizaron muestras endometriales de mujeres con fallo recurrente de implantación y las compararon con tejidos de controles fértiles durante la fase secretora media, lista para la implantación. Las mujeres con fallos repetidos mostraron niveles notablemente más bajos de HBP1 y de sus socios aguas abajo IGFBP1, FKBP5 y FOSL2, aunque los niveles del receptor de progesterona fueron similares entre los grupos. Este patrón encaja con la idea de «resistencia a la progesterona»: la hormona está presente, pero el tejido no puede montar una respuesta completa porque faltan factores clave de apoyo como HBP1.
Qué significa esto para las pacientes
En términos accesibles, este estudio sugiere que HBP1 actúa como un ajuste maestro en el panel de control del revestimiento uterino. Cuando está correctamente activado, ayuda a que las señales de progesterona se escuchen, anima a las células a dejar de dividirse y especializarse, y aumenta la producción de moléculas favorables a la implantación como IGFBP1. Cuando HBP1 es demasiado bajo, el endometrio puede parecer normal al microscopio pero funcionar mal, lo que lleva a que los embriones no logren establecerse. Comprender y medir HBP1 y su red podría, en el futuro, ayudar a los médicos a identificar a las mujeres con riesgo de problemas de implantación e inspirar nuevos tratamientos que restablezcan la receptividad del útero.
Cita: Guo, Y., Tian, W., Nie, C. et al. HBP1 enhances progesterone receptor activity and IGFBP1 expression driving endometrial decidualization. Commun Biol 9, 286 (2026). https://doi.org/10.1038/s42003-026-09567-1
Palabras clave: decidualización endometrial, implantación del embrión, señalización de la progesterona, infertilidad, HBP1