Clear Sky Science · es
Una división del trabajo en la integración percepción‑acción mediante un acoplamiento jerárquico alfa‑beta a beta‑gamma y control catecolaminérgico local
Cómo el cerebro enlaza ver y hacer
La vida cotidiana depende de decidir rápidamente si actuar o contenerse: frenar en un semáforo en rojo, ignorar una ventana emergente, impedir que la mano toque una sartén caliente. Este estudio pregunta cómo los ritmos internos del cerebro nos ayudan a alternar entre “ir” y “parar”, y cómo un fármaco común, el metilfenidato (MPH, conocido por su uso en el TDAH), modula esos ritmos para mejorar el autocontrol.
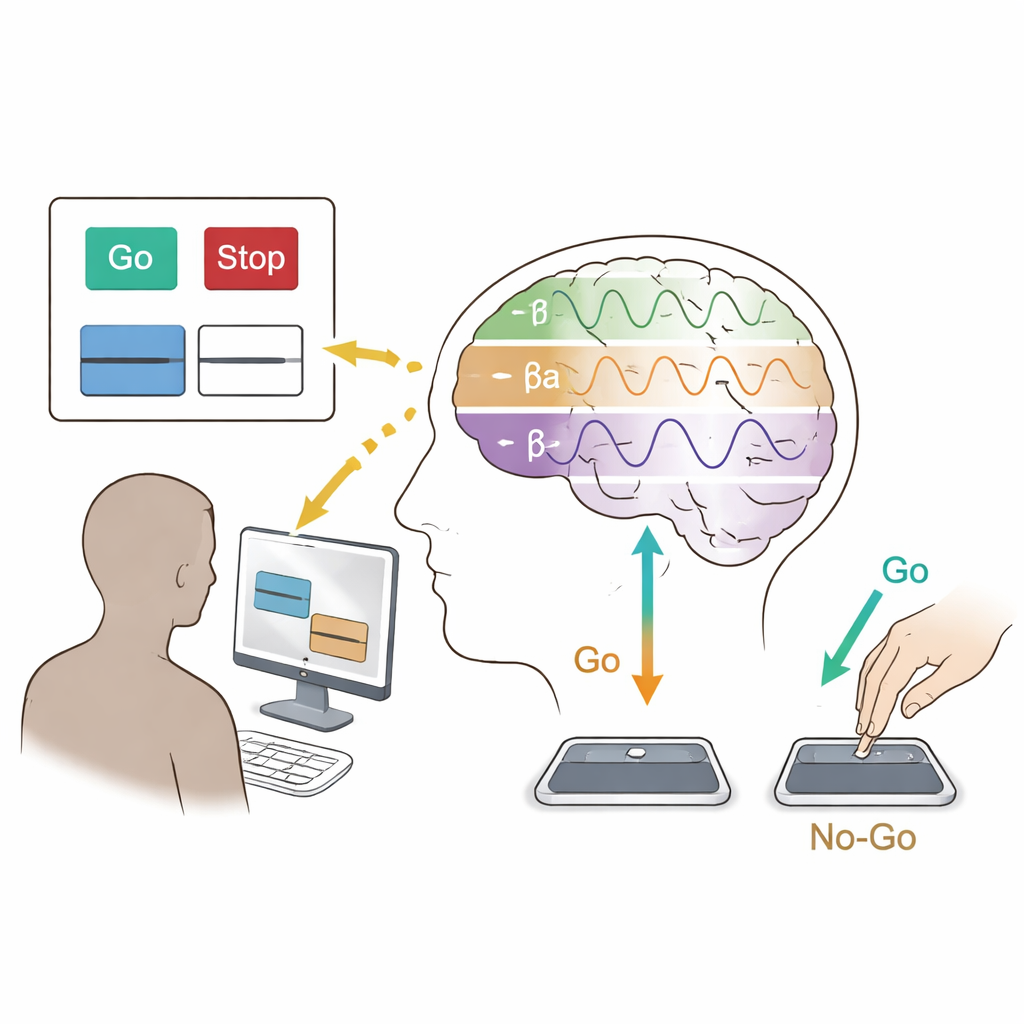
Parar, empezar y señales confusas
Los investigadores usaron una tarea por ordenador en la que los participantes o bien pulsaban una tecla (“Go”) o debían inhibir la respuesta (“No‑Go”). Algunas señales eran muy fáciles de distinguir: una palabra en verde que indicaba “pulsa” frente a una palabra en rojo que indicaba “para”. Otras eran más confusas, compartiendo colores o formas, de modo que “ir” y “parar” se parecían. En estos casos solapados, el cerebro tuvo que deshacer y reconstruir el enlace habitual entre lo que se ve y lo que se hace. Como era de esperar, las personas cometieron muchas más erratas —pulsando cuando no debían— cuando las señales se solapaban. Al tomar metilfenidato en lugar de placebo, cometieron menos de esos errores, especialmente en la condición más confusa y solapada, lo que indica que el fármaco mejoró la capacidad de parar en el momento adecuado.
Ritmos cerebrales que trabajan juntos
Mientras los participantes realizaban la tarea, el equipo registró su actividad cerebral con EEG. En lugar de fijarse solo en la potencia de cada ritmo, se centraron en cómo ritmos más lentos y más rápidos interactúan, un patrón llamado acoplamiento fase‑amplitud. En términos sencillos: ¿marcan las ondas lentas el momento para los estallidos de actividad más rápida, como un director que guía a la orquesta? Estudiaron cuatro bandas principales de ritmo frecuentemente asociadas al pensamiento y la acción: alfa, beta y gamma (más theta, que resultó menos relevante aquí). Encontraron que tres emparejamientos estaban especialmente activos cuando las personas intentaban detener acciones: acoplamientos alfa‑beta, alfa‑gamma y beta‑gamma, siendo beta‑gamma el más fuerte. Los acoplamientos relacionados con theta fueron débiles y no destacaron de forma fiable sobre el ruido.
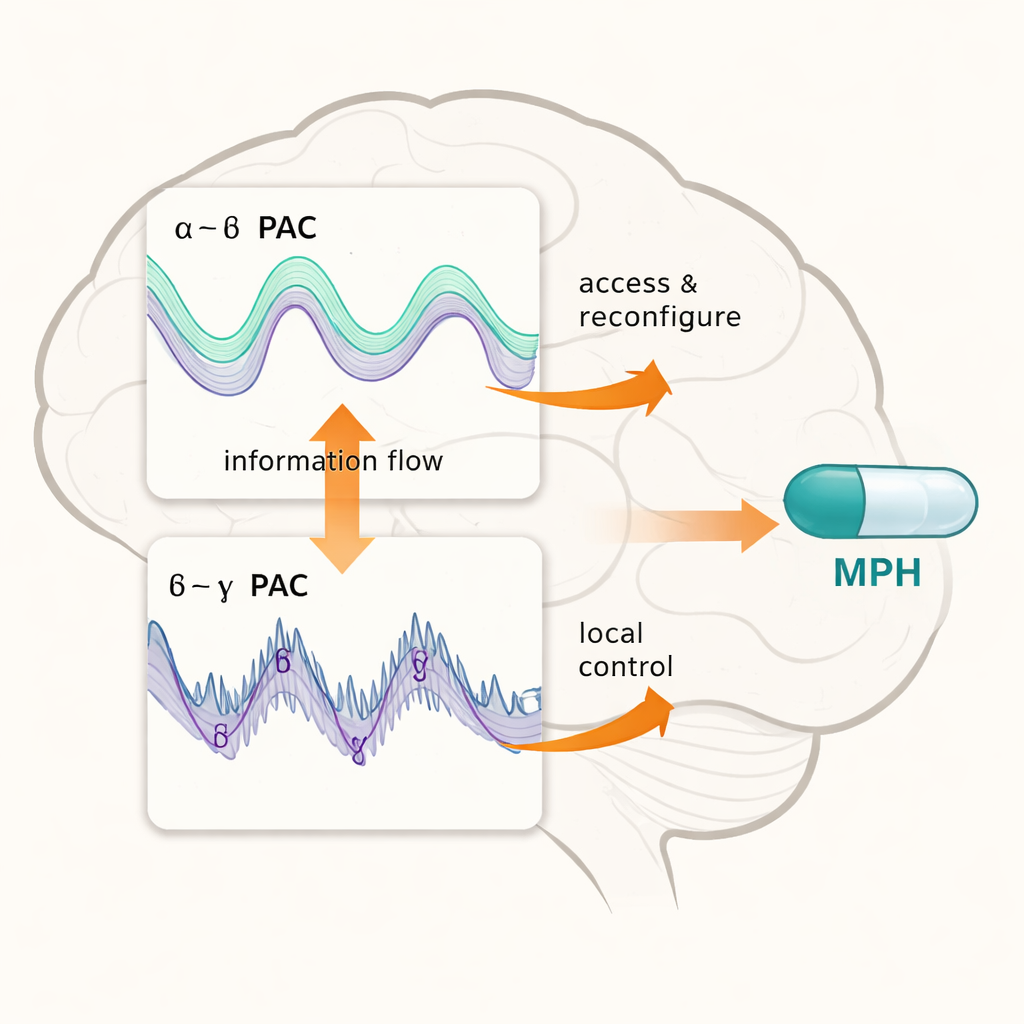
Una jerarquía temporal para el control flexible
Para entender cuándo importaban estos acoplamientos, los investigadores los siguieron a lo largo del tiempo tras la aparición de cada señal. El acoplamiento alfa‑beta mostró dos picos: uno temprano alrededor de 130–250 milisegundos después de la señal y otro tardío en torno a 530–770 milisegundos. El acoplamiento beta‑gamma fue principalmente más fuerte en este periodo tardío. Cuando las señales de “ir” y “parar” se solapaban y exigían un control más flexible, tanto alfa‑beta como beta‑gamma se intensificaron respecto a la condición fácil. Esto sugiere una división del trabajo: al principio, el acoplamiento alfa‑beta ayuda a acceder y ajustar el enlace entre percepción y acción; más tarde, el acoplamiento beta‑gamma contribuye a refinar y estabilizar el plan de acción actualizado. Usando un método de teoría de la información, los autores también hallaron que los cambios en el acoplamiento alfa‑beta tendían a predecir cambios posteriores en beta‑gamma, pero no al revés. Eso implica que ritmos más lentos (alfa‑beta) preparan el terreno para el funcionamiento de ritmos más rápidos (beta‑gamma), formando una cadena de control jerárquica en lugar de una red plana.
Cómo el medicamento ajusta el control local
El estudio también examinó cómo las catecolaminas —neuroquímicos como la dopamina y la noradrenalina, aumentados por el metilfenidato— interactúan con esta jerarquía rítmica. Bajo metilfenidato, el patrón global de flujo de información de alfa‑beta a beta‑gamma se mantuvo, y el propio acoplamiento alfa‑beta no cambió de forma fiable. Sin embargo, el acoplamiento beta‑gamma se fortaleció en ventanas temporales específicas, tanto en ensayos fáciles como difíciles. Las estimaciones de fuentes cerebrales apuntaron a regiones implicadas en la atención, la unión de características y el reinicio de estados, como partes de la corteza parietal y zonas mediales posteriores. En conjunto, esto sugiere que el fármaco no reescribe la jerarquía general de control, sino que afina los procesos locales donde los ritmos beta‑gamma ayudan a mantener y agudizar la representación activa de “hacer” o “no hacer”.
Qué significa esto para el autocontrol cotidiano
Para el público general, el mensaje principal es que el cerebro utiliza una división del trabajo cuidadosamente sincronizada para conectar lo que vemos con lo que hacemos. Los ritmos más lentos coordinan cuándo se accede y reconfigura la información, mientras que los ritmos más rápidos se encargan de los detalles finos y de la estabilidad del plan de acción elegido. El metilfenidato parece respetar la cadena de mando básica pero mejora la precisión de la etapa de control local. Comprender este sistema por capas puede ayudar a explicar por qué estos fármacos mejoran el autocontrol en condiciones como el TDAH y podría orientar enfoques futuros para apoyar un comportamiento flexible y dirigido a objetivos.
Cita: Zhupa, M., Beste, C. A division of labor in perception-action integration via hierarchical alpha-beta to beta-gamma coupling and local catecholaminergic control. Commun Biol 9, 284 (2026). https://doi.org/10.1038/s42003-026-09564-4
Palabras clave: inhibición de la respuesta, ritmos cerebrales, metilfenidato, integración percepción‑acción, control cognitivo