Clear Sky Science · es
El metabolito intestinal ácido indol-3-acético agrava el lupus neuropsiquiátrico vía la vía AHR/STAT3 en la microglía
Cómo los microbios intestinales pueden afectar la mente
Las personas con lupus, una enfermedad autoinmune, a veces desarrollan problemas graves con el pensamiento, el estado de ánimo y la memoria—una condición denominada lupus neuropsiquiátrico. Estos síntomas cerebrales pueden ser incapacitantes, y los médicos aún tienen dificultades para explicar exactamente por qué ocurren o cómo tratarlos. Este estudio explora a un culpable inesperado: ciertas bacterias intestinales y los compuestos que producen, que podrían viajar desde el intestino hasta el cerebro y avivar la inflamación allí.
De microbios intestinales a conducta alterada
Los investigadores comenzaron preguntando si los microbios intestinales de pacientes con lupus neuropsiquiátrico tienen efectos distintos de los de pacientes con lupus sin síntomas cerebrales. Trasplantaron bacterias fecales de cada grupo de pacientes a ratones sanos que previamente habían sido despojados de sus propios microbios intestinales. Los ratones que recibieron microbios de pacientes con lupus neuropsiquiátrico desarrollaron comportamientos más semejantes a la ansiedad, signos de depresión y problemas de aprendizaje y memoria que los ratones que recibieron microbios de otros pacientes con lupus. Sus cerebros mostraron una mayor activación de la microglía—las células inmunitarias del cerebro—y niveles más altos de moléculas inflamatorias. La barrera protectora alrededor del cerebro, conocida como barrera hematoencefálica, también era más permeable en estos animales, lo que sugiere que algo en la microbiota trasplantada dañaba esta barrera crítica.
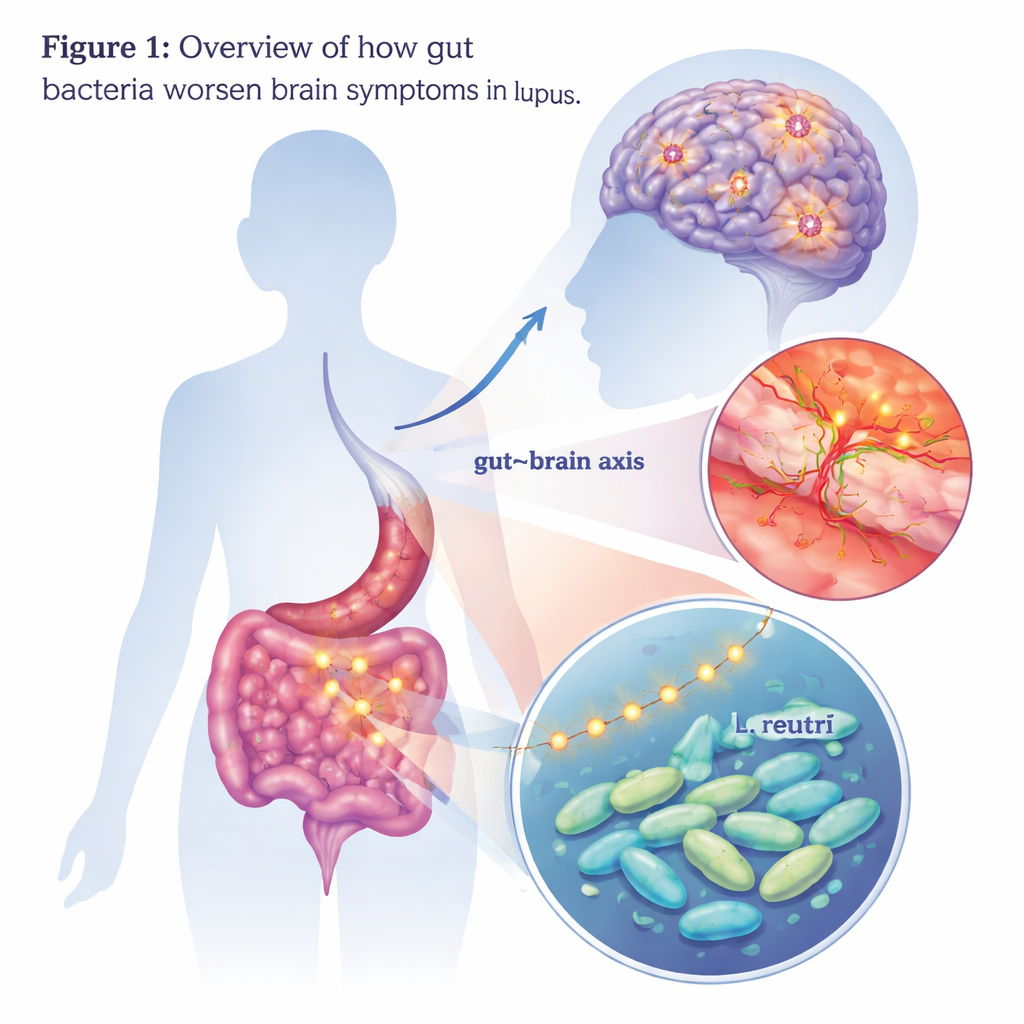
Enfoque en una sola bacteria
Para identificar qué microbios podrían ser responsables, el equipo comparó las comunidades bacterianas intestinales de pacientes y ratones. Un grupo destacó: Lactobacillus, y en especial una especie llamada Lactobacillus reuteri, era más abundante en pacientes con lupus neuropsiquiátrico y en ratones que mostraban cambios cerebrales. Cuando los científicos alimentaron solo con L. reuteri a ratones predispuestos al lupus, los animales desarrollaron comportamientos más marcados de ansiedad y depresión y obtuvieron peores resultados en pruebas de memoria. Sus cerebros mostraron mayor activación de la microglía, mayor pérdida de neuronas y una mayor alteración de la barrera hematoencefálica. Estos hallazgos sugieren que, al menos en el contexto del lupus, esta bacteria normalmente considerada beneficiosa puede asumir un papel más dañino.
Una molécula pequeña con grandes efectos
L. reuteri es conocida por producir un compuesto llamado ácido indol-3-acético (AIA) a partir del triptófano de la dieta. Mediante pruebas químicas sensibles, el equipo encontró niveles más altos de AIA en las heces de pacientes con lupus neuropsiquiátrico que en otros pacientes con lupus, y confirmaron que cultivos de L. reuteri producen mucho más AIA que bacterias intestinales comunes como Escherichia coli. En pacientes con lupus neuropsiquiátrico, los niveles de AIA en el líquido que rodea el cerebro y la médula espinal se correlacionaron con niveles más altos de citoquinas inflamatorias, lo que insinúa que esta molécula puede alcanzar el sistema nervioso central y desencadenar inflamación. En ratones predispuestos al lupus, alimentar con L. reuteri aumentó los niveles de AIA en el intestino, la sangre y el cerebro. Administrar AIA por sí solo a estos ratones reprodujo muchos de los mismos cambios: comportamientos anormales, activación de la microglía, señales inflamatorias elevadas y un debilitamiento de la barrera hematoencefálica e intestinal.
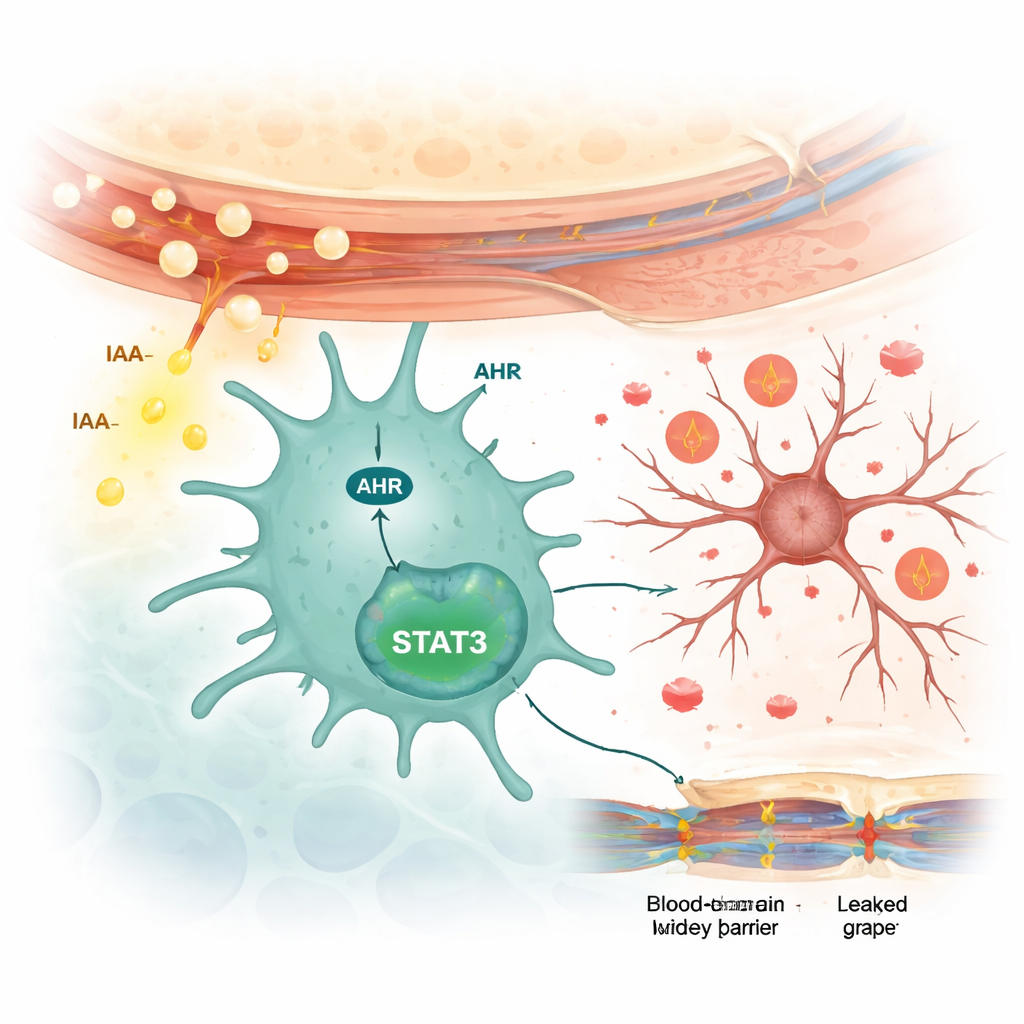
Cómo se activan las células inmunitarias cerebrales
Los científicos examinaron luego cómo comunica AIA con las células cerebrales. Encontraron que AIA aumentaba la actividad de una proteína sensora llamada receptor de hidrocarburos arílicos (AHR) específicamente en la microglía, no en las neuronas ni en las células de soporte estrelladas llamadas astrocitos. En microglía cultivada, AIA elevó los niveles de AHR y activó una proteína de señalización aguas abajo llamada STAT3, que a su vez impulsó la producción de citoquinas inflamatorias. Bloquear AHR con un fármaco impidió la activación de STAT3 y redujo la liberación de esas señales inflamatorias. Cuando ratones predispuestos al lupus fueron tratados con el fármaco bloqueador de AHR, sus comportamientos de ansiedad y depresión mejoraron, la activación microglial disminuyó, las moléculas inflamatorias se redujeron y la barrera hematoencefálica se volvió menos permeable.
Qué significa esto para los pacientes
En conjunto, el estudio describe una cadena de eventos que vincula el intestino con el cerebro en el lupus neuropsiquiátrico. Una sobreabundancia de L. reuteri en el intestino produce AIA adicional, que debilita la barrera intestinal y entra en el torrente sanguíneo. El AIA llega al cerebro, donde activa la señalización AHR/STAT3 en la microglía, desencadenando una inflamación que daña las neuronas y afloja la barrera hematoencefálica. Para los pacientes, estos hallazgos sugieren que alterar las bacterias intestinales, reducir metabolitos nocivos como el AIA o bloquear la vía AHR/STAT3 en la microglía podría, algún día, ayudar a proteger el cerebro de los devastadores efectos del lupus neuropsiquiátrico.
Cita: Feng, Y., Zheng, L., Tang, W. et al. Gut metabolite indole-3-acetic acid aggravates neuropsychiatric lupus via the AHR/STAT3 pathway in microglia. Commun Biol 9, 281 (2026). https://doi.org/10.1038/s42003-026-09561-7
Palabras clave: lupus neuropsiquiátrico, microbiota intestinal, Lactobacillus reuteri, inflamación de la microglía, barrera hematoencefálica