Clear Sky Science · es
La terapia dinámica estimulada por radionúclidos induce vías complementarias de muerte celular cáncerica: necroptosis inmunogénica y apoptosis
Volver las tretas del cáncer en su contra
El cáncer es famoso por eludir nuestros mejores tratamientos, sobre todo en tumores mamarios agresivos que se diseminan por todo el cuerpo. Este estudio explora un enfoque ingenioso llamado terapia dinámica estimulada por radionúclidos (RaST), que emplea trazadores usados en imagen médica y nanopartículas activadas por luz para matar células cancerosas de formas que además despiertan al sistema inmunitario. Para el lector, este trabajo importa porque sugiere cómo herramientas de imagen existentes y materiales inteligentes podrían reconvertirse para lograr un control del cáncer más duradero y mediado por la inmunidad, en lugar de una simple reducción temporal del tumor.
Una nueva forma de iluminar los tumores desde dentro
Los tratamientos oncológicos basados en luz tradicionales solo funcionan donde un haz externo puede llegar, como la piel o tumores superficiales. RaST sortea esta limitación usando un azúcar radioactivo, similar al trazador ya empleado en PET, que se acumula de forma natural en las células cancerosas de rápido crecimiento. A medida que este trazador atraviesa el tumor, emite un tenue resplandor azulado conocido como radiación Cherenkov. Los investigadores diseñaron diminutas nanopartículas de dióxido de titanio recubiertas con una proteína que dirige al tumor para que también se concentren allí. Cuando el trazador y las nanopartículas se encuentran, la luz interna activa las partículas, que a su vez generan ráfagas de especies reactivas de oxígeno —moléculas altamente reactivas que dañan las células cancerosas desde el interior.
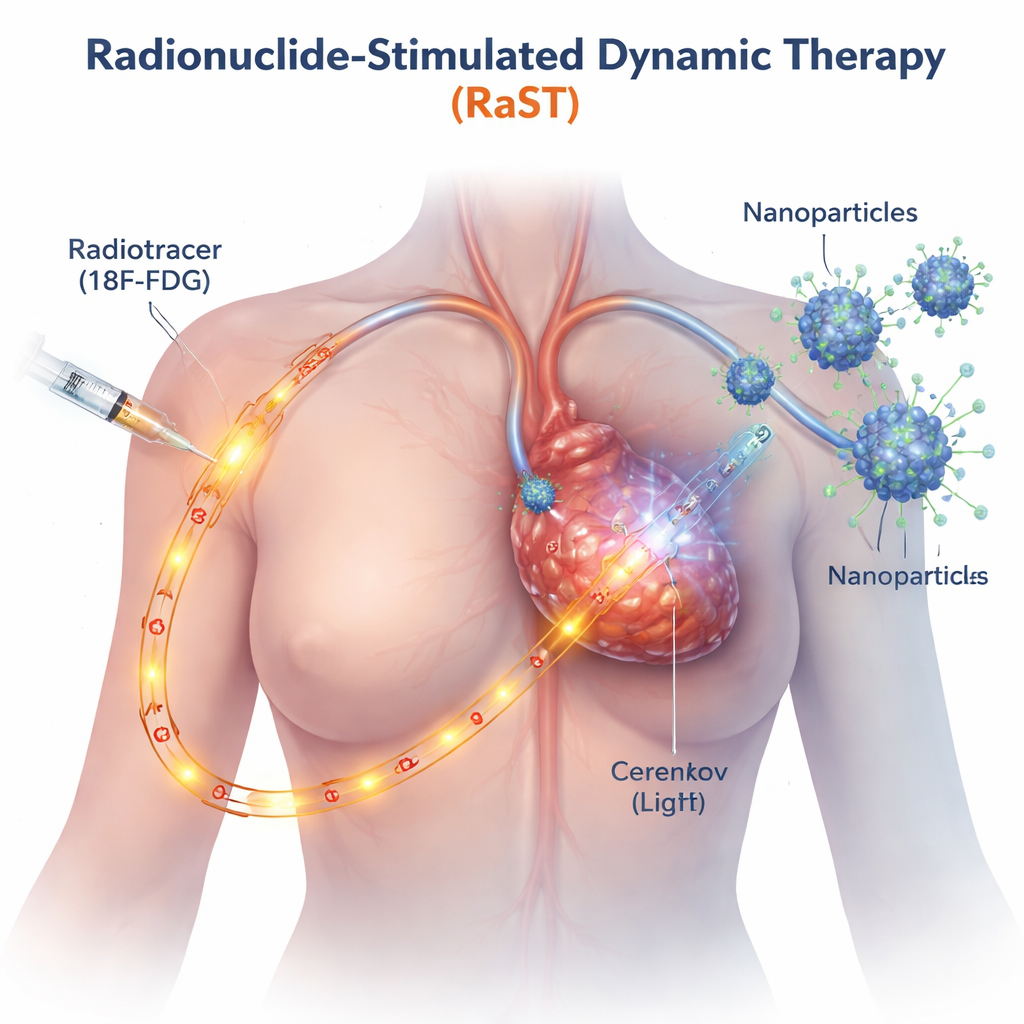
Activando dos vías distintas de muerte celular
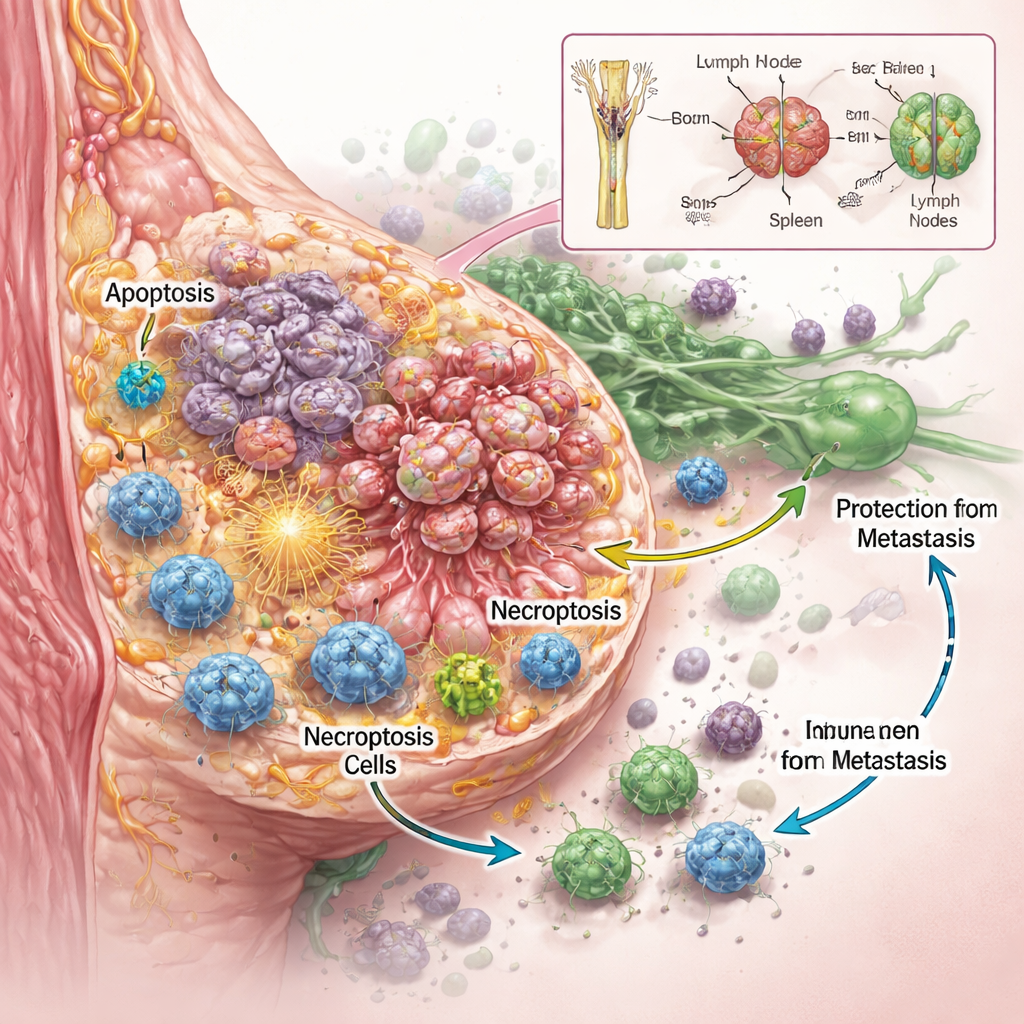
El equipo quiso saber no solo si RaST mataba células cancerosas, sino cómo lo hacía. Usando varias líneas celulares de cáncer de mama agresivo en el laboratorio, hallaron que dosis cuidadosamente ajustadas del trazador radioactivo y las nanopartículas actuaban en conjunto para dañar las células tumorales más eficazmente que cada componente por separado, incluso en tipos conocidos por resistir la quimioterapia estándar. Imágenes detalladas y mediciones de proteínas revelaron que RaST activaba simultáneamente dos programas regulados de muerte celular. Uno fue la apoptosis, a menudo descrita como el “suicidio” celular, donde las células se desmontan de forma ordenada. El otro fue la necroptosis, una forma más explosiva de muerte celular en la que las células se hinchan, se rompen y liberan señales de alarma moleculares a su alrededor. Estas señales, conocidas como moléculas asociadas al daño y citocinas inflamatorias, pueden actuar como bengalas que atraen y activan células del sistema inmunitario.
Movilizar al sistema inmunitario para un control duradero
Para comprobar si este estilo inflamatorio de eliminación tumoral tenía importancia en organismos vivos, los investigadores probaron RaST en modelos murinos de cáncer de mama. En ratones carentes de defensas inmunitarias clave, RaST hizo poco para frenar el crecimiento tumoral o la diseminación a los pulmones, a pesar de generar abundante muerte celular local. Pero en ratones con sistemas inmunitarios intactos, el mismo tratamiento produjo respuestas tumorales parciales y completas y previno la metástasis a los pulmones. Los tumores expuestos a RaST se llenaron de células inmunitarias —especialmente células mieloides como macrófagos y células dendríticas— que son hábiles en engullir material muerto y presentar fragmentos tumorales a los linfocitos T. Análisis de sangre mostraron oleadas de señales estimulantes y reguladoras de la inmunidad a lo largo del tiempo, lo que sugiere que RaST primero desencadena un ataque contra el cáncer y después evoluciona hacia un estado más equilibrado a medida que los tumores se reducen o se estabilizan.
Rastrear remanentes ocultos y proteger contra la recaída
Incluso en ratones donde los tumores parecían curados por completo por RaST, un tinte de imagen altamente sensible reveló más tarde pequeños focos de células cancerosas residuales alojadas en ganglios linfáticos. De manera notable, estos animales no desarrollaron nuevos tumores ni metástasis a distancia durante muchos meses. Los análisis químicos mostraron que las nanopartículas de dióxido de titanio, inicialmente abundantes en huesos e hígado, se redistribuyeron gradualmente al bazo y a los ganglios linfáticos —precisamente los centros donde patrullan las células inmunitarias. Esa lenta migración probablemente mantiene una fuente local de oxígeno reactivo disponible para las células inmunitarias, ayudándolas a reconocer y controlar estos remanentes cancerosos ocultos antes de que puedan reproducirse o diseminarse.
Qué podría significar esto para la atención oncólogica futura
En términos sencillos, este trabajo demuestra que RaST es más que otra forma de envenenar células tumorales. Al combinar trazadores radioactivos, nanopartículas sensibles a la luz y las defensas del propio organismo, empuja a las células cancerosas hacia dos formas de muerte programada que alertan en voz alta al sistema inmunitario. En animales con sistemas inmunitarios competentes, esto conduce a un control duradero de tumores mamarios agresivos y bloquea la metástasis, incluso cuando unas pocas células cancerosas persisten en ganglios linfáticos. Aunque queda mucho por hacer antes de que este enfoque pueda ensayarse ampliamente en humanos, el estudio apunta a tratamientos futuros que no se limiten a reducir tumores, sino a reconfigurar la relación entre cáncer, muerte celular e inmunidad para que el propio cuerpo ayude a mantener la enfermedad bajo control a largo plazo.
Cita: Egbulefu, C., Black, K., Su, X. et al. Radionuclide-stimulated dynamic therapy induces complementary immunogenic necroptosis and apoptosis cancer cell death pathways. Commun Biol 9, 275 (2026). https://doi.org/10.1038/s42003-026-09555-5
Palabras clave: cáncer de mama, nanopartículas, inmunoterapia, terapia con radionúclidos, necroptosis