Clear Sky Science · es
La glicofagia es una vía bilateria ancestral que sostiene la adaptación metabólica mediante la evolución estructural de STBD1
Cómo las ostras revelan trucos energéticos ocultos
Los animales sobreviven a tiempos difíciles recurriendo a combustible almacenado, pero no todos dependen del mismo tipo de “batería”. Este estudio examina la ostra del Pacífico y muestra que, a diferencia de muchos otros animales que se apoyan en la grasa, las ostras dependen en gran medida del azúcar almacenado en forma de glucógeno. El trabajo pone al descubierto una ruta celular poco conocida —denominada glicofagia— que ayuda a las ostras a vaciar y rellenar rápidamente sus reservas de azúcar, y traza cómo este sistema evolucionó a lo largo del reino animal.
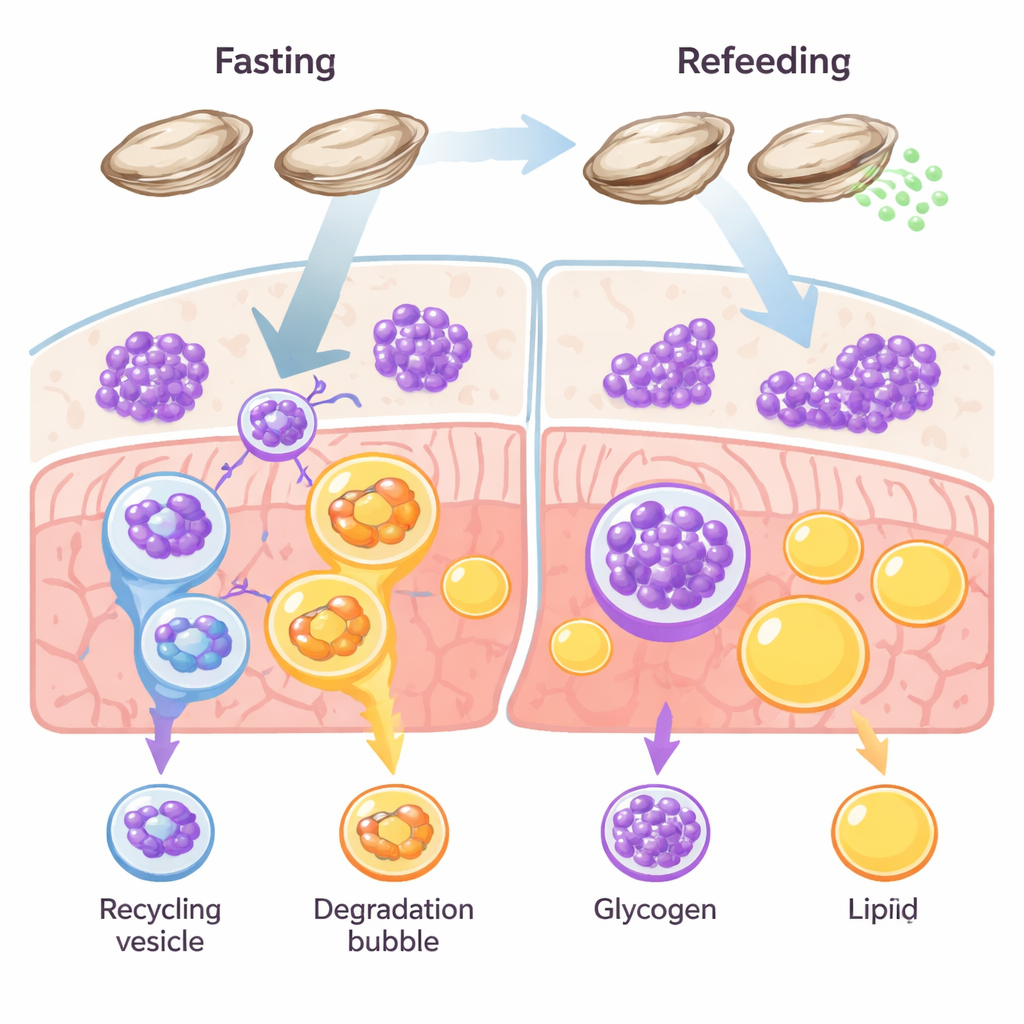
Una estrategia de supervivencia centrada en el azúcar
La mayoría de los animales gestionan varias reservas de energía, principalmente grasa y glucógeno. En vertebrados como peces y mamíferos, la grasa suele dominar como reserva a largo plazo. Las ostras rompen esta regla. Sus tejidos están llenos de glucógeno, y trabajos previos sugerían que estos moluscos consumen azúcar, en lugar de grasa, cuando la comida escasea o cuando producen huevos y esperma. Los autores se propusieron comprobar si la glicofagia —una degradación dirigida del glucógeno dentro de las células— actúa como una vía principal de supervivencia en ostras durante el ayuno y la recuperación posterior.
Observando cómo las células pasan del almacenamiento al gasto
El equipo privó de alimento a ostras del Pacífico durante dos semanas y luego las alimentó de nuevo, siguiendo cómo respondían sus tejidos a lo largo del tiempo. Durante el ayuno, coloraciones microscópicas mostraron un aumento de marcadores de autofagia —señales de “limpieza” celular— precisamente donde se almacenaba el glucógeno, mientras que el propio glucógeno disminuía. Las reservas de grasa, en contraste, apenas cambiaron. Cuando las ostras volvieron a alimentarse, el glucógeno reapareció rápidamente y las señales de autofagia cayeron. Al mismo tiempo, los niveles de una proteína receptora clave llamada STBD1, que conecta específicamente el glucógeno con la maquinaria de autofagia, aumentaron y disminuyeron al compás del uso del glucógeno. Otro receptor vinculado al reciclaje de grasas, p62, se mantuvo en gran medida estable. En conjunto, estos patrones apuntan a una ruta de reciclaje dedicada y centrada en el azúcar: la glicofagia, no la lipofagia (descomposición de grasa), realiza el trabajo principal en el balance energético de la ostra.
El gancho molecular que captura el glucógeno
La glicofagia depende de que STBD1 actúe como un gancho molecular: se une al glucógeno y lo entrega a pequeñas proteínas adaptadoras que construyen vesículas de reciclaje. En las ostras, STBD1 resultó estar cableada de forma diferente respecto a su homóloga en vertebrados. La proteína de la ostra lleva su región captadora de glucógeno, conocida como dominio CBM20, en el extremo delantero (N-terminal), mientras que STBD1 vertebrada sitúa este mismo módulo en el extremo trasero (C-terminal) e incorpora una cola extra hidrofóbica que la ancla a membranas celulares. Modelos por ordenador y simulaciones sugirieron que la disposición N-terminal de la ostra confiere al CBM20 un agarre más fuerte y versátil sobre las cadenas de azúcar ramificadas. Experimentos de laboratorio respaldaron esto: STBD1 purificada de ostra se unió al glucógeno con más afinidad que STBD1 de pez o ratón, y cuando todas las versiones se expresaron en células humanas, la proteína de ostra provocó una caída más marcada del glucógeno durante la autofagia inducida.
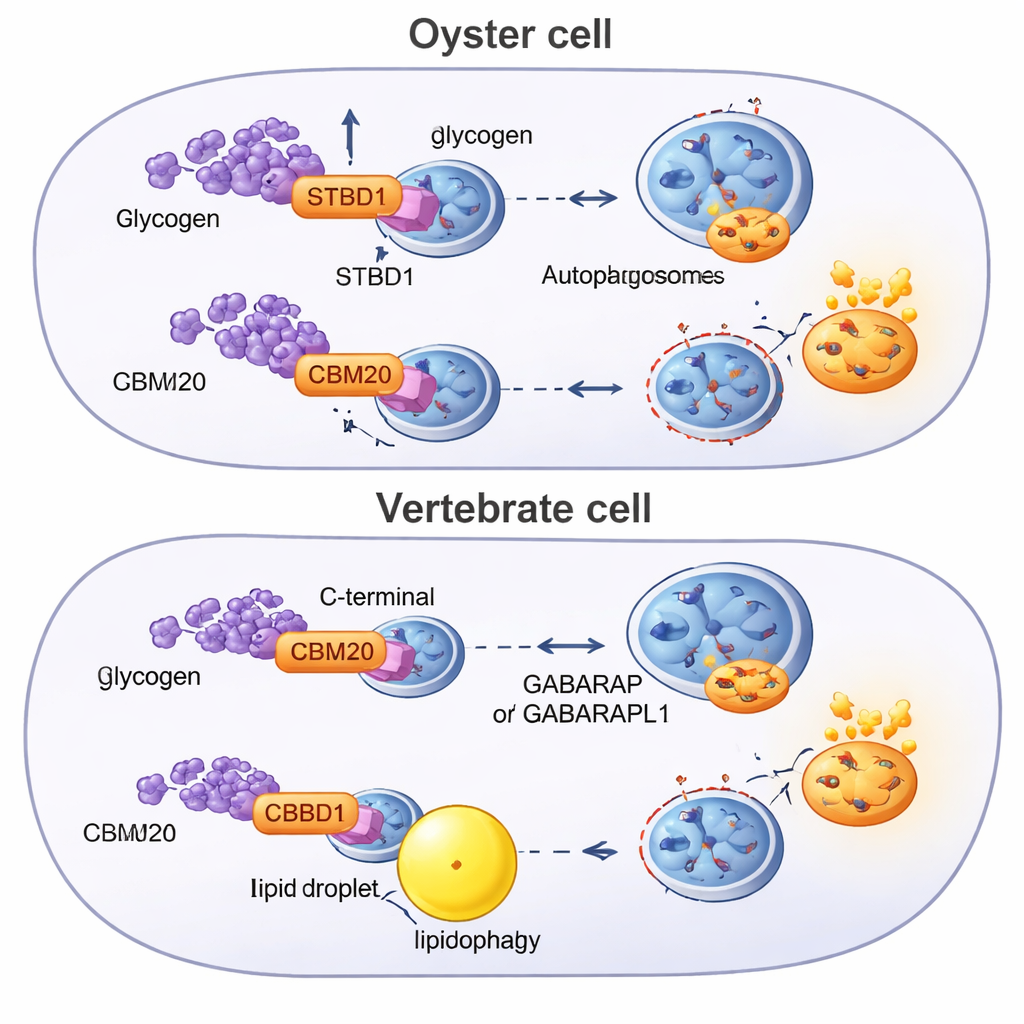
Reconectando una vía ancestral a lo largo de los animales
Para entender de dónde procede este sistema, los investigadores examinaron genomas de decenas de animales en busca de proteínas que contuvieran CBM20 y construyeron árboles evolutivos. Hallaron que STBD1 es una invención de los bilaterios —apareció en el ancestro común de los animales con planos corporales bilaterales— pero su estructura ha sido reordenada en distintas líneas. Las ostras y otros lophotrocozoos tienden a conservar el diseño ancestral con CBM20 en el N-terminal, a veces incluso duplicando el módulo de unión al azúcar. Los cordados, el grupo que incluye a los vertebrados, muestran una versión distinta en la que CBM20 se ha desplazado a la cola de la proteína. Este reordenamiento se correlaciona con una unión al glucógeno más débil y con una estrategia metabólica que recae más en la descomposición de grasas mediante lipofagia, respaldada por otros receptores y adaptadores de autofagia que las ostras no poseen.
Qué significa esto para las elecciones energéticas de la vida
Para el público general, la conclusión es que los animales han evolucionado más de una manera de soportar la escasez de energía. Las ostras muestran una estrategia antigua centrada en el azúcar: una versión de alta afinidad de STBD1 captura el glucógeno con rapidez y lo alimenta a las unidades de reciclaje celular, convirtiendo a la glicofagia en una fuente principal de energía durante el estrés. Los vertebrados, en cambio, parecen haber cambiado parte de esa fuerte sujeción al azúcar por un enfoque más equilibrado o inclinado a la grasa, respaldado por distintos socios proteicos y configuraciones de dominios. Al vincular la estructura detallada de proteínas con las elecciones de combustible a nivel de organismo, este estudio ilustra cómo pequeños “reordenamientos” moleculares pueden ayudar a diferentes ramas del árbol animal a adaptarse a sus propios entornos y estilos de vida.
Cita: Ren, L., Bai, Y., Shi, C. et al. Glycophagy is an ancient bilaterian pathway supporting metabolic adaptation through STBD1 structural evolution. Commun Biol 9, 268 (2026). https://doi.org/10.1038/s42003-026-09546-6
Palabras clave: glicofagia, metabolismo del glucógeno, biología de la ostra, autofagia, evolución del metabolismo