Clear Sky Science · es
Reprogramación epigenética y metabólica en feocromocitomas y paragangliomas metastásicos impulsada por mutaciones en SDHB
Por qué importan estos tumores raros
Los feocromocitomas y paragangliomas son tumores poco frecuentes que se originan en células nerviosas productoras de hormonas, a menudo cerca de las glándulas suprarrenales. La mayoría crecen de forma lenta y pueden curarse con cirugía, pero aproximadamente uno de cada cinco llega a diseminarse a otros órganos, volviéndose potencialmente mortal. Este estudio plantea una pregunta simple pero crucial: ¿qué hace que algunos de estos tumores se vuelvan peligrosos? Al indagar en cómo estos cánceres encienden y apagan genes y cómo obtienen su combustible, los investigadores descubren una debilidad oculta que podría, algún día, ser blanco de nuevas terapias.
Del crecimiento silencioso a la diseminación letal
El equipo se centró en tumores con alteraciones en un gen llamado SDHB. SDHB ayuda a las mitocondrias —las plantas de energía de la célula— a ejecutar parte del ciclo de Krebs, una vía central de producción de energía. Cuando SDHB está dañado, se acumula una molécula llamada succinato y las células pasan a comportarse como si vivieran con bajo oxígeno, incluso cuando no es así. Los investigadores estudiaron tejido de 34 pacientes, comparando tumores localizados con otros que ya se habían diseminado. Mediante un mapa de metilación del ADN de alta resolución, que muestra cómo las etiquetas químicas regulan la actividad génica, hallaron que los tumores metastásicos presentaban un patrón más intenso de silenciamiento génico que los benignos, especialmente cuando SDHB estaba mutado.
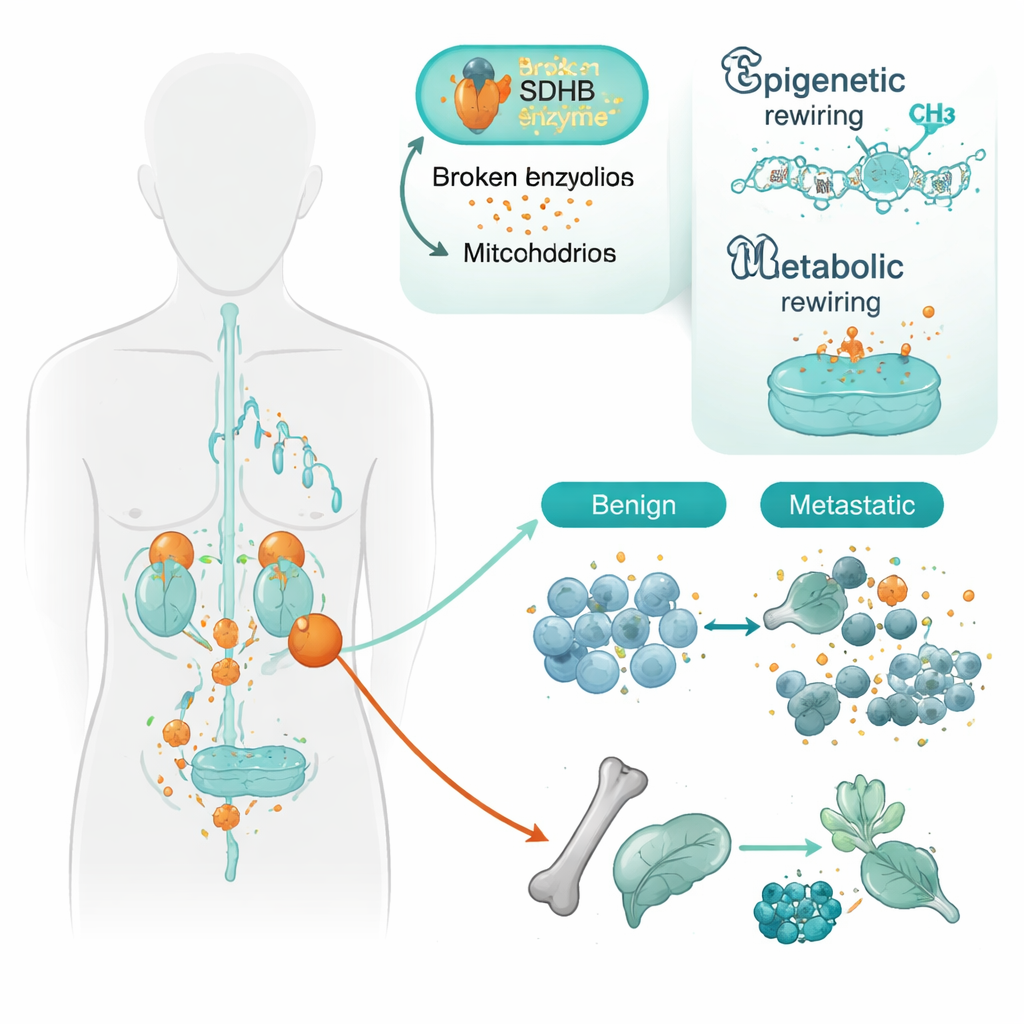
Reprogramación de la identidad celular
Muchos de los genes silenciados en tumores agresivos eran aquellos que ayudan a las células de tipo nervioso a madurar y mantener su identidad especializada. Incluyen familias génicas que orientan cómo las células se adhieren entre sí, organizan su ADN y deciden qué tipo de célula deben ser. Un ejemplo destacado fue un gen de adhesión celular llamado PCDHGC3. Incluso en tumores SDHB mutados que no se diseminaban, la región reguladora de este gen ya estaba parcialmente apagada; en los tumores metastásicos, el silenciamiento era aún más marcado. Otro gen, SATB2, implicado en la organización de grandes tramos de ADN, se silenció solo en tumores metastásicos, independientemente del estado de SDHB. En conjunto, estos patrones sugieren que la pérdida de SDHB “prepara” a las células hacia un estado menos maduro y más móvil, y cambios epigenéticos adicionales contribuyen luego a que se desprendan y se diseminen.
Reconfiguración de cómo los tumores consumen azúcares
Sorprendentemente, no todos los cambios implicaron apagones génicos. Un conjunto menor de genes perdió metilación y aumentó su actividad, y estos estaban muy implicados en el transporte de azúcares hacia las células. Entre ellos destacó el gen del transportador de fructosa SLC2A5. Su producto, conocido como GLUT5, introduce fructosa —un azúcar presente en la fruta y en muchos alimentos procesados— en las células. En modelos celulares expuestos a bajo oxígeno, SLC2A5 se activó de forma sostenida, mientras que otros transportadores de azúcares respondieron de forma menos constante. Los autores además establecieron cultivos celulares derivados de pacientes con tumores PPGL y demostraron que, cuando la glucosa escaseaba, añadir fructosa ayudaba a estas células a seguir dividiéndose, especialmente en condiciones de hipoxia que imitan el microambiente tumoral.
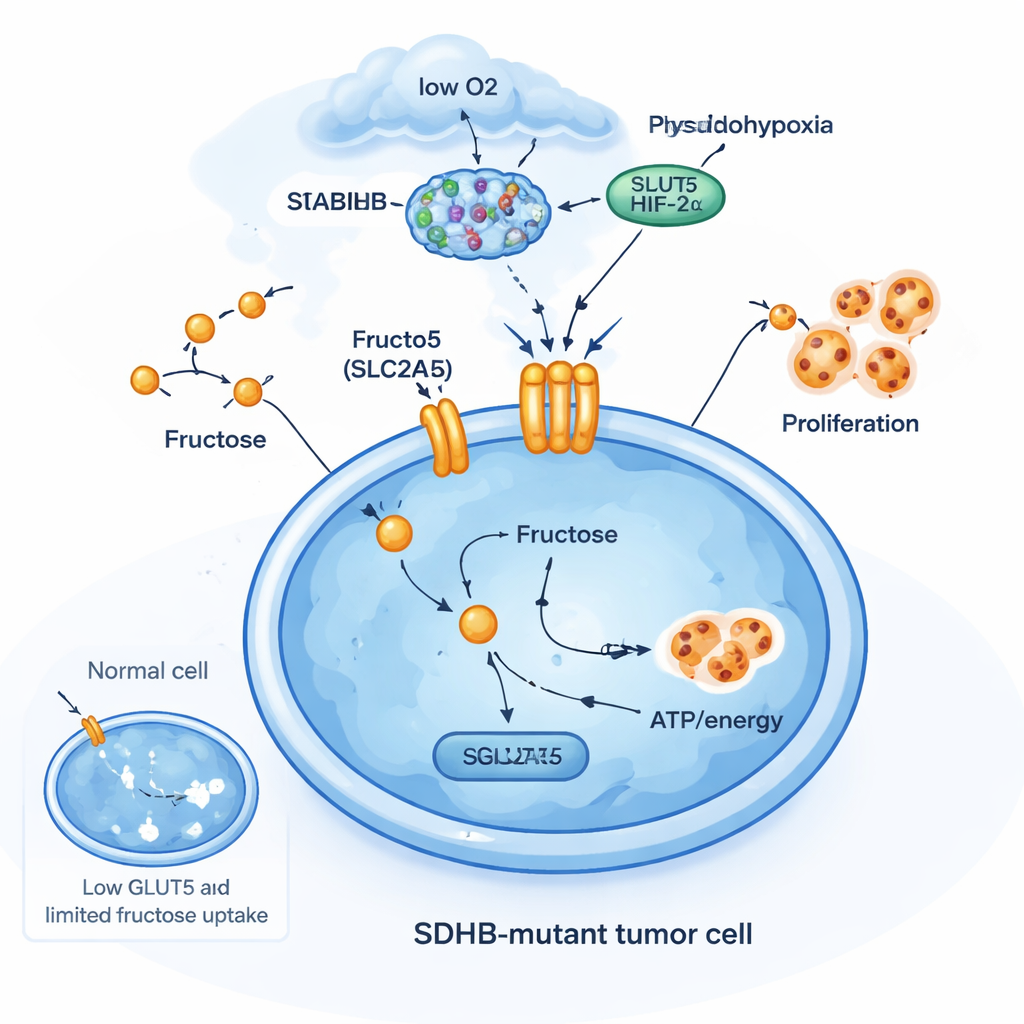
Un truco de supervivencia alimentado por fructosa
Para entender por qué son importantes las mutaciones en SDHB, el equipo eliminó SDHB en varios tipos celulares. En células de tipo cromafín de la glándula suprarrenal y en una línea de cáncer renal con activación constante del factor sensor de oxígeno HIF2α, la pérdida de SDHB aumentó los niveles de SLC2A5. Pero en líneas celulares tumorales más comunes que carecían de esas características neuroendocrinas o de HIF2α, el mismo bloqueo de SDHB no activó SLC2A5. Esto demuestra que el transportador de fructosa no forma parte de una respuesta genérica al estrés; es una adaptación muy específica en ciertos tipos celulares que ya viven en un estado de “pseudo‑hipoxia”. En estas células, la pérdida de SDHB, la acumulación de succinato y la actividad de HIF2α cooperan para abrir una nueva puerta metabólica: la captación de fructosa para nutrir el crecimiento cuando el oxígeno y la glucosa son limitados.
Qué significa esto para los pacientes
En términos sencillos, el estudio revela un doble cambio en los PPGL metastásicos con mutaciones en SDHB. Primero, su sistema de control del ADN se reprograma para empujar a las células hacia un estado menos especializado y más plástico, propenso a la invasión. Segundo, su sistema energético se reconfigura para aprovechar la fructosa como combustible alternativo en nichos duros de bajo oxígeno y baja glucosa. Al identificar al transportador de fructosa SLC2A5/GLUT5 como un actor clave en este proceso, el trabajo apunta a un posible talón de Aquiles: bloquear la captación o el metabolismo de la fructosa podría privar selectivamente de recursos a estos tumores mientras respeta la mayoría de tejidos normales. Aunque tales terapias aún no están disponibles, mapear este paisaje epigenético y metabólico es un paso crítico hacia tratamientos más precisos y centrados en el metabolismo para pacientes con PPGL de alto riesgo y mutación en SDHB.
Cita: Cubiella, T., Alba-Linares, J.J., San-Juan-Guardado, J. et al. Epigenetic and metabolic rewiring in metastatic pheochromocytomas and paragangliomas driven by SDHB mutations. Commun Biol 9, 266 (2026). https://doi.org/10.1038/s42003-026-09543-9
Palabras clave: feocromocitoma, paraganglioma, mutación SDHB, epigenética, metabolismo de la fructosa