Clear Sky Science · es
Análisis multiómico de las redes de señalización humanas de PHACTR1
Por qué este gen de los vasos sanguíneos te importa
Los infartos, los ictus y la hipertensión arterial tienen su origen en la salud de nuestros vasos sanguíneos. Un solo gen llamado PHACTR1 ha aparecido repetidamente en grandes estudios genéticos de estas afecciones, pero los científicos no habían comprendido bien por qué. Este estudio empleó una exploración amplia y “a todos los niveles” dentro de células humanas para mapear lo que PHACTR1 hace realmente, revelando cómo puede influir en el crecimiento celular, el uso de energía y el manejo del hierro, procesos que en última instancia determinan la salud de las arterias.
Un barrido integral dentro de las células
En lugar de centrarse en una molécula a la vez, los investigadores usaron una estrategia llamada multiómica: midieron simultáneamente miles de ARNs, proteínas, pequeños metabolitos y lípidos en las células. Modificaron células humanas para que produjeran PHACTR1 en exceso o con el gen reducido, imitando diferencias genéticas naturales observadas en personas. Al comparar estas células alteradas con controles normales a través de cuatro capas moleculares y procesar los datos con software de rutas biológicas sofisticado, construyeron un mapa global de cómo los cambios en PHACTR1 se propagan por la maquinaria interna de la célula. 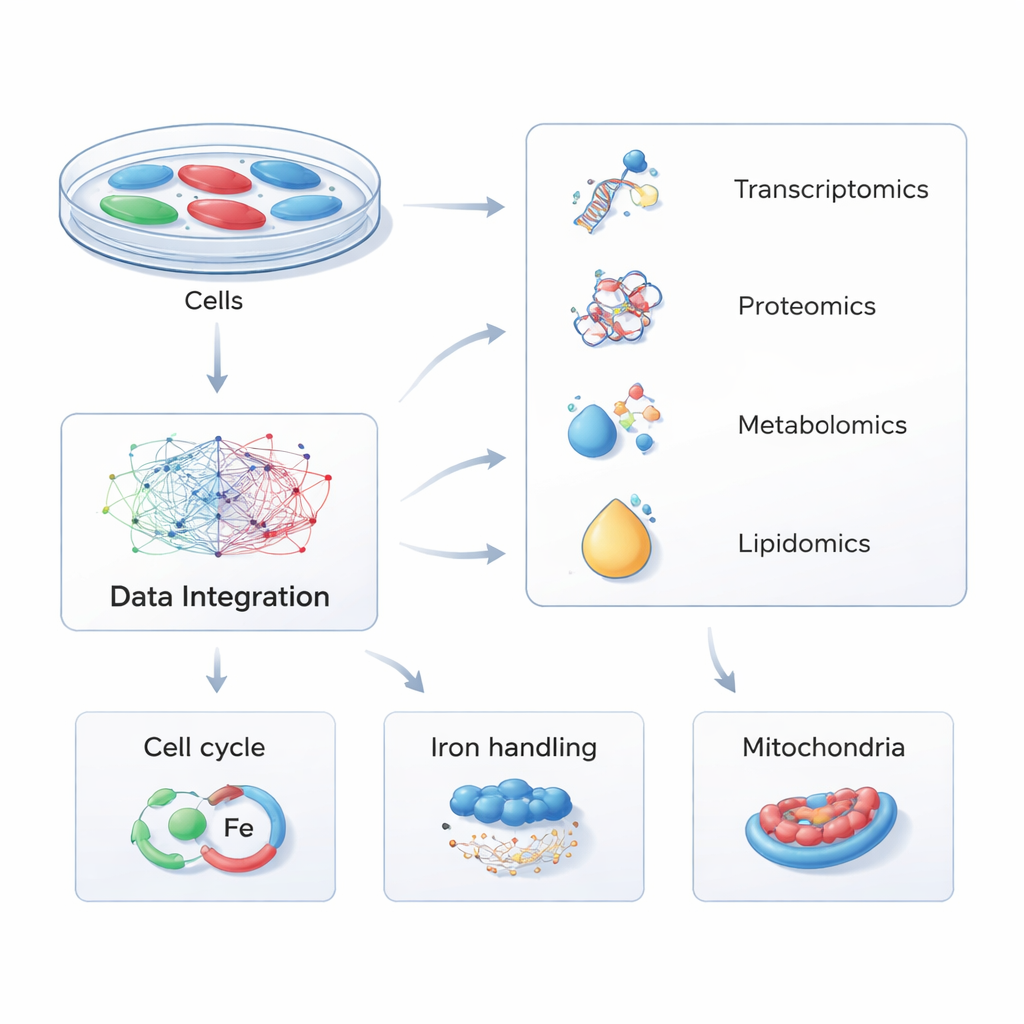
Más allá del andamiaje celular: control de los ciclos de crecimiento
Hasta ahora se conocía PHACTR1 sobre todo por ayudar a organizar el andamiaje interno de filamentos de actina. Los nuevos datos mostraron que también influye de manera importante en el control del ciclo celular: la coreografía por la que las células copian su ADN y se dividen. Las células con exceso de PHACTR1 salieron de la fase de reposo G1 y se acumularon en fases de copia de ADN y pre-division, con menos células que lograron entrar en mitosis completa. Reguladores clave como la ciclina B1, Cdt1 y otras proteínas del ciclo celular se vieron alterados. Cuando el equipo repitió los experimentos en células endoteliales humanas primarias —las células que recubren los vasos sanguíneos— volvieron a observar cambios en los reguladores centrales del ciclo celular. Esto sugiere que PHACTR1 contribuye a decidir cuándo las células vasculares reposan, se dividen o se detienen, un equilibrio crucial tanto para reparar las paredes vasculares como para evitar crecimientos tisulares peligrosos.
Gestión del hierro y defensa contra el daño
La integración multiómica también apuntó a rutas relacionadas con el hierro y a una forma especializada de muerte celular impulsada por el hierro denominada ferroptosis. Aunque las células no estaban muriendo activamente por ferroptosis, el aumento de PHACTR1 redujo los niveles de proteínas clave en el manejo del hierro, incluidos la cadena pesada de la ferritina (la principal cápsula de almacenamiento del hierro) y la hemooxigenasa 1 (que recicla hierro a partir del hemo). En células endoteliales primarias, PHACTR1 alteró de forma similar estas proteínas y a defensores clave contra el daño oxidativo. Dado que un manejo inadecuado del hierro puede alimentar la inflamación, el estrés oxidativo y placas arteriales inestables, estos resultados sugieren que PHACTR1 puede ajustar cómo las células vasculares almacenan y desintoxican el hierro, afectando potencialmente la vulnerabilidad a ciertas enfermedades vasculares.
Mitocondrias, energía y salud arterial
Otra sorpresa fue el papel de PHACTR1 en las mitocondrias, las centrales energéticas de la célula. El equipo detectó proteína PHACTR1 dentro de mitocondrias aisladas y observó que cambiar sus niveles remodelaba la red mitocondrial. Cuando PHACTR1 estaba elevado, las mitocondrias eran más alargadas y una proteína llamada Drp1 presentaba una modificación química en un sitio que reduce la fragmentación mitocondrial. Los niveles de una proteína andamio, AKAP1, que ayuda a organizar la señalización en la superficie mitocondrial, subieron y bajaron en paralelo con PHACTR1. Estos cambios estructurales coincidieron con variaciones en la producción de energía celular: PHACTR1 alto redujo la producción mitocondrial de ATP y se asoció con la acumulación de ciertos derivados de ácidos grasos que indican una quema de grasas más lenta, mientras que PHACTR1 bajo impulsó a las células a depender más de la glucólisis, la quema de azúcar. Los análisis de muestras de arteria humana mostraron que PHACTR1 y AKAP1 tienden a activarse de forma conjunta, vinculando este circuito de control mitocondrial directamente con vasos sanguíneos reales. 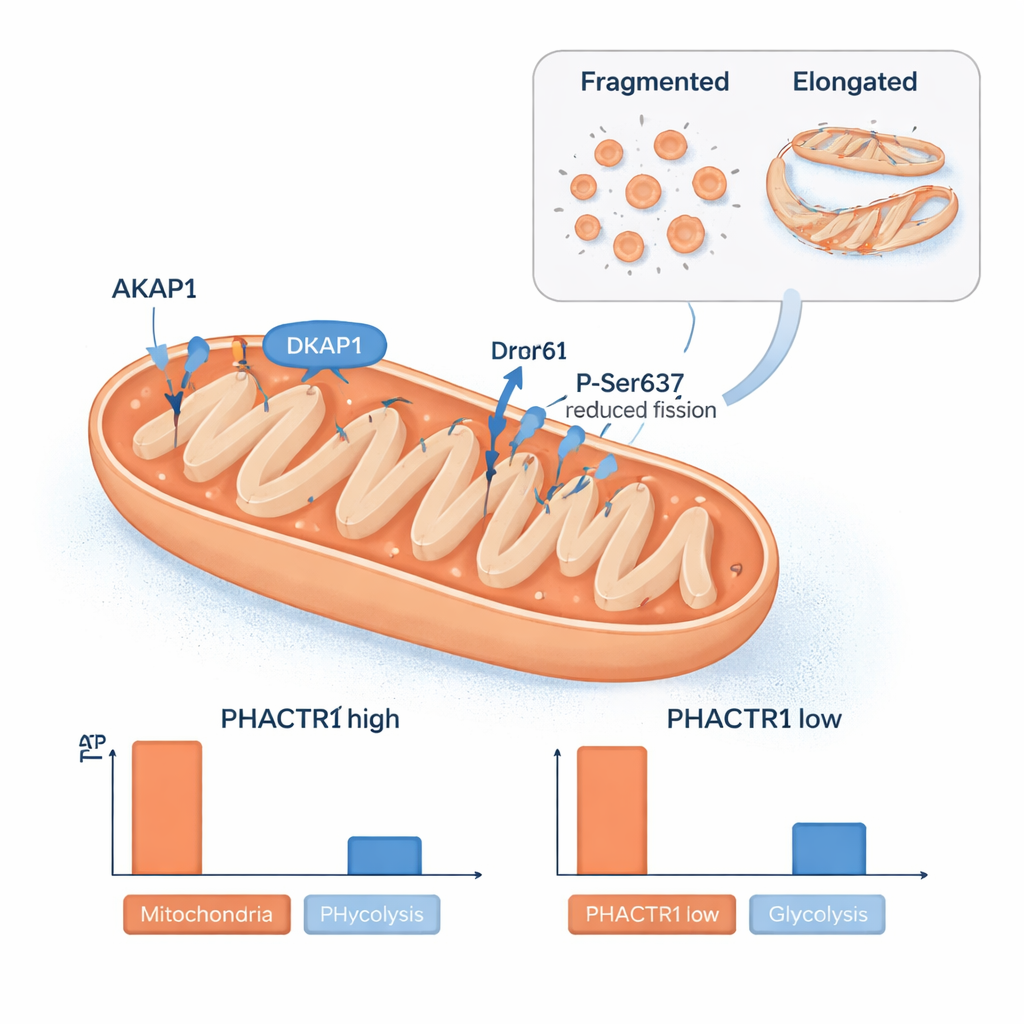
Qué significa todo esto para los vasos sanguíneos
En conjunto, este trabajo demuestra que PHACTR1 no es un gen de un solo propósito sino un coordinador maestro que influye en cómo las células vasculares se dividen, almacenan hierro y obtienen energía. Al mapear estas conexiones a través de miles de moléculas, el estudio ayuda a explicar por qué las diferencias naturales en PHACTR1 se asocian con una amplia gama de enfermedades vasculares —desde enfermedad coronaria hasta desgarros arteriales espontáneos y migraña. Para el público no especializado, la conclusión es que un gen marcado por la genética humana ahora se está rastreando hasta comportamientos celulares concretos que influyen en el crecimiento de placas, la estabilidad de los vasos y el balance energético. A la larga, comprender estas redes controladas por PHACTR1 podría abrir la puerta a terapias más precisas que modulen los ciclos celulares, el manejo del hierro o la función mitocondrial para devolver un estado más saludable a personas con riesgo de enfermedad cardiovascular.
Cita: Wolhuter, K., Ma, L., Bryce, N.S. et al. Multi-omic analysis of human PHACTR1 signaling networks. Commun Biol 9, 265 (2026). https://doi.org/10.1038/s42003-026-09542-w
Palabras clave: PHACTR1, enfermedad vascular, multiómica, mitocondrias, metabolismo del hierro