Clear Sky Science · es
Dirigir PAK4 potencia la piroptosis inducida por gemcitabina en el cáncer de páncreas a través del eje NLRP1/caspasa-3/GSDME
Por qué matar células cancerosas de forma “incendiaria” podría importar
El cáncer de páncreas se encuentra entre los más letales y, aun con los mejores fármacos quimioterapéuticos, estos a menudo dejan de ser efectivos cuando los tumores desarrollan resistencia. Este estudio explora un giro inesperado: el mismo fármaco, la gemcitabina, puede matar células cancerosas de una forma más explosiva e inflamatoria llamada piroptosis —si se desactiva un “freno” molecular clave llamado PAK4. Comprender y dirigir este freno podría hacer que los tratamientos existentes funcionen mejor para muchos pacientes.
Un cáncer empecinado que elude el tratamiento
El adenocarcinoma ductal pancreático suele diagnosticarse en estadios avanzados y responde mal a la terapia, por lo que la gemcitabina sigue siendo un fármaco central pese a sus limitaciones. La gemcitabina normalmente induce muerte celular por apoptosis, una forma ordenada y silenciosa de muerte celular programada. Pero más de la mitad de los tumores pancreáticos examinados en este estudio producían altos niveles de una proteína llamada GSDME, que puede convertir esa muerte silenciosa en piroptosis: una forma rápida y “explosiva” de muerte celular que daña la membrana celular y libera señales inflamatorias. Esto planteó una pregunta clave: si los tumores pueden sufrir piroptosis, ¿por qué tantos siguen siendo resistentes a la gemcitabina?
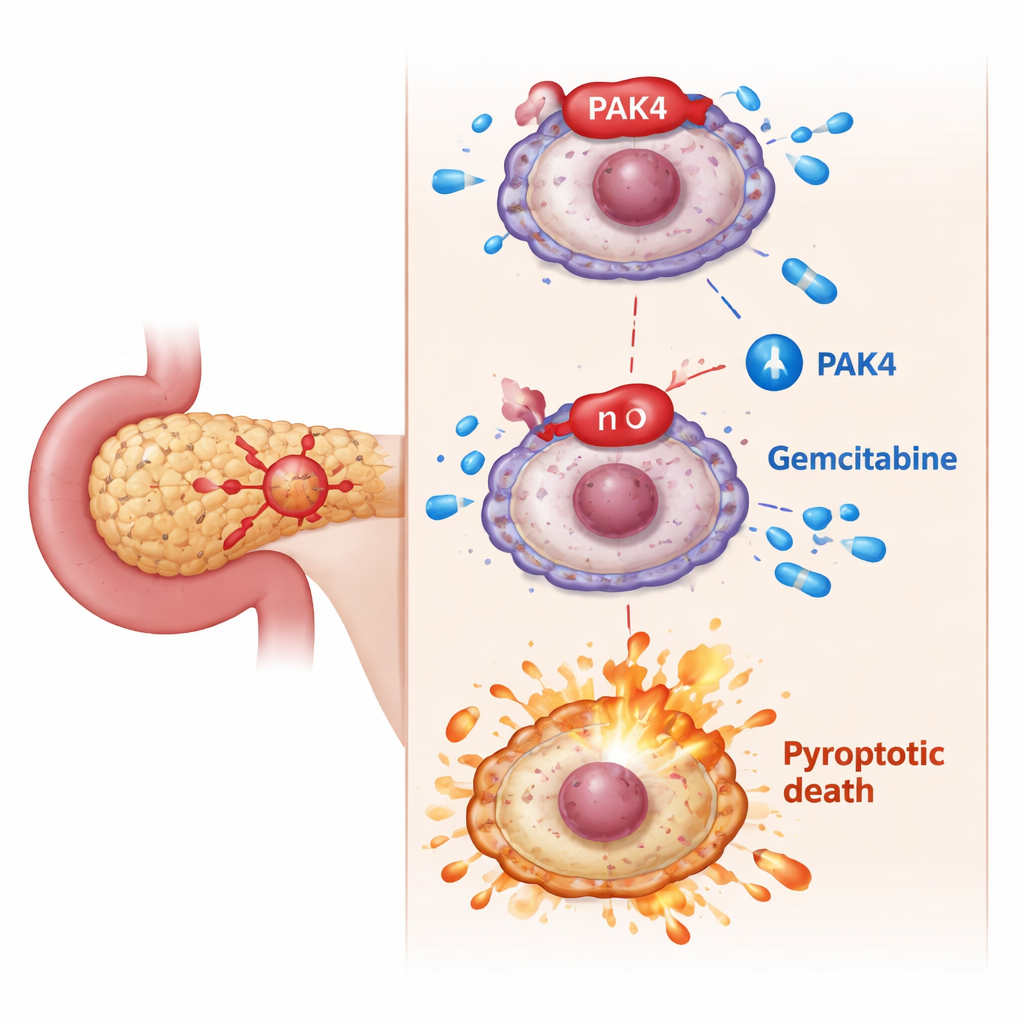
El freno oculto: PAK4 bloquea la muerte celular incendiaria
Los investigadores se centraron en PAK4, una proteína promotora del crecimiento conocida por estar hiperactiva en el cáncer de páncreas y asociada a mala respuesta a la gemcitabina. En experimentos celulares, las células cancerosas con altos niveles de PAK4 resultaron más difíciles de eliminar con gemcitabina. Cuando el equipo redujo PAK4, la gemcitabina se volvió mucho más letal: las células mostraron rasgos clásicos de piroptosis —hinchazón, burbujas tipo globo, membranas rotas y liberación aumentada del contenido intracelular. A nivel molecular, este cambio dependió de que GSDME fuera cortada en un fragmento activo por otra proteína llamada caspasa-3. Bloquear la caspasa-3 impidió que GSDME desencadenara piroptosis, confirmando que PAK4 actúa normalmente para mantener este camino de muerte bajo control.
Cómo PAK4 desmantela la alarma de muerte de la célula
Profundizando, los científicos hallaron que PAK4 no ataca directamente a GSDME. En su lugar, sabotea un “sensor de alarma” aguas arriba llamado NLRP1. En pacientes, niveles más altos de NLRP1 se asociaron con mejor supervivencia, lo que sugiere que ayuda al organismo a mantener los tumores a raya. En las células cancerosas, cuando se eliminó NLRP1, la muerte celular inducida por gemcitabina y la activación de GSDME disminuyeron drásticamente, lo que muestra que NLRP1 alimenta la maquinaria de la piroptosis. Los niveles de PAK4 y NLRP1 se relacionaron de forma inversa en muestras tumorales: donde PAK4 era alto, NLRP1 era bajo. El estudio demostró que PAK4 activo actúa a través de otra proteína, la ligasa E3 Mdm2, para etiquetar a NLRP1 y dirigirlo al sistema de eliminación celular. Al marcar NLRP1 de esta manera, PAK4 impide la activación de una reacción en cadena —mediante caspasa-9 y caspasa-3— que normalmente culminaría en una piroptosis impulsada por GSDME.
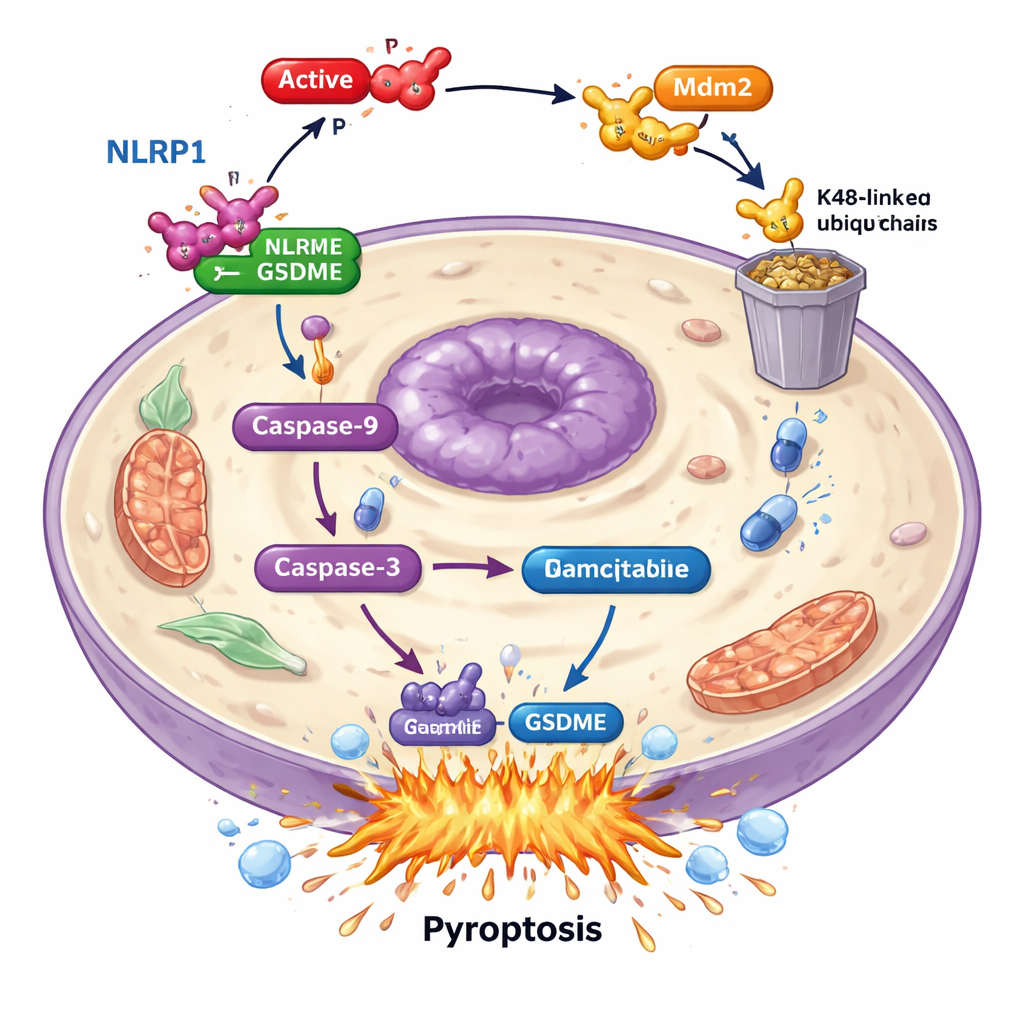
Apagar PAK4 para potenciar la quimioterapia
Dado que PAK4 actúa como freno de la piroptosis, el equipo probó si bloquear su actividad podía reavivar el poder letal de la gemcitabina. Utilizaron un inhibidor de PAK4 de pequeña molécula llamado PF-3758309. Por sí solo, este inhibidor ya inclinó a las células de cáncer de páncreas hacia la piroptosis, aumentando la activación de caspasa-3, la escisión de GSDME y la ruptura de la membrana celular. Combinado con gemcitabina, el efecto fue aún mayor: más células murieron por piroptosis y los marcadores moleculares de la vía de muerte se amplificaron. En modelos de ratón con tumores pancreáticos humanos, tanto reducir PAK4 como tratar con el inhibidor de PAK4 hizo que la gemcitabina redujera los tumores con más eficacia y aumentó los marcadores de piroptosis dentro de los cánceres.
Qué significa esto para los pacientes y tratamientos futuros
En términos sencillos, este trabajo revela un bloqueo molecular —PAK4— que impide que las células de cáncer de páncreas mueran de una forma especialmente destructiva durante la quimioterapia. Al desactivar PAK4, los médicos podrían empujar a los tumores tratados con gemcitabina hacia la piroptosis, haciendo el fármaco más efectivo y potencialmente activando al sistema inmunitario contra el cáncer. Aunque se necesita más trabajo en modelos derivados de pacientes y ensayos clínicos, el estudio propone una hoja de ruta clara: dirigir la vía PAK4–Mdm2–NLRP1–GSDME para convertir tumores resistentes en tumores sensibles, usando fármacos ya disponibles en combinaciones más inteligentes.
Cita: Lu, T., Song, Y., Liang, K. et al. Targeting PAK4 promotes Gemcitabine-induced pyroptosis in pancreatic cancer via NLRP1/caspase-3/GSDME axis. Commun Biol 9, 260 (2026). https://doi.org/10.1038/s42003-026-09538-6
Palabras clave: cáncer de páncreas, resistencia a gemcitabina, piroptosis, PAK4, terapia dirigida