Clear Sky Science · es
La fluvastatina suprime el inicio y la progresión del cáncer de mama mediante la diana CYP4Z1
Por qué un fármaco contra el colesterol importa para el cáncer de mama
Muchas mujeres tratadas por cáncer de mama desarrollan niveles anormales de grasas en sangre y afrontan la amenaza continua de que la enfermedad reaparezca o se disemine. Este estudio explora una idea sugerente: ¿podría una pastilla común para bajar el colesterol, la fluvastatina, reutilizarse para frenar o prevenir el cáncer de mama desactivando una proteína que alimenta a las células tumorales especialmente peligrosas, con características similares a las de las células madre?
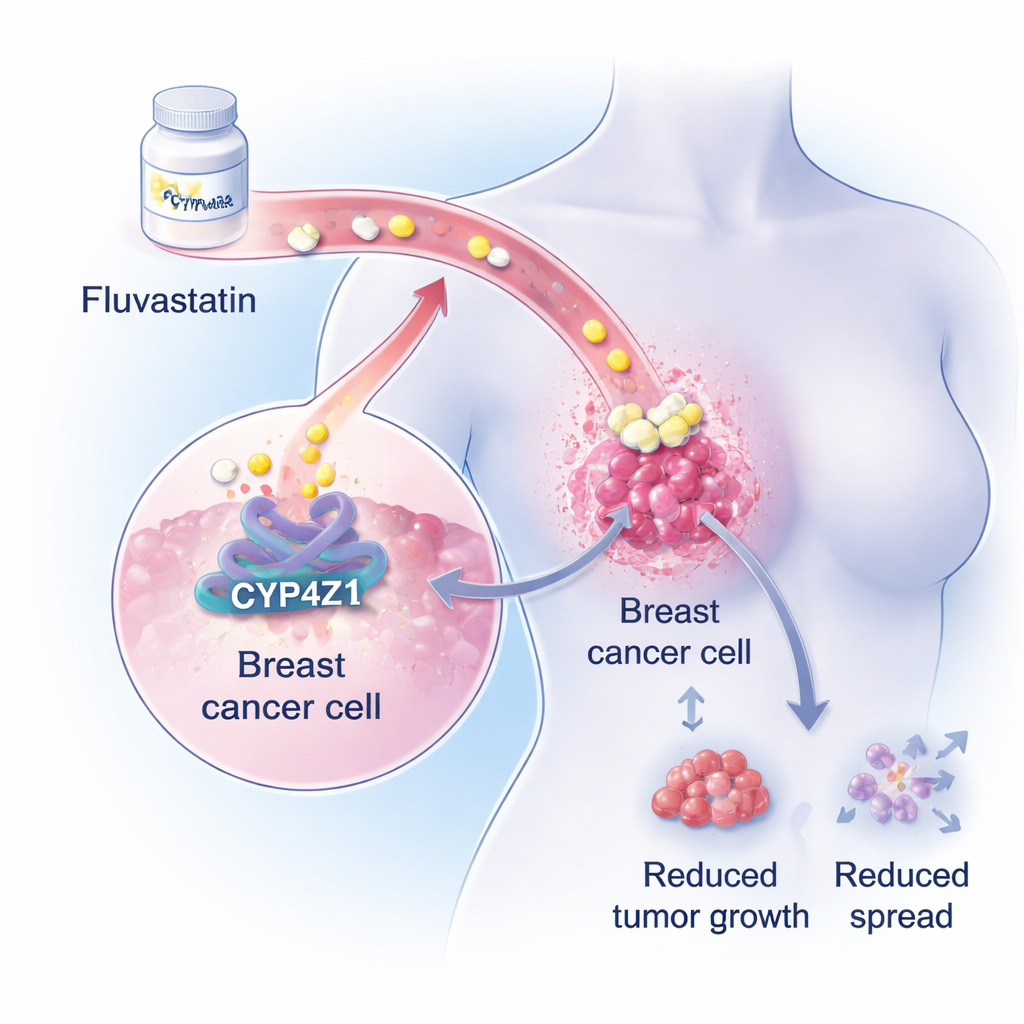
Un motor oculto dentro de los tumores mamarios
Los investigadores se centran en una proteína poco conocida llamada CYP4Z1, que se encuentra en niveles altos en las células de cáncer de mama pero no en el tejido mamario sano. Trabajos previos mostraron que CYP4Z1 ayuda a las células cancerosas a comportarse más como células madre: células capaces de autorrenovarse indefinidamente, resistir la quimioterapia y reiniciar tumores tras el tratamiento. En amplios análisis genéticos y bioquímicos, el equipo demuestra ahora que la hiperactividad de CYP4Z1 potencia fuertemente las vías de síntesis de lípidos dentro de las células de cáncer de mama, en particular la producción de triglicéridos, una grasa de almacenamiento mayor. Dado que muchas pacientes con cáncer de mama ya desarrollan alteraciones de las grasas en sangre durante la quimioterapia, ese papel promotor de lípidos de CYP4Z1 sugirió una oportunidad para fármacos hipolipemiantes ya existentes.
Reutilizar la fluvastatina, de la salud cardiaca a la atención oncológica
Para probar esta idea, los científicos cribaron una pequeña biblioteca de 23 fármacos aprobados por la FDA usados para reducir los lípidos sanguíneos. La fluvastatina, una estatina ampliamente prescrita para el colesterol alto, destacó: bloqueó directamente la actividad enzimática de CYP4Z1 de forma dependiente de la dosis. En dosis mucho menos perjudiciales para las células mamarias normales que para las cancerosas, la fluvastatina redujo drásticamente marcadores clave de “stemness”, la capacidad de las células de cáncer de mama para formar “esferas tumorales” flotantes y su capacidad de migrar e invadir a través de barreras tipo tejido en ensayos de laboratorio. También volvió las células tumorales más sensibles a la quimioterapia con adriamicina, lo que sugiere que podría potenciar los tratamientos existentes.
Poner el fármaco a prueba en animales vivos
El equipo evaluó luego la fluvastatina en modelos murinos. En ratones implantados con células humanas de cáncer de mama, el tratamiento periódico con fluvastatina ralentizó el crecimiento tumoral, redujo los niveles de un marcador de stemness (ALDH1A1) y del marcador de proliferación celular Ki67 en los tumores, y disminuyó el número de nódulos metastásicos que aparecieron en los pulmones. Es importante que los ratones tratados con fluvastatina mantuvieron su peso corporal y no mostraron anomalías graves en sangre ni en médula ósea, lo que respalda un perfil de seguridad favorable a la dosis probada. En un modelo genético más realista —ratones diseñados para desarrollar tumores mamarios impulsados por un gen carcinógeno— los investigadores introdujeron además CYP4Z1 humano en el tejido mamario. Estos ratones desarrollaron más lesiones precancerosas y cancerosas, y más metástasis hepáticas y pulmonares, que los animales de control. El tratamiento con fluvastatina redujo sustancialmente tanto el número de lesiones mamarias como las metástasis a distancia, especialmente en ratones portadores del gen humano CYP4Z1 adicional.
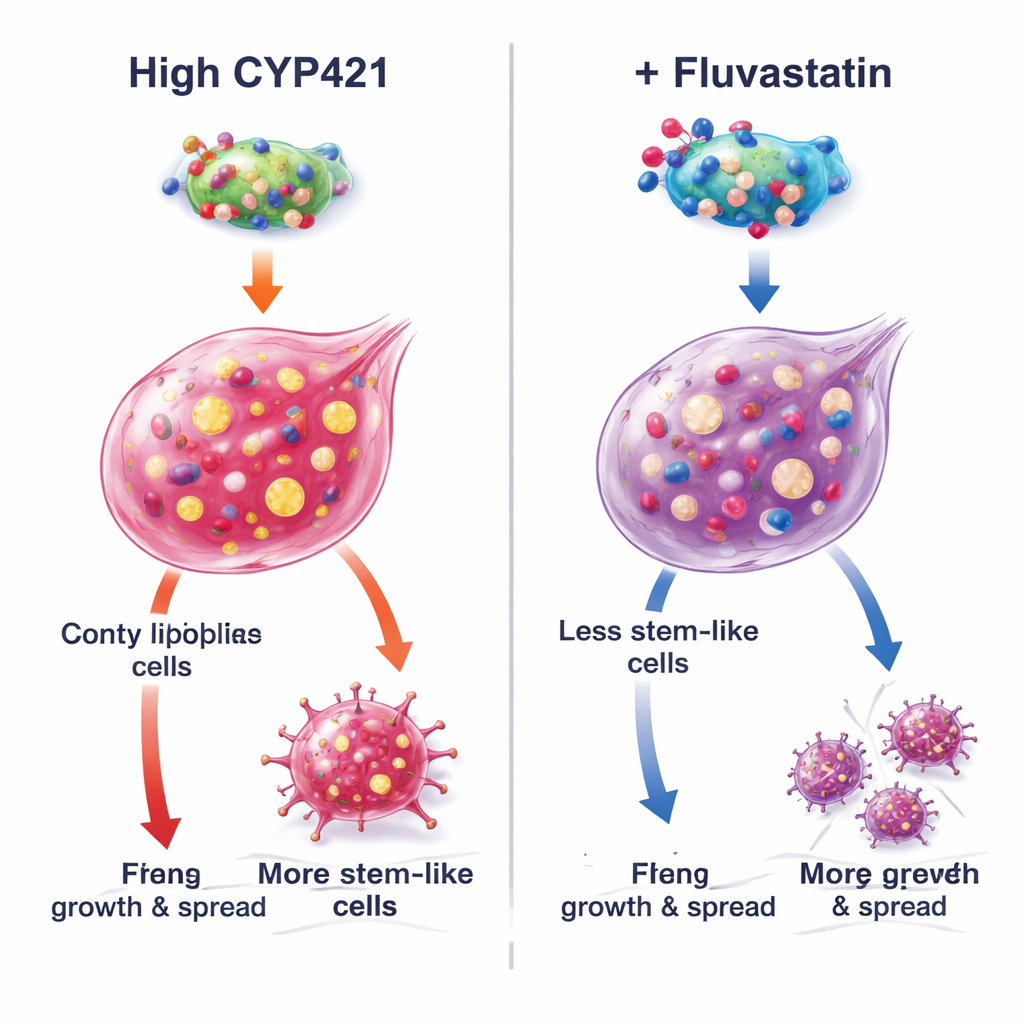
Cómo la fluvastatina desactiva una proteína promotora de cáncer
Para entender el mecanismo, los autores combinaron modelado por ordenador con ingeniería proteica precisa. Predijeron que la fluvastatina se inserta en el sitio activo de CYP4Z1 en tres aminoácidos críticos (Lys109, Pro444 y Arg450). Cuando esos sitios se mutaron, la actividad de CYP4Z1 cayó y la fluvastatina ya no pudo inhibirla más, confirmando esas posiciones como puntos de acoplamiento. En células que carecen de CYP4Z1 de forma natural, la adición de la proteína normal aumentó la stemness y activó la señalización promotora del crecimiento PI3K/AKT, mientras que la fluvastatina revirtió esos efectos. Las versiones mutantes de CYP4Z1 fueron menos potentes y menos sensibles al fármaco. Experimentos adicionales mostraron que el impacto de la fluvastatina se debilitó cuando la producción de triglicéridos se incrementó artificialmente, o cuando CYP4Z1 se redujo mediante silenciamiento, subrayando que los efectos más fuertes del fármaco provienen de bloquear esta proteína específica y sus consecuencias en la síntesis de lípidos más que de inducir la muerte celular por ferroptosis impulsada por hierro.
Qué supone esto para las pacientes
En conjunto, el estudio sugiere que la fluvastatina, más allá de reducir el colesterol, puede frenar las etapas iniciales y la diseminación tardía del cáncer de mama en modelos experimentales al dirigirse a CYP4Z1, una proteína que impulsa el metabolismo lipídico y el comportamiento tipo célula madre en los tumores. Dado que la fluvastatina ya está aprobada y su seguridad está bien caracterizada, estos hallazgos ofrecen una vía prometedora para pruebas clínicas más rápidas como terapia complementaria, particularmente en pacientes cuyos tumores expresan fuertemente CYP4Z1. Aunque se necesita más trabajo para probar este enfoque en humanos e identificar posibles dianas adicionales del fármaco, la investigación abre la puerta a usar un medicamento conocido para el corazón como parte de una nueva estrategia contra los cánceres de mama agresivos y propensos a la recaída.
Cita: Li, H., Chen, Y., Shi, W. et al. Fluvastatin suppresses breast cancer initiation and progression via targeting CYP4Z1. Commun Biol 9, 254 (2026). https://doi.org/10.1038/s42003-026-09532-y
Palabras clave: cáncer de mama, fluvastatina, células madre cancerosas, metabolismo de lípidos, reutilización de fármacos