Clear Sky Science · es
miARNs diferencialmente expresados en la corteza temporal de pacientes con enfermedad de Alzheimer y su asociación con la patología tau
Por qué importan los pequeños interruptores cerebrales en el Alzheimer
La enfermedad de Alzheimer roba la memoria y la independencia de las personas de forma progresiva, pero aún carecemos de tratamientos que la detengan o reviertan. Este estudio se centra en algunos de los interruptores de control más pequeños del cerebro: moléculas cortas de ARN llamadas microARNs, que ayudan a decidir qué proteínas producen las células. Al examinar tejido cerebral de personas con Alzheimer, los investigadores preguntaron si los cambios en estos microARNs están relacionados con una característica clave de la enfermedad: la acumulación y propagación de la proteína tau anómala dentro de las células cerebrales.
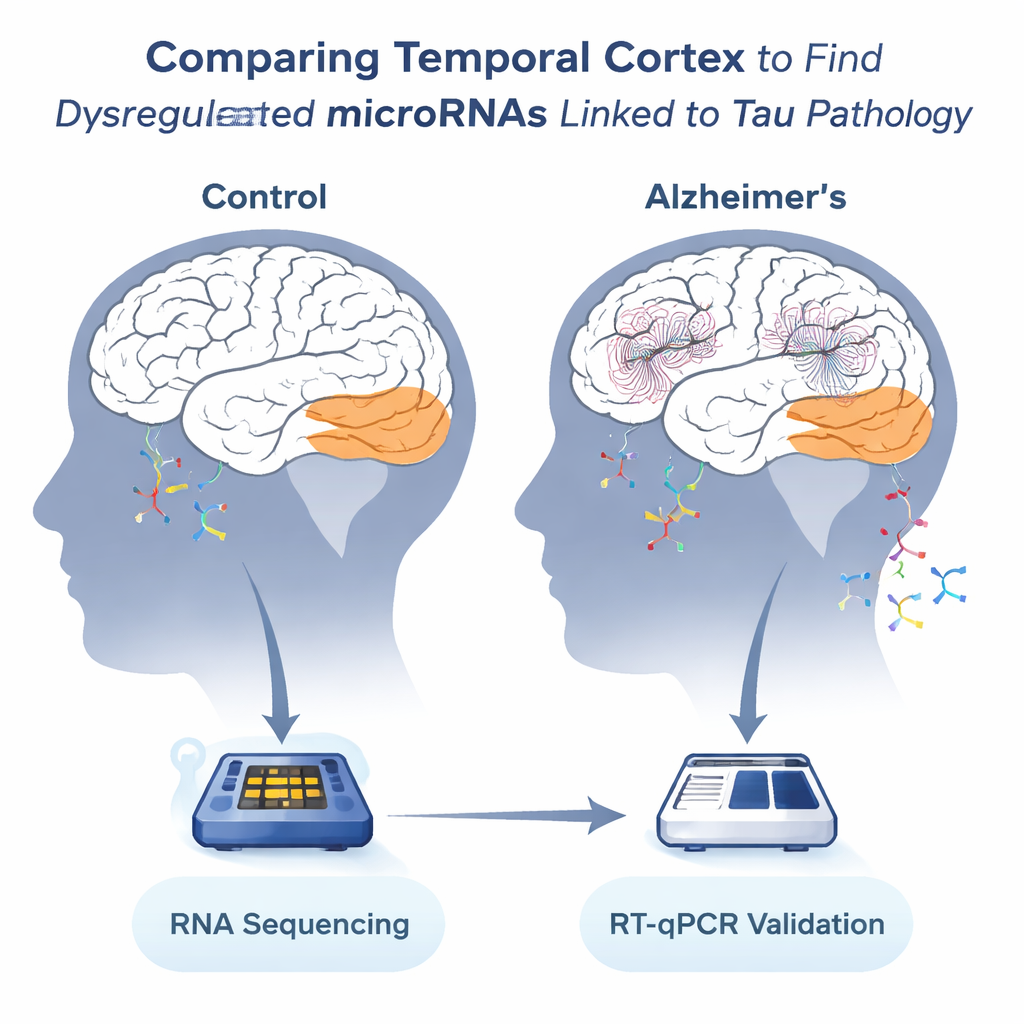
Analizando los mensajes en una región cerebral vulnerable
El equipo se centró en la corteza temporal, una región importante para el lenguaje y la memoria que se ve muy afectada en el Alzheimer. Tras el fallecimiento, se recopilaron muestras de 36 individuos —13 sin Alzheimer y 23 con la enfermedad— de dos bancos de cerebros europeos. Los científicos extrajeron ARN de este tejido y utilizaron secuenciación de alto rendimiento para contar cientos de microARNs diferentes. Dado que el tejido cerebral se degrada después de la muerte, verificaron cuidadosamente la calidad del ARN y seleccionaron 19 muestras con integridad aceptable para el análisis más detallado; luego usaron las 36 muestras para confirmar sus hallazgos clave.
Descubriendo una firma de microARNs del Alzheimer
De entre 449 microARNs detectados, 13 destacaron por estar consistentemente alterados en la corteza temporal de Alzheimer. Ocho estaban reducidos y cinco aumentados en comparación con cerebros de control. Varias de las señales más fuertes involucraron microARNs ya sospechados de tener importancia en el Alzheimer: miR-129-5p, miR-132-3p y miR-146b-5p eran todos más bajos, mientras que miR-151a-5p era más alto. Estas moléculas son abundantes en el cerebro y se sabe que regulan redes de genes implicadas en la salud neuronal. Usando una técnica segunda, más dirigida (RT-qPCR), los autores validaron que esos mismos microARNs cambiaban en la misma dirección, incluso al incluir muestras de menor calidad, lo que refuerza la confianza en que el patrón es real.
Relacionando los pequeños interruptores con el empeoramiento de los ovillos de tau
La gravedad del Alzheimer en el cerebro a menudo se evalúa por la etapa de Braak, que refleja hasta qué punto los ovillos de tau se han propagado por distintas regiones. Los investigadores observaron que los niveles de miR-129-5p, miR-132-3p y miR-146b-5p disminuían de forma gradual a medida que aumentaba la etapa de Braak, mientras que miR-151a-5p tendía a aumentar. También midieron directamente una forma de tau altamente fosforilada y propensa a formar ovillos en las mismas muestras. Los cerebros con más de esta tau anómala mostraron el mismo patrón: menos miR-129-5p, miR-132-3p y miR-146b-5p, y más miR-151a-5p. En otras palabras, los cambios en los microARNs siguieron tanto la clasificación microscópica como los signos bioquímicos de la patología tau, lo que sugiere que están estrechamente ligados al proceso de la enfermedad y no son meros espectadores aleatorios.
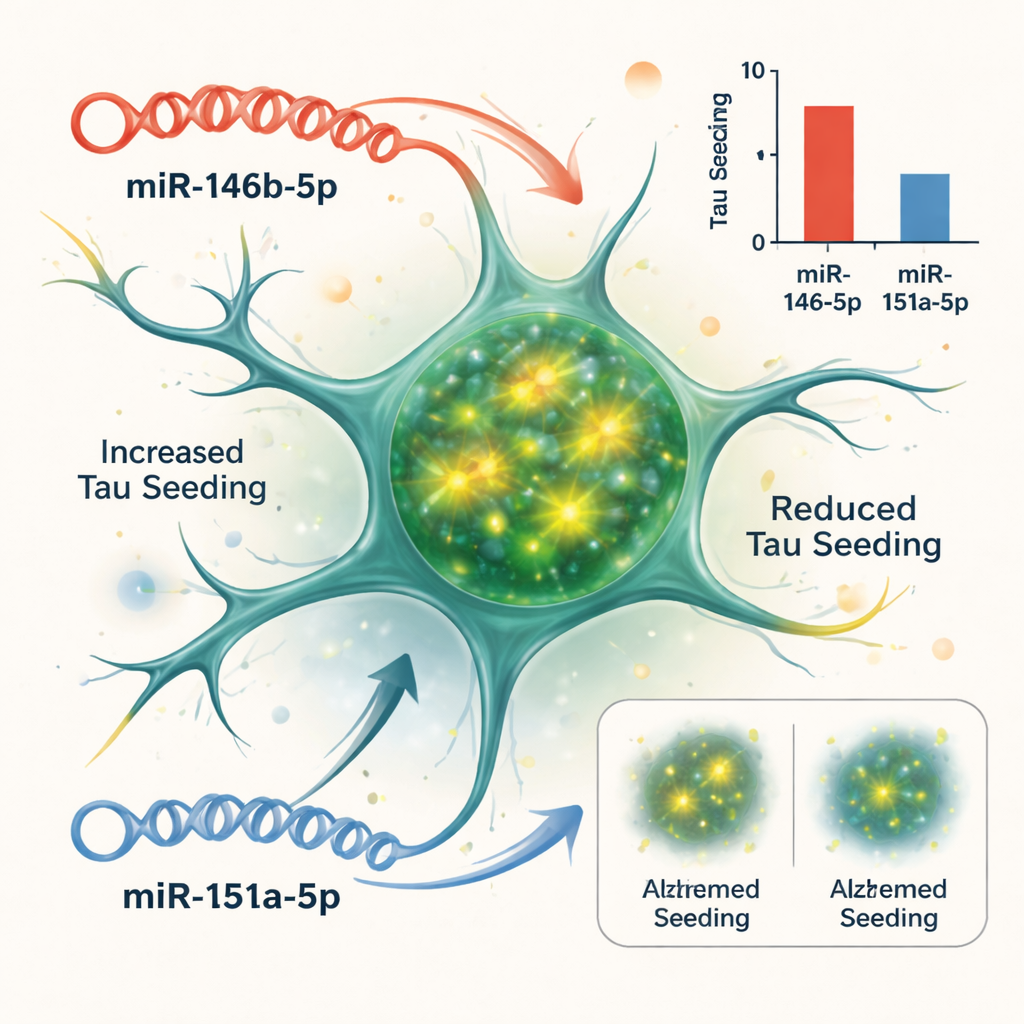
Probando causa y efecto en un modelo celular
La correlación no prueba que los microARNs impulsen la enfermedad, por lo que el equipo recurrió a un sistema celular que informa sobre la facilidad con la que la tau agregada puede "sembrar" nuevos cúmulos. Usaron células biosensor diseñadas para iluminarse cuando se forman fibras de tau en su interior. Al añadir material rico en tau procedente de cerebros con Alzheimer, las células generaron una señal fluorescente intensa. Al aumentar o bloquear microARNs específicos en estas células, los científicos pudieron ver cuáles alteraban esta siembra de tau. Dos destacaron: aumentar miR-146b-5p empeoró la siembra de tau, mientras que bloquearlo la redujo; por el contrario, aumentar miR-151a-5p atenuó la siembra de tau, y su inhibición la hizo más robusta. Otros microARNs probados tuvieron poco efecto en este ensayo.
Qué podría significar para el diagnóstico y el tratamiento futuros
Para entender qué podrían estar haciendo estos microARNs, los autores usaron herramientas computacionales para mapear sus genes diana predichos en vías biológicas conocidas. Los microARNs regulados a la baja —especialmente miR-129-5p, miR-132-3p y miR-146b-5p— se relacionaron con redes implicadas en la supervivencia neuronal, la señalización química en las sinapsis y vías asociadas al Alzheimer. Esto sugiere que perder su influencia reguladora normal podría alterar a la vez múltiples sistemas protectores, mientras que el aumento de miR-151a-5p puede representar un intento tardío y parcial del cerebro por contrarrestar la agregación de tau. Aunque este trabajo se basa en tejido post-mortem y en modelos celulares simplificados, refuerza la idea de que microARNs específicos tanto reflejan como modulan la patología tau. A largo plazo, medir estas moléculas en líquido cefalorraquídeo o sangre podría ayudar a seguir la progresión de la enfermedad, y ajustar con precisión sus niveles en el cerebro podría ofrecer una nueva vía para frenar o prevenir la propagación de la tau tóxica.
Cita: Nagaraj, S., Quintanilla-Sánchez, C., Ando, K. et al. Differentially expressed miRNAs in the temporal cortex of Alzheimer’s disease patients and their association to tau pathology. Commun Biol 9, 253 (2026). https://doi.org/10.1038/s42003-026-09530-0
Palabras clave: Enfermedad de Alzheimer, microARN, patología tau, corteza temporal, neurodegeneración