Clear Sky Science · es
El bloqueo específico del empalme génico puede desregular microARN primarios incrustados en intrones
Mensajes ocultos dentro de nuestros genes
Muchas terapias génicas nuevas actúan modulando los mensajes de ARN de nuestras células, pero esos ARN a menudo ocultan «notas al margen» que los científicos apenas empiezan a comprender. Este estudio muestra que fármacos diseñados para corregir empalmes defectuosos de genes pueden, por accidente, aumentar pequeños ARN reguladores enterrados dentro de intrones —los tramos no codificantes entre segmentos génicos— con efectos sorprendentes sobre la conectividad y el desarrollo cerebral.
Terapias génicas que reescriben el ARN
Los oligonucleótidos antisentido, u ASO, son fragmentos sintéticos cortos de material genético que se adhieren al ARN y cambian la forma en que se lee o procesa. Varios ASO ya se están probando o usando para enfermedades genéticas raras, en especial aquellas causadas por fallos en el empalme del ARN —el paso que une los segmentos codificantes de un gen. La mayoría de las pruebas de seguridad se centran en si un ASO restablece la proteína correcta y evita efectos secundarios evidentes. Pero muchos genes también alojan ARN no codificantes, incluidos microARN, dentro de sus intrones. Estas diminutas moléculas pueden ajustar fuertemente la actividad génica, y hasta la mitad de los microARN conocidos en vertebrados proceden de intrones. El nuevo estudio plantea la pregunta: ¿qué ocurre con estos microARN incrustados cuando forzamos cambios en el empalme con ASO?
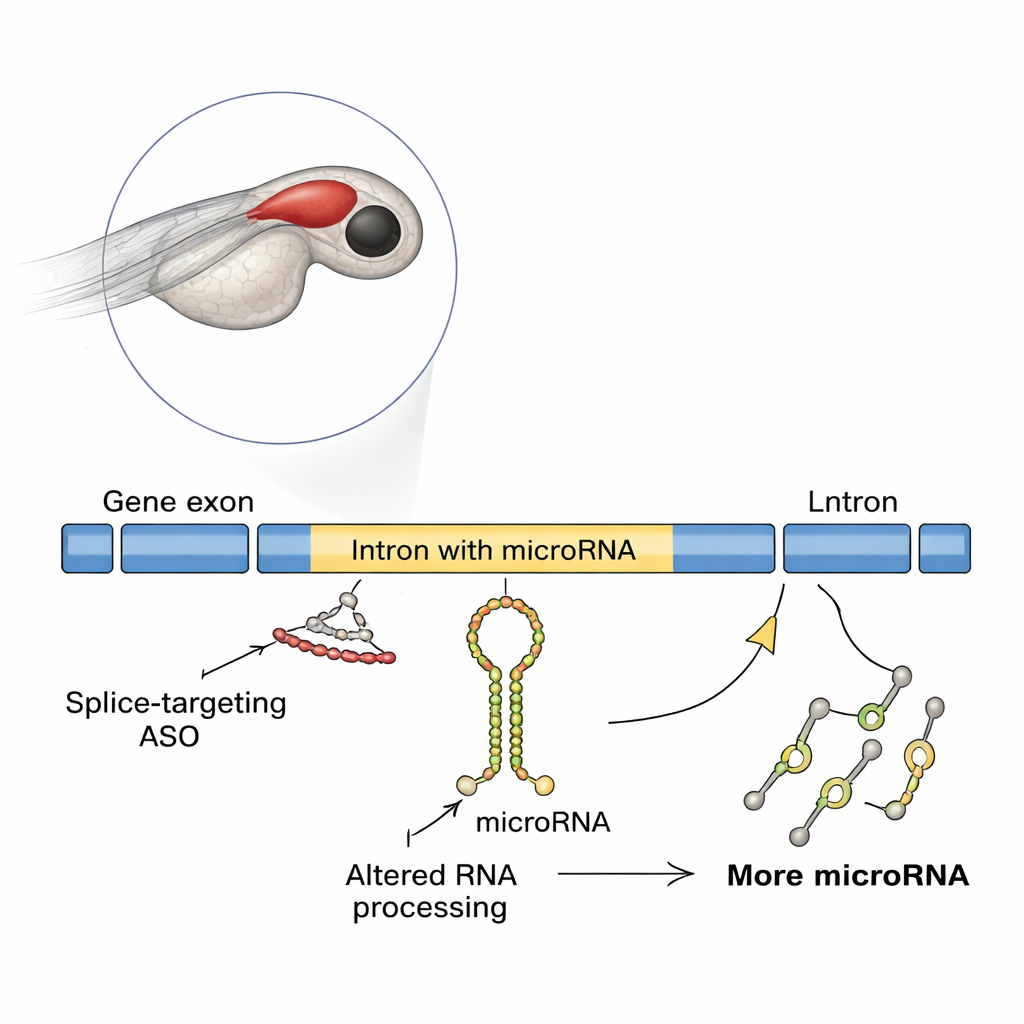
Un efecto sorprendente en cerebros de peces en desarrollo
Los investigadores usaron pez cebra, un modelo de vertebrado popular cuyos embriones transparentes facilitan el seguimiento del desarrollo cerebral. Se centraron en un gen llamado slit3, que ayuda a guiar las fibras nerviosas y contiene un microARN llamado mir-218a-1 dentro de uno de sus intrones. Cuando el equipo bloqueó el inicio de la traducción de slit3, el desarrollo de los axones de la hipófisis productora de hormonas parecía normal. Pero cuando usaron un ASO distinto que bloqueaba el empalme en un sitio específico de slit3, los axones que deberían proyectar hacia la hipófisis posterior se vieron drásticamente reducidos, aunque el número de neuronas productoras de oxitocina permaneció igual. Pruebas moleculares mostraron que ese ASO bloqueador del empalme provocó retención del intrón en el ARN del gen, aumentando inesperadamente los niveles del transcrito de slit3, su intrón largo y el transcrito primario intrónico de mir-218a-1.
El microARN, no la pérdida de proteína, impulsa los defectos
Para desenmarañar la causa del problema axonal, los autores compararon varios escenarios. Bloquear solo el mir-218a-1 maduro no cambió los niveles de slit3, y un ASO separado dirigido a otro sitio de empalme cercano al microARN no produjo defectos axonales ni aumentó mir-218a-1. De forma crucial, cuando el ASO bloqueador de empalme de slit3 se combinó con un ASO que neutraliza mir-218a-1, la conectividad axonal se recuperó en gran medida. De igual modo, en peces cebra genéticamente carentes de mir-218a-1, el mismo ASO bloqueador de empalme ya no causó defectos axonales, mientras que inyectar un análogo sintético de mir-218a pudo reproducir el fenotipo en peces normales. Estos experimentos apuntan a que el aumento del microARN intrónico —más que una proteína Slit3 truncada— es el principal impulsor de la alteración del desarrollo.
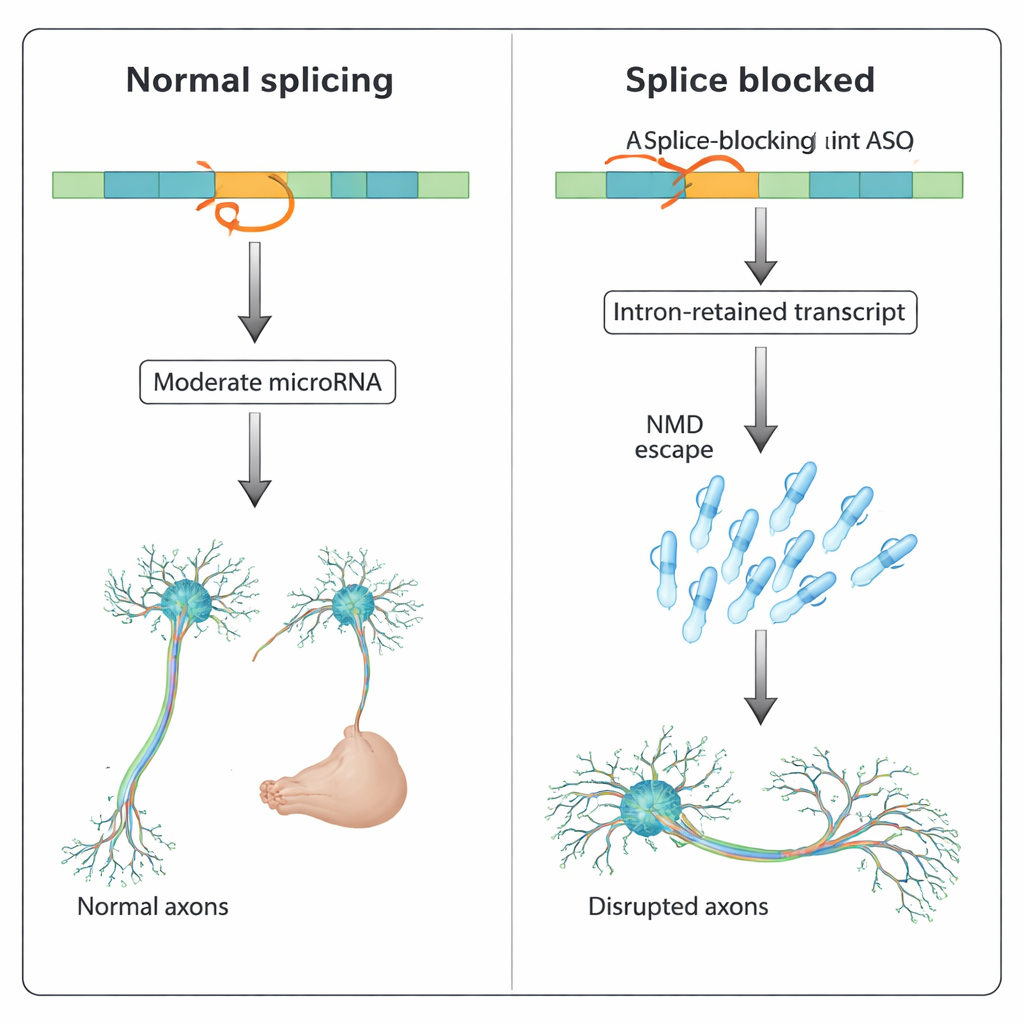
Un patrón más amplio en múltiples genes
El equipo preguntó entonces si este efecto es exclusivo de slit3. Buscaron en el genoma del pez cebra y hallaron docenas de genes codificadores de proteína que albergan microARN intrónicos, muchos implicados en el desarrollo y la señalización. Dos de esos genes, pank2 y dnm2a, habían mostrado previamente problemas de desarrollo severos cuando su empalme fue bloqueado por ASO, incluidos acumulación de líquido cerebral, hinchazón del corazón y deformidades corporales —problemas que los mutantes nulos genéticos de los mismos genes no reproducían. En este estudio, la coinyección de ASO que bloqueaban específicamente los microARN intrónicos mir-103 (en pank2) o mir-199-5p (en dnm2a) rescató parcialmente estos fenotipos inducidos por ASO. En algunos casos, el bloqueo del microARN también restauró la expresión del gen anfitrión, mientras que en otros no lo hizo, lo que sugiere que la actividad incrementada del microARN por sí sola puede ser perjudicial incluso cuando los cambios en los niveles globales son modestos.
Qué significa esto para futuros tratamientos
Los hallazgos revelan que los ASO dirigidos al empalme pueden hacer más que provocar omisión de exones o retención de intrones: pueden estabilizar transcritos con intrones retenidos que evaden el sistema de control de calidad celular y aumentar microARN primarios intrónicos, que a su vez desregulan redes de genes diana. En neuronas en desarrollo, una actividad microARN descontrolada puede distorsionar el crecimiento axonal y la conectividad. Para los desarrolladores de fármacos, esto significa que fenotipos inusuales u «off‑target» en pruebas animales no siempre derivan de vías genéricas de toxicidad como la activación de p53, sino de efectos no deseados sobre ARN intrónicos ocultos. Comparar cuidadosamente ASO que bloquean la traducción y los que bloquean el empalme, y monitorizar la expresión de microARN intrónicos, podría ayudar a detectar estos riesgos de forma temprana y a perfeccionar el diseño de ASO antes de que lleguen a pacientes.
Cita: Ali, M.H., Ramesh, A.R., Nedunchezhian, N. et al. Targeted blocking of gene splicing can dysregulate intron-embedded primary microRNAs. Commun Biol 9, 252 (2026). https://doi.org/10.1038/s42003-026-09529-7
Palabras clave: oligonucleótidos antisentido, microARN, empalme de ARN, desarrollo de pez cebra, seguridad de la terapia génica