Clear Sky Science · es
El nimbolide mejora el SDRA y la colitis ulcerosa al interrumpir la activación del inflamasoma NLRP3
Por qué es importante frenar la inflamación descontrolada
Muchas enfermedades graves, desde la insuficiencia pulmonar potencialmente mortal hasta las dolorosas afecciones intestinales, no se deben únicamente a gérmenes o lesiones, sino al propio sistema inmunitario cuando entra en modo sobreactivado. Este estudio explora si un compuesto natural llamado nimbolide, derivado del árbol neem, puede actuar como un “freno” preciso sobre una potente máquina inflamatoria dentro de nuestras células inmunitarias, abriendo así una vía potencialmente más segura para tratar condiciones como el síndrome de distrés respiratorio agudo (SDRA) y la colitis ulcerosa.
Una alarma problemática dentro de las células inmunes
En el centro de esta historia hay un sistema de alarma molecular llamado inflamasoma NLRP3. Cuando las células inmunes detectan peligro —señales de infecciones, tejidos dañados o cristales— puede ensamblarse como una estructura de tres piezas: el sensor NLRP3, el adaptador ASC y la enzima Caspasa‑1. Una vez armado, este complejo activa mensajeros potentes como IL‑1β e IL‑18 y puede desencadenar una forma inflamatoria de muerte celular llamada piroptosis. Aunque esta respuesta ayuda a eliminar amenazas, cuando se sobreactiva contribuye a enfermedades crónicas y agudas, incluyendo artritis, complicaciones de la diabetes, Alzheimer, SDRA y enfermedad inflamatoria intestinal. Los laboratorios farmacéuticos han intentado domar a NLRP3 con compuestos sintéticos, pero muchos candidatos han fracasado por toxicidad, efectos secundarios o mala farmacocinética, lo que deja una necesidad clara de inhibidores más seguros y selectivos.
Descubriendo un inhibidor potente de origen vegetal
Los investigadores evaluaron 126 compuestos naturales para ver cuáles bloqueaban mejor la liberación de IL‑1β en células inmunes de ratón. El nimbolide destacó, reduciendo la secreción de IL‑1β en más del 80% a las dosis de prueba. Experimentos adicionales mostraron que el nimbolide reducía de forma notable la activación de la Caspasa‑1, la liberación de IL‑1β y la muerte piroptótica en macrófagos derivados de médula ósea de ratón, con una potencia similar a un fármaco de referencia llamado MCC950. De forma importante, el nimbolide no frenó la liberación de otros mensajeros inmunitarios como IL‑6, lo que sugiere que actúa de manera focalizada en lugar de apagar la inmunidad en general. Al probarse con diversos desencadenantes que activan NLRP3 —como ATP, nigericina, cristales de alúmina e imiquimod— el nimbolide redujo de forma consistente la actividad del inflamasoma, incluso en células humanas THP‑1. En contraste, no bloqueó dos inflamasomas relacionados, AIM2 y NLRC4, lo que subraya su especificidad por NLRP3.
Cómo bloquea nimbolide la máquina inflamatoria
Para entender el mecanismo de nimbolide, el equipo investigó si interfieren los primeros pasos de “preparación” controlados por la vía NF‑κB, o las etapas tardías cuando el inflamasoma se ensambla físicamente. El tratamiento a corto plazo, administrado tras la preparación, dejó intactas las señales clave de priming y la expresión génica, pero aun así redujo IL‑1β y la activación de Caspasa‑1, indicando que el nimbolide actúa principalmente en la etapa de ensamblaje. Pruebas bioquímicas detalladas revelaron que el nimbolide no altera los flujos de potasio o calcio, el daño mitocondrial ni la interacción de NLRP3 con su proteína auxiliar NEK7. En cambio, interfiere con el apretón de manos crucial entre NLRP3 y ASC, reduce el agrupamiento de ASC en «specks» y evita que NLRP3 forme oligómeros de orden superior. Mediante ensayos de unión y modelado molecular, los autores mostraron que el nimbolide se une directamente a la región NACHT de NLRP3 en un aminoácido específico, la Lisina 565. Cuando este sitio se mutó, el nimbolide dejó de proteger a NLRP3 de la degradación y ya no rompía su unión con ASC, confirmando a la Lis565 como el punto clave de anclaje. Cabe destacar que, mientras otros fármacos suelen dirigirse a la actividad ATPasa de NLRP3, el nimbolide bloquea el ensamblaje sin afectar al consumo de ATP, ofreciendo un modo de acción distinto.
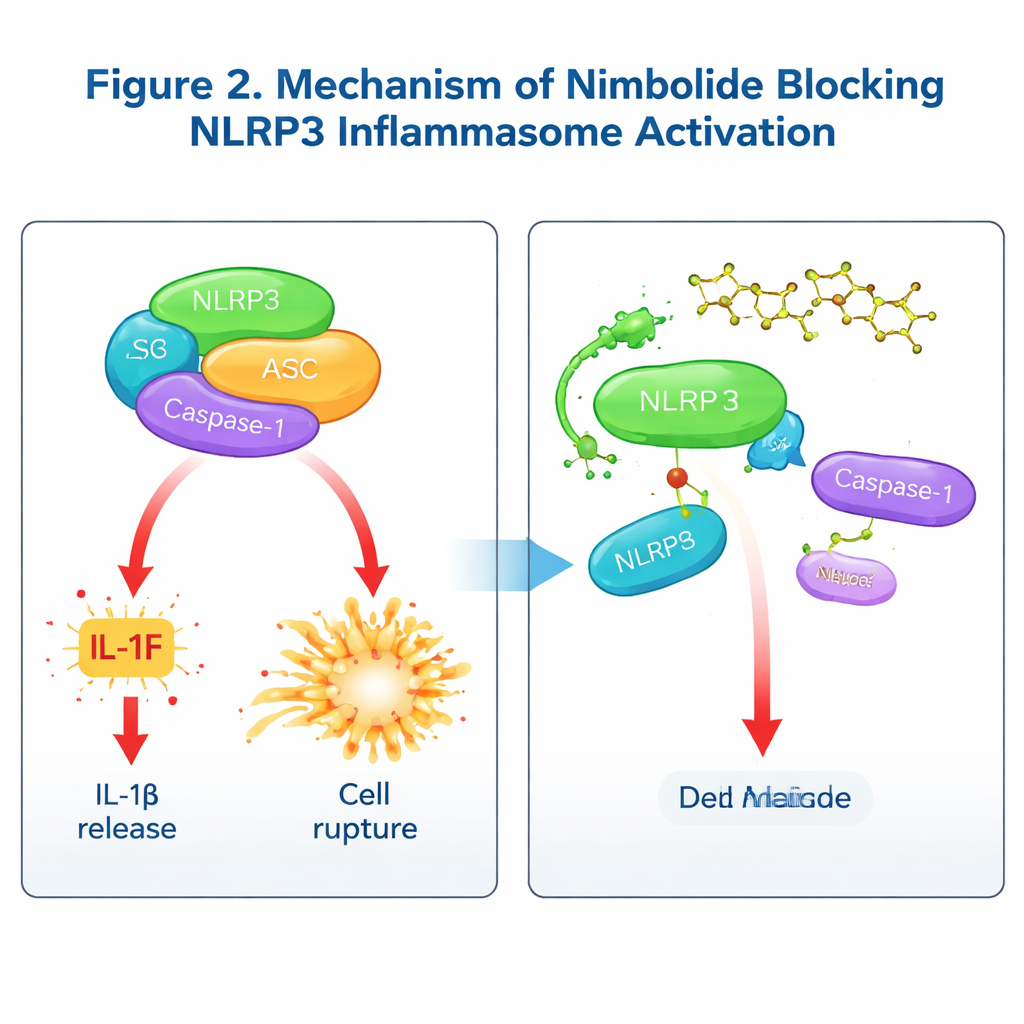
Probando nimbolide en enfermedades de pulmón e intestino
El equipo siguió preguntando si este efecto molecular se traduce en protección real en modelos de enfermedad. En ratones tratados con una toxina bacteriana para inducir SDRA, el nimbolide administrado antes del insulto redujo el daño tisular pulmonar, la acumulación de líquido y la filtración de proteínas en los espacios aéreos. Hubo menos células inmunes infiltradas en los pulmones y menores niveles de IL‑1β tanto en el tejido pulmonar como en sangre. Beneficios similares se observaron en un modelo donde la toxina se administró directamente a las vías respiratorias. En un modelo separado de colitis ulcerosa, en el que los ratones bebieron un químico que lesiona el colon, el nimbolide limitó la pérdida de peso, mejoró la consistencia y el sangrado de las heces, preservó la longitud del colon y redujo los signos microscópicos de inflamación y erosión tisular, junto con la disminución de IL‑1β en el colon. Crucialmente, en ratones genéticamente modificados que carecen de NLRP3, la enfermedad ya era más leve y el nimbolide dejó de aportar beneficio adicional, lo que subraya que sus efectos protectores dependen de bloquear NLRP3.
Qué podría significar esto para tratamientos futuros
Para el público general, la lección clave es que el nimbolide actúa como un freno inteligente sobre uno de los interruptores inflamatorios más potentes del organismo. Al unirse a un sitio preciso en NLRP3 y evitar que el inflamasoma se arme, calma la inflamación excesiva tanto en pulmones como en intestino sin apagar de forma general las defensas inmunitarias. Aunque el nimbolide en sí necesitará mejoras en aspectos como estabilidad y administración antes de poder convertirse en medicamento, este trabajo lo posiciona como un punto de partida prometedor —y como un plano— para diseñar fármacos de nueva generación contra enfermedades impulsadas por NLRP3, como el SDRA y la colitis ulcerosa.
Cita: Xu, H., Lin, Y., Luo, W. et al. Nimbolide ameliorates ARDS and ulcerative colitis by disrupting NLRP3 inflammasome activation. Commun Biol 9, 246 (2026). https://doi.org/10.1038/s42003-026-09524-y
Palabras clave: nimbolide, inflamasoma NLRP3, inflamación, síndrome de distrés respiratorio agudo, colitis ulcerosa