Clear Sky Science · es
Estudio de asociación a escala del epigenoma de la interleucina-6 circulante conecta la metilación del ADN con la salud inmunometabólica e inflamatoria
Por qué esto importa para la salud cotidiana
La inflamación crónica de bajo grado moldea silenciosamente nuestro riesgo de enfermedades como la diabetes tipo 2, las enfermedades cardiovasculares y la enfermedad inflamatoria intestinal. Un actor clave en este proceso es una proteína de señalización en la sangre llamada interleucina‑6 (IL‑6). Este estudio plantea una pregunta fundamental: ¿cómo interacciona la IL‑6 con nuestro epigenoma —las marcas químicas en el ADN que ayudan a controlar la actividad genética— y qué significa eso para nuestra salud a largo plazo?
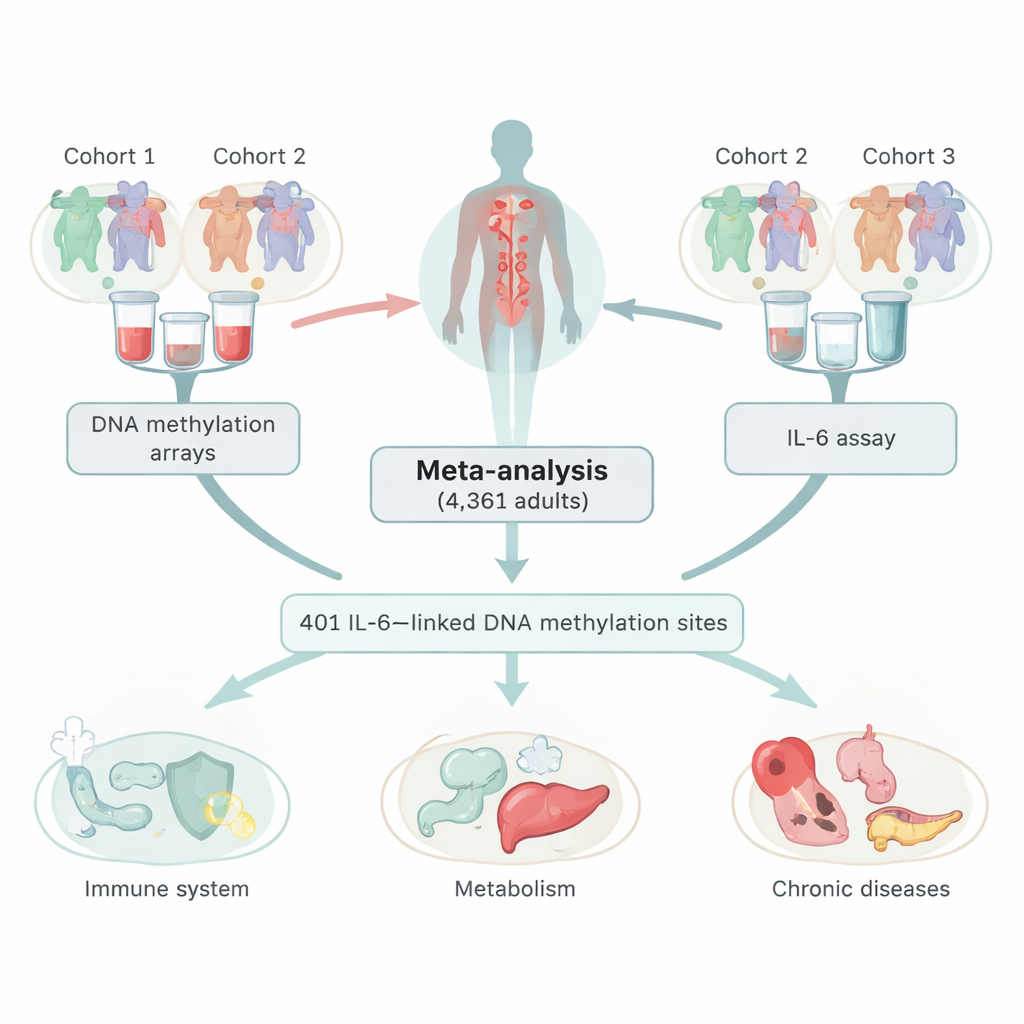
Examinando marcadores químicos en el ADN
Los investigadores combinaron datos de tres grandes estudios europeos, abarcando 4.361 adultos que donaron muestras de sangre. En estas muestras midieron tanto los niveles de IL‑6 como la metilación del ADN, una marca química común en el ADN que puede aumentar o disminuir la actividad de los genes sin cambiar el código genético. Al escanear más de 400.000 sitios a lo largo del genoma identificaron 401 ubicaciones donde los niveles de metilación se correlacionaron con la cantidad de IL‑6 circulante. La mayoría de estos sitios mostró un patrón inverso: niveles más altos de IL‑6 iban de la mano con menor metilación en esos puntos. El equipo comprobó cuidadosamente que estos vínculos no fuesen simplemente efectos secundarios del tabaquismo, diferencias en tipos celulares sanguíneos o de otro marcador inflamatorio llamado proteína C reactiva (CRP).
Conectando inflamación con metabolismo y enfermedad
A continuación, los autores preguntaron si estos sitios de ADN vinculados a la IL‑6 se solapaban con señales observadas en otros grandes estudios epigenéticos. Encontraron un fuerte enriquecimiento para rasgos con un componente inflamatorio o metabólico, incluyendo índice de masa corporal, lípidos sanguíneos, presión arterial, glucemia, diabetes tipo 2, enfermedad renal crónica y afecciones psiquiátricas y relacionadas con el estrés. Muchos de los mismos sitios de metilación ya se habían asociado anteriormente con la CRP, pero los patrones sugirieron que la IL‑6 y la CRP aportan firmas epigenéticas en parte distintas. En otras palabras, las marcas químicas asociadas con la IL‑6 no son una copia exacta de las asociadas con la CRP y pueden aportar información adicional sobre el estado inflamatorio y metabólico de una persona.
Dónde en el genoma ocurre la actividad
Para entender qué podrían estar haciendo estos sitios de metilación, el equipo los mapeó sobre regiones regulatorias conocidas del genoma. Encontraron que los sitios asociados a la IL‑6 se concentraban en elementos de control activos, como los enhancers —fragmentos de ADN que ayudan a activar genes— en lugar de en regiones silenciosas. Esos sitios también estaban cerca de secuencias de unión para factores de transcripción que regulan directamente la IL‑6 y las respuestas al estrés, incluidos NF‑κB, Atf4, CHOP y Nrf2. Al combinar los datos de metilación con grandes conjuntos de datos de expresión génica, los investigadores vincularon más de 400 genes a los sitios relacionados con la IL‑6. Muchos de esos genes están en el centro del control inmunitario y metabólico, incluidos SOCS3, IL6R, AIM2, IFI16, MTOR y RORC, y participan en vías que impulsan la activación y el uso de energía en un tipo especializado de célula T (células Th17) implicada en enfermedades inflamatorias crónicas.
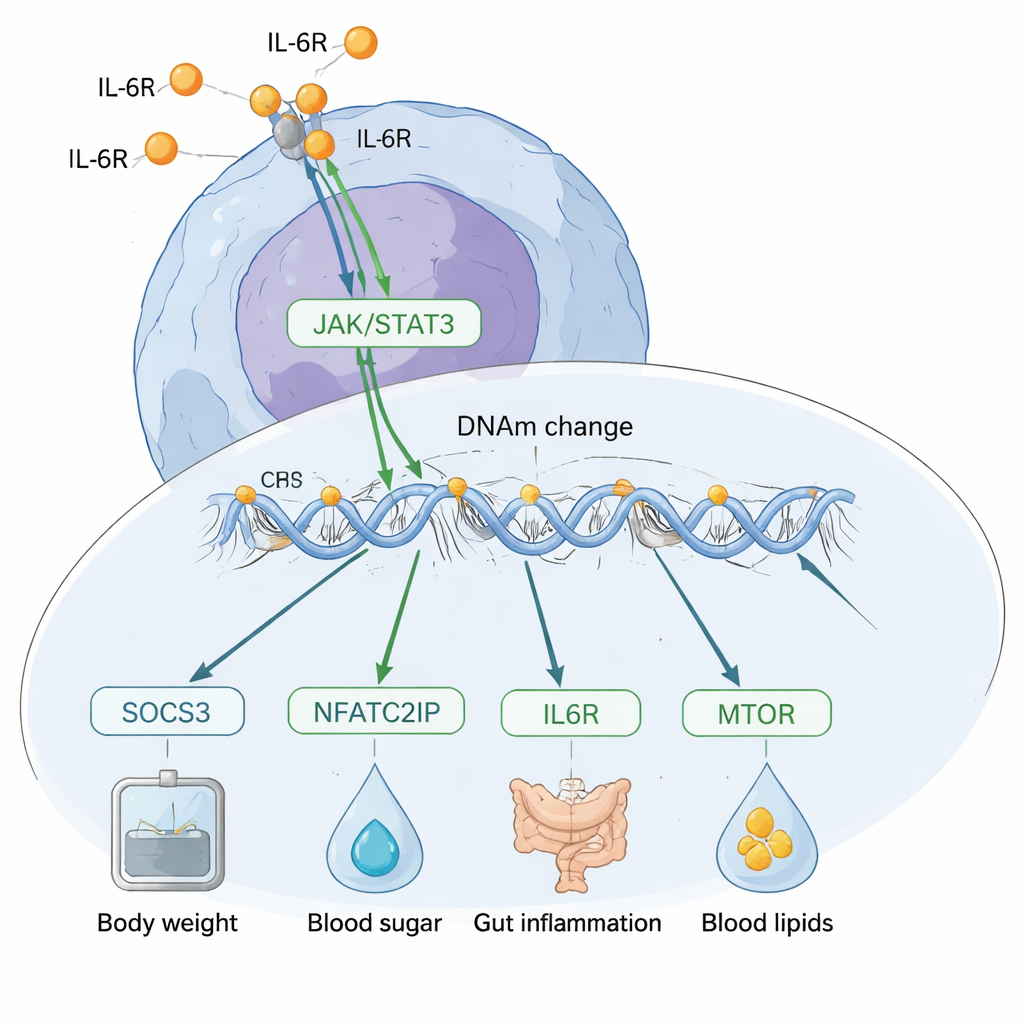
¿En qué dirección va la causa y el efecto?
Un reto importante es determinar si la metilación del ADN está provocando cambios en la IL‑6, o si la IL‑6 está remodelando la metilación. El equipo empleó varias estrategias genéticas para sondear esta dirección. En todo el genoma, sus análisis de “triangulación” respaldaron un modelo en el que la IL‑6 principalmente impulsa cambios en la metilación del ADN, más que al revés. Luego se centraron en sitios específicos y encontraron que los cambios de metilación cerca del gen SOCS3 parecen mediar el impacto de la IL‑6 en factores de riesgo como el peso corporal, el colesterol, los niveles de CRP y la enfermedad inflamatoria intestinal. En contraste, un sitio destacado cercano a un regulador génico llamado NFATC2IP mostró signos de influir en la propia producción de IL‑6 y también pareció afectar múltiples condiciones, incluido el índice de masa corporal, la diabetes tipo 2 y la inflamación intestinal.
Qué significa esto para la prevención y el tratamiento futuros
Para un lector no especialista, el mensaje central es que la IL‑6 y las marcas epigenéticas en el ADN están estrechamente entrelazadas en formas que afectan a muchas enfermedades comunes. La mayor parte del tiempo, la IL‑6 parece dejar una “huella” química en el genoma, especialmente en células inmunitarias, marcando y posiblemente estabilizando estados proinflamatorios. En algunos sitios clave, sin embargo, la metilación podría ayudar a fijar cuánto IL‑6 se produce y cuán intensamente responden las vías inmunitarias. Estos hallazgos señalan a los patrones de metilación del ADN como indicadores prometedores basados en sangre del estado inflamatorio y metabólico, y sugieren que cambios epigenéticos cuidadosamente dirigidos —especialmente alrededor de genes como SOCS3 y NFATC2IP— podrían algún día complementar los fármacos que bloquean la IL‑6 en la prevención o el tratamiento de enfermedades crónicas.
Cita: Sinke, L., van Dongen, J., Delerue, T. et al. Epigenome-wide association study of circulating interleukin-6 connects DNA methylation to immunometabolic and inflammatory health. Commun Biol 9, 242 (2026). https://doi.org/10.1038/s42003-026-09520-2
Palabras clave: interleucina-6, metilación del ADN, inflamación, enfermedad metabólica, epigenética