Clear Sky Science · es
MAT2A aumenta la transcripción de PARN a través de SRF para acelerar la glucólisis y promover la progresión maligna en el osteosarcoma
Por qué importa este estudio sobre el cáncer óseo
El osteosarcoma es el cáncer óseo más frecuente en niños y adolescentes, y los tratamientos apenas han cambiado en décadas. Muchos pacientes jóvenes siguen afrontando malos resultados, sobre todo si el cáncer se disemina o es resistente a la quimioterapia. Este estudio descubre una proteína “interruptor maestro” oculta llamada MAT2A que ayuda a las células de osteosarcoma a crecer, reconfigurar su uso de energía y formar tumores agresivos, y muestra que un fármaco dirigido contra MAT2A puede frenar o reducir estos tumores en modelos de laboratorio.
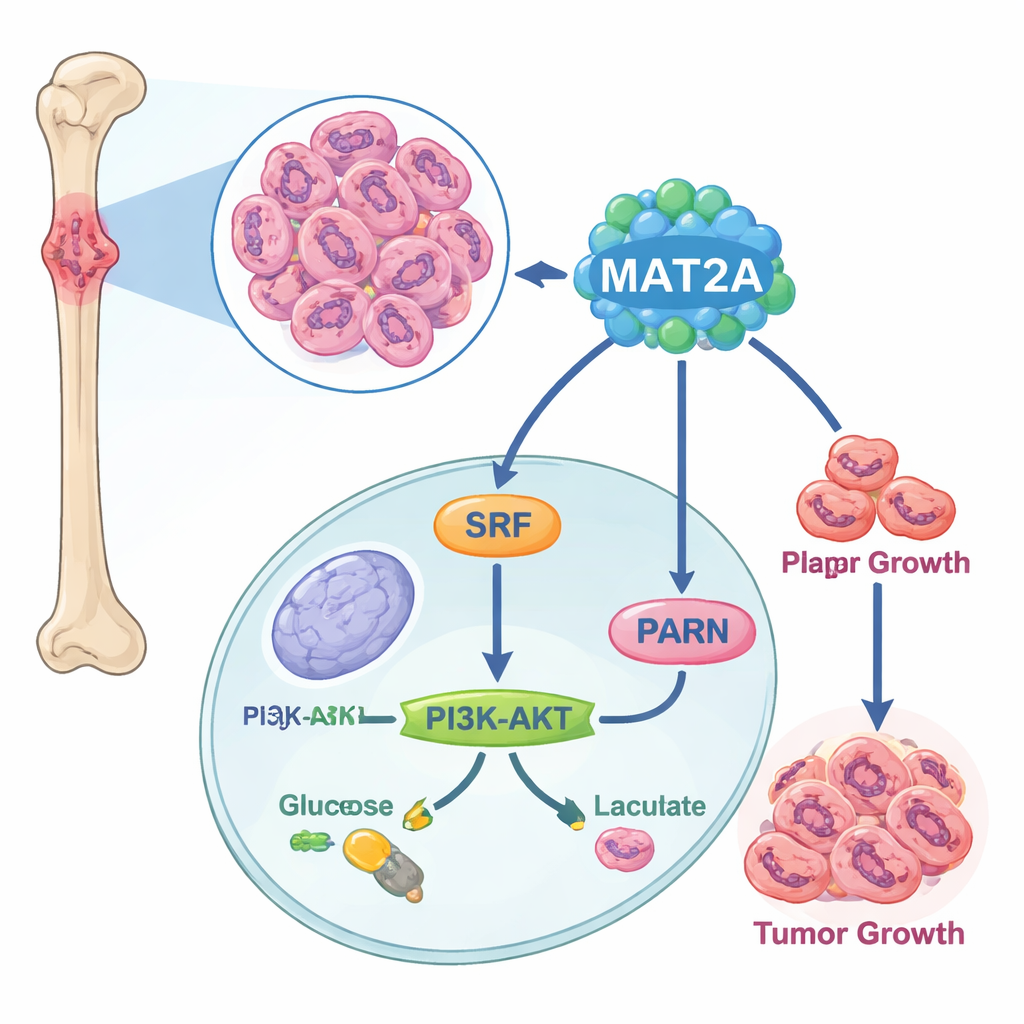
Un motor escondido dentro de las células tumorales
Los investigadores empezaron comparando muestras de cáncer óseo con tejido óseo normal a nivel de célula única. Encontraron que el tejido de osteosarcoma contiene más células que construyen el tumor y menos células inmunitarias, y que un gen en particular—MAT2A—estaba inusualmente activo en las células cancerosas. Análisis de bases de datos públicas de cáncer y de líneas celulares cultivadas en el laboratorio confirmaron que los niveles de MAT2A eran mucho más altos en osteosarcoma que en células óseas sanas, y que los pacientes con más MAT2A tendían a tener enfermedad más avanzada y afectación de ganglios linfáticos. Esto situó a MAT2A en el centro de atención como un posible impulsor de la enfermedad más que como un mero espectador.
Reducir MAT2A frena el crecimiento del cáncer
Para comprobar la importancia real de MAT2A en el comportamiento tumoral, el equipo empleó herramientas genéticas para bajar los niveles de MAT2A en líneas celulares de osteosarcoma. Cuando se silenció MAT2A, las células cancerosas se dividieron más despacio y fueron más propensas a sufrir muerte celular programada. En ratones implantados con estas células modificadas, los tumores crecieron mucho más despacio y fueron significativamente más pequeños, aunque el peso corporal de los animales permaneció estable. Estos experimentos demostraron que las células de osteosarcoma dependen en gran medida de MAT2A tanto para la supervivencia como para su capacidad de formar tumores.
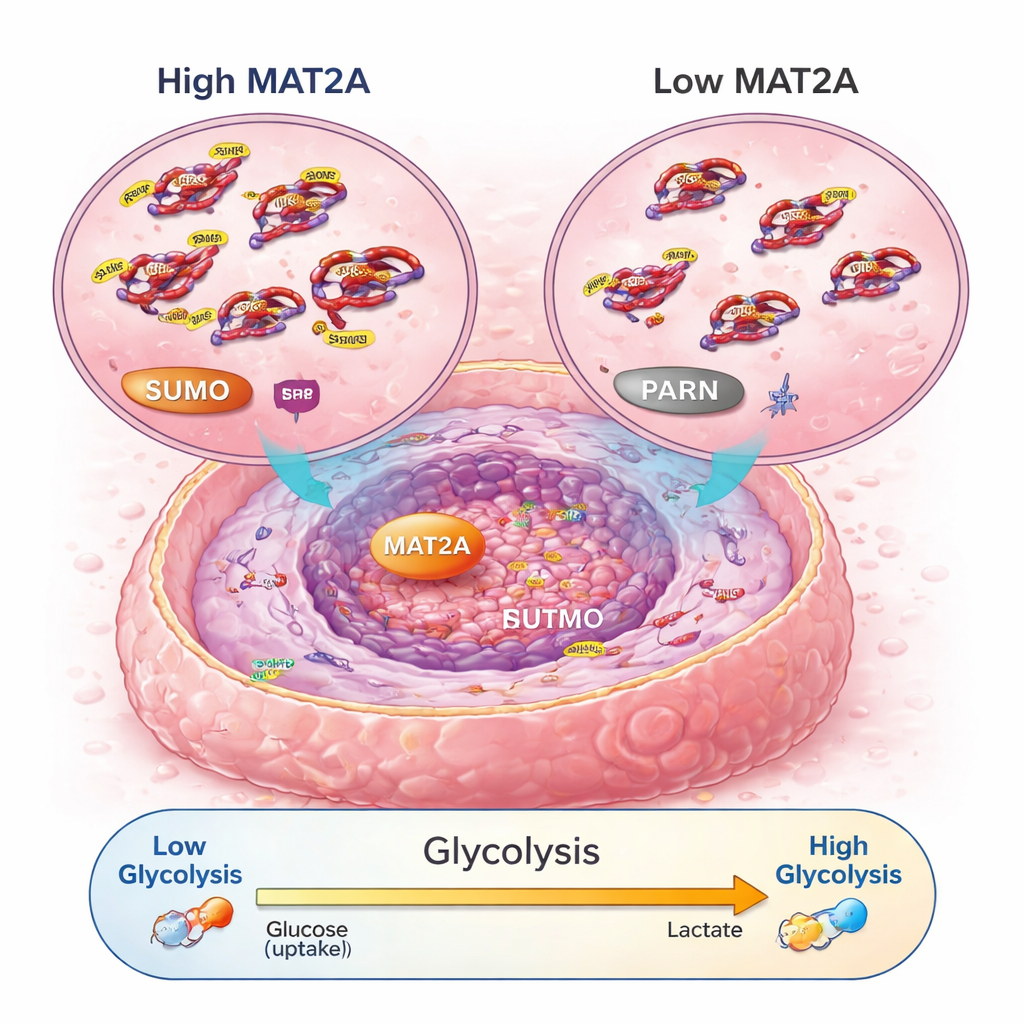
Un relevo de señales que potencia el consumo de combustible celular
Indagando más, los científicos descubrieron que MAT2A hace más que su función metabólica habitual. Dentro del núcleo se une a un factor de transcripción llamado SRF, ayudando a mantener SRF estable y activo al promover una etiqueta química conocida como SUMO. A su vez, SRF activa un gen llamado PARN, que entonces pone en marcha la conocida vía PI3K–AKT y aumenta la maquinaria de la glucólisis aeróbica—una forma rápida pero ineficiente de generar energía que favorecen las células cancerosas. Cuando se redujo MAT2A, las células cancerosas produjeron menos ATP (su moneda energética), captaron menos glucosa, generaron menos ácido láctico y se desplazaron de nuevo hacia una respiración más tranquila y dependiente del oxígeno. Interferir con PARN o AKT pudo deshacer los efectos pro‑crecimiento y pro‑glucólisis de MAT2A, confirmando que este relevo—MAT2A a SRF a PARN a PI3K–AKT—actúa como un circuito clave de energía y crecimiento en el osteosarcoma.
Un papel no tradicional y un objetivo farmacológico
De manera llamativa, una versión de MAT2A que carecía de su actividad enzimática normal seguía apoyando la estabilidad de SRF y la activación de PARN, lo que indica que este papel promotor del cáncer no depende de su reacción química habitual. En cambio, MAT2A actúa más como un andamio que organiza otras proteínas. Esto tiene implicaciones prácticas: los fármacos no necesitan necesariamente bloquear su centro catalítico para debilitar los tumores. Los investigadores probaron un inhibidor de pequeña molécula llamado FIDAS‑5, diseñado para atacar MAT2A, tanto en cultivos celulares como en modelos de ratón. El tratamiento redujo SRF nuclear, disminuyó la señalización de PARN y PI3K–AKT, atenuó la glucólisis, ralentizó el crecimiento celular y provocó la muerte de células cancerosas. En ratones, FIDAS‑5 redujo o frenó los tumores sin pérdida de peso apreciable, lo que sugiere efectos secundarios tolerables en este contexto.
Qué significa esto para los pacientes y futuras terapias
Para no especialistas, el mensaje esencial es que las células de osteosarcoma dependen de MAT2A para mantener sus programas de crecimiento y sus motores de quema de azúcar a plena velocidad. Al estabilizar proteínas de control clave y potenciar una cadena de señales, MAT2A ayuda a los tumores a crecer más rápido y volverse más agresivos. Bloquear esta proteína—ya sea por métodos basados en genes o con un fármaco como FIDAS‑5—corta ese soporte, obligando a las células cancerosas a desacelerarse, consumir energía de forma menos frenética y, en última instancia, morir. Aunque queda mucho trabajo antes de que tales tratamientos lleguen a la clínica, este estudio posiciona a MAT2A como un objetivo prometedor en la lucha contra el cáncer óseo, abriendo una vía potencial hacia terapias más precisas y menos tóxicas para pacientes jóvenes.
Cita: Ren, Z., Chen, H., Qiao, Q. et al. MAT2A enhances PARN transcription via SRF to accelerate glycolysis and drive malignant progression in osteosarcoma. Commun Biol 9, 241 (2026). https://doi.org/10.1038/s42003-026-09518-w
Palabras clave: osteosarcoma, MAT2A, metabolismo del cáncer, vía PI3K AKT, terapia dirigida