Clear Sky Science · es
Análisis computacional de la heterogeneidad de epítopos en inmunotinciones a partir de series de dilución de anticuerpos
Por qué importa la calidad de la tinción con anticuerpos
Desde el seguimiento de células cancerosas hasta el diagnóstico de infecciones, la biología moderna depende en gran medida de anticuerpos que «iluminan» moléculas específicas dentro de las células. Sin embargo, muchos laboratorios lidian a escondidas con un problema persistente: tinciones demasiado débiles, con mucho ruido o simplemente engañosas. Este artículo presenta un método práctico, basado en ordenador, para extraer más información de una serie de dilución de anticuerpos rutinaria, ayudando a los investigadores a ajustar sus tinciones para obtener imágenes más nítidas, mediciones más fiables e incluso nuevas maneras de teñir varios objetivos en un único canal de color. 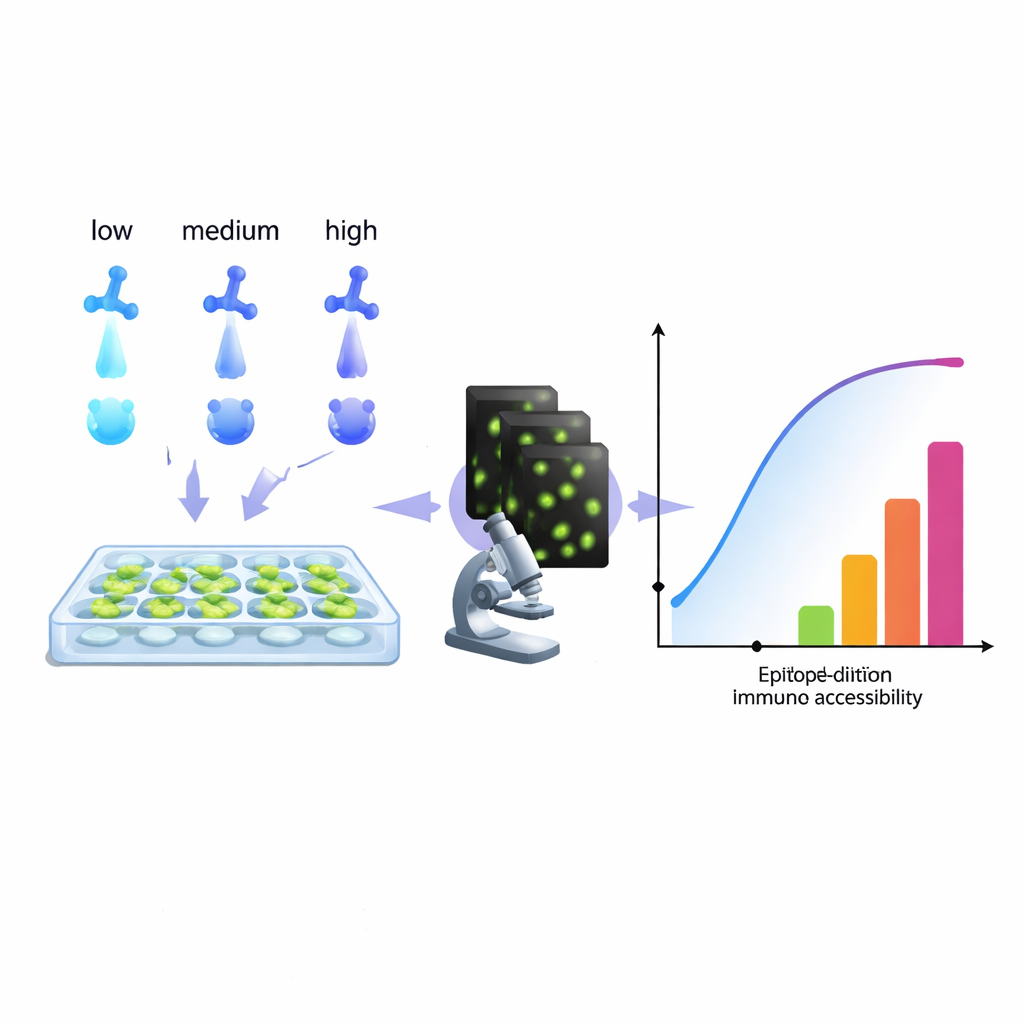
Cómo suelen optimizar los científicos las tinciones con anticuerpos
Cuando los investigadores montan un experimento de inmunotinción, normalmente estiman una concentración de anticuerpo a partir de la hoja de datos, prueban unas pocas diluciones y eligen la que «se ve bien». Sin embargo, detrás de esa decisión influyen numerosos factores diminutos: la conformación de la proteína, el hacinamiento dentro de las células, el pH y la capacidad del anticuerpo para encajarse en su sitio; todos ellos determinan si un anticuerpo se mantiene ligado o se elimina con el lavado. Las herramientas tradicionales que miden la unión de anticuerpos, como la resonancia de plasmón superficial, funcionan mejor con proteínas purificadas en superficies artificiales, no con células o tejidos densamente empaquetados. Eso significa que los valores que proporcionan pueden no coincidir con el sistema biológico real donde se usan los anticuerpos. Como resultado, los laboratorios pueden elegir sin saber concentraciones que aumenten el fondo borroso o que oculten dianas importantes pero menos accesibles.
Convertir series de dilución simples en «mapas de accesibilidad»
Los autores proponen un enfoque distinto: tratar una serie típica de dilución de anticuerpos como un conjunto de datos rico y ajustarlo con un modelo que refleje lo que realmente ve la imagen—anticuerpos que permanecen unidos incluso después de lavados repetidos. Analizando cómo crece la señal con la concentración, su algoritmo reconstruye un «histograma de accesibilidad». En lugar de intentar aislar constantes químicas puras de unión, este histograma agrupa sitios diana en «clases de epítopos» técnicas según lo fácil que resulta teñirlos en condiciones reales. Un mismo epítopo biológico puede aparecer en varias clases si, por ejemplo, es fácil de alcanzar en una parte de la célula y más difícil en una región congestionada. Crucialmente, este método funciona directamente con la lectora del microscopio, sin necesitar proteínas purificadas ni hardware adicional, por lo que cualquier laboratorio que pueda ejecutar una serie de diluciones y cuantificar la fluorescencia puede, en principio, construir tales histogramas. 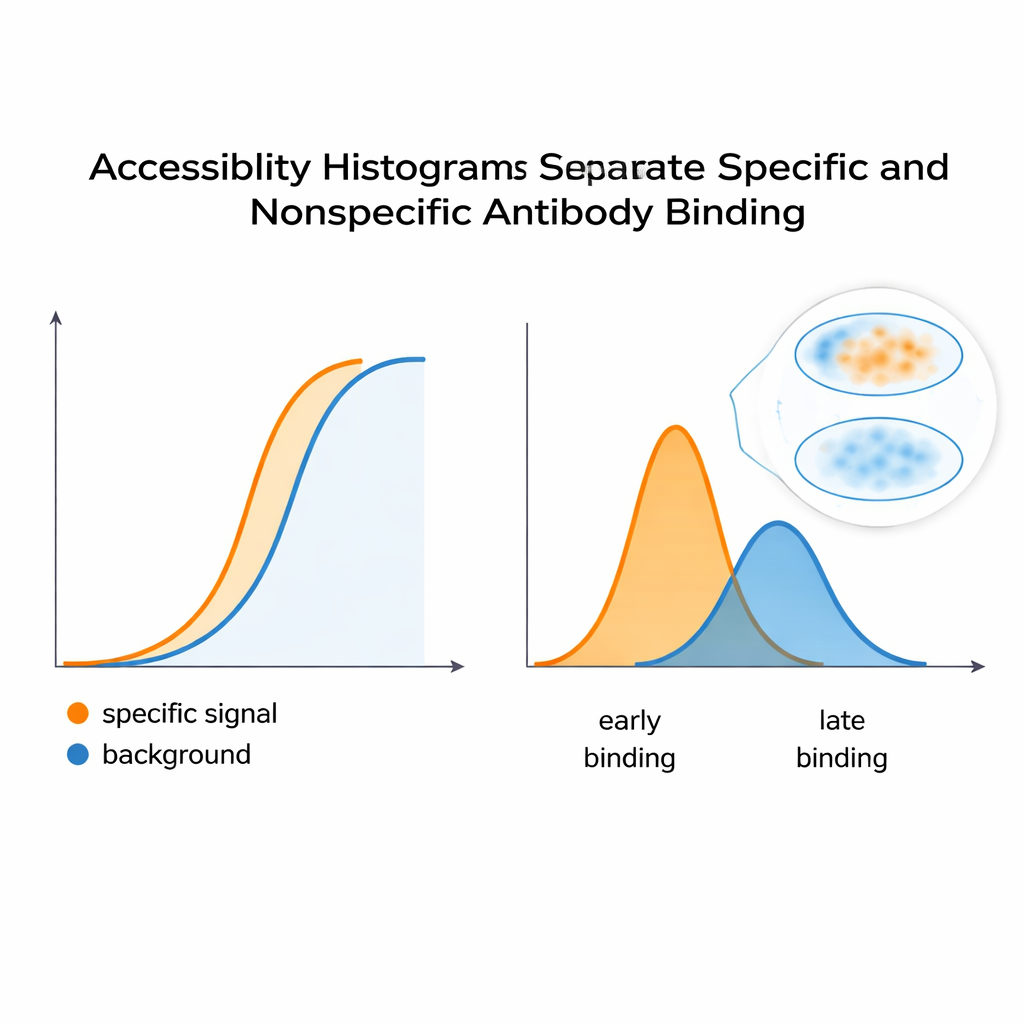
Separar la señal real del fondo
Para comprobar si estos histogramas capturan realmente el comportamiento de la tinción, el equipo construyó un sistema controlado usando células HeLa y dos anticuerpos monoclonales: uno que imita una señal específica deseada y otro que actúa como fondo no deseado. Cuando se mezclaron, la curva de fluorescencia combinada parecía una única respuesta suave—nada evidente sugería dos contribuyentes distintos. Pero el análisis computacional dividió esa curva en picos separados en el histograma de accesibilidad, revelando al menos dos clases de epítopos subyacentes. Una estrategia similar aplicada a un anticuerpo que reconoce un sitio sensible a la conformación en una subunidad reguladora de PKA mostró que cambios en la conformación proteica—inducidos por la molécula cAMP—desplazaron la distribución de epítopos accesibles. Esto sugiere que el método puede detectar cuando las estructuras proteicas se abren o se cierran, cambiando la facilidad con la que los anticuerpos pueden unirse dentro de las células.
Elegir mejores diluciones y teñir más con un solo color
Como cada pico en el histograma de accesibilidad contribuye principalmente en un cierto rango de concentraciones, los autores usan estos picos como guía para escoger diluciones «óptimas». Los picos de baja accesibilidad que aparecen solo a niveles muy altos de anticuerpo probablemente incluyan unión inespecífica, mientras que los picos tempranos suelen reflejar la diana prevista. Al modelar cómo los picos individuales construyen la curva global de respuesta a la dosis, el equipo puede sugerir diluciones que maximizan la señal específica antes de que aparezcan picos problemáticos—a veces mucho más diluidas que las recomendaciones del proveedor. Además, extienden esta idea hacia una forma ingeniosa de «multiplexación computacional». Tiñendo la misma muestra fija repetidamente con concentraciones cuidadosamente elegidas, obteniendo imágenes después de cada ronda y restando imágenes anteriores de las posteriores, aíslan señales vinculadas a diferentes clases de accesibilidad, separando efectivamente múltiples dianas dentro de un único canal de fluorescencia.
Qué implica esto para el trabajo cotidiano de laboratorio
En términos sencillos, este trabajo convierte un paso rutinario de resolución de problemas—realizar una serie de dilución de anticuerpos—en una herramienta cuantitativa. Los histogramas de accesibilidad ayudan a los científicos a detectar complejidad oculta en sus tinciones, elegir diluciones que reduzcan un fondo engañoso y, en algunos casos, separar señales superpuestas sin necesidad de etiquetas fluorescentes adicionales. Aunque el modelo subyacente es intencionadamente simple y no captura cada detalle molecular, está diseñado para ser fácil de usar y lo suficientemente robusto para datos del mundo real. Si se adoptara ampliamente, este enfoque podría hacer las técnicas basadas en anticuerpos—desde la microscopía básica hasta ensayos diagnósticos—más fiables, más informativas y menos dependientes del ensayo y error.
Cita: Tschimmel, D., Saeed, M., Milani, M. et al. Computational epitope heterogeneity analysis in immunostainings from antibody-dilution series. Commun Biol 9, 238 (2026). https://doi.org/10.1038/s42003-026-09517-x
Palabras clave: tinción con anticuerpos, inmunofluorescencia, accesibilidad de epítopos, respuesta a la dosis, multiplexación computacional