Clear Sky Science · es
Avances estratégicos para estudios estructurales por cryo-EM de GPCRs pequeños (<100 kDa)
Por qué importan para la medicina estos pequeños interruptores celulares
Gran parte de la medicina moderna actúa mediante un suave empujón a pequeños interruptores situados en las membranas celulares, llamados receptores acoplados a proteína G (GPCRs). Estos sensores detectan hormonas, olores y fármacos, y alrededor de un tercio de los medicamentos aprobados actúa sobre ellos. Para diseñar fármacos más seguros e inteligentes, los científicos necesitan imágenes 3D detalladas de estos receptores, especialmente en sus formas "apagadas" o inactivas, a las que muchos fármacos se dirigen específicamente. Este artículo explica cómo los investigadores están aprendiendo a ver algunos de los GPCRs más pequeños con criomicroscopía electrónica (cryo-EM), un potente método de imagen que permite observar moléculas congeladas en un estado casi natural.
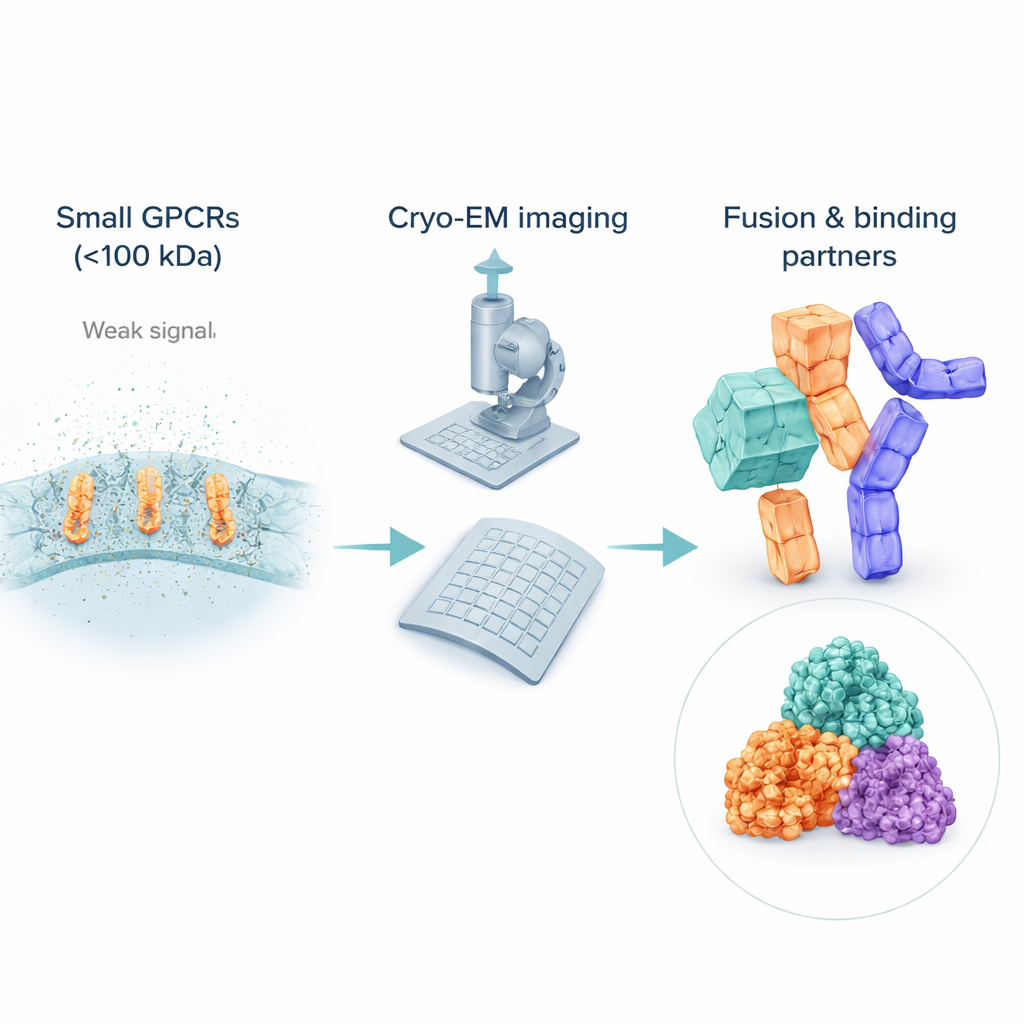
El desafío de ver receptores muy pequeños
Aunque la cryo-EM ha revolucionado la biología estructural, todavía tiene dificultades con moléculas pequeñas y flexibles. Muchos GPCRs inactivos pesan mucho menos de 100 kilodaltons, lo que los hace difíciles de detectar y alinear en imágenes ruidosas. Para mantenerlos solubles, los científicos envuelven estos receptores en burbujas de detergente o en análogos lipídicos, que a menudo parecen "más grandes" ante el haz de electrones que el propio receptor, ocultando la señal de la proteína de interés. A diferencia de los receptores activos, que están unidos a parejas voluminosas como las proteínas G, los GPCRs inactivos suelen carecer de rasgos externos prominentes, por lo que los algoritmos tienen dificultades para promediar muchas imágenes en una vista 3D nítida. Como resultado, la mayoría de las estructuras de GPCR inactivos todavía provienen de métodos más antiguos de rayos X, dejando un hueco en la cobertura por cryo-EM justo en el lugar donde actúan muchos fármacos.
Aumentar el tamaño de los receptores con ayudantes incorporados
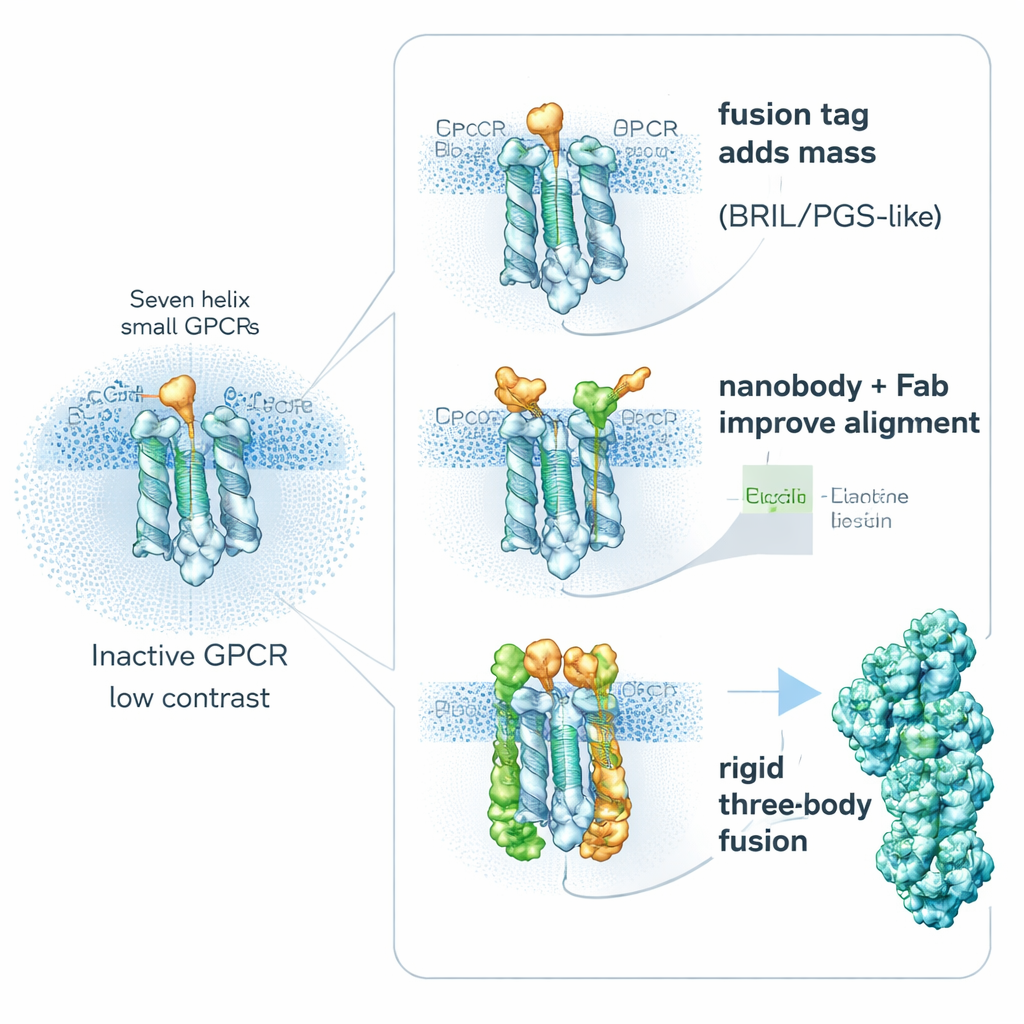
Una estrategia clave es sorprendentemente simple: hacer el receptor "más pesado" a propósito. Los investigadores fusionan genéticamente pequeñas proteínas auxiliares estables en partes flexibles de los GPCRs para aumentar su tamaño y rigidez, sin bloquear las regiones importantes de unión a fármacos. Entre los auxiliares populares están BRIL (un haz de cuatro hélices), PGS (un fragmento enzimático termoestable) y una proteína mayor en forma de abrazadera llamada calcineurina. Estos socios de fusión suelen insertarse en un bucle interno móvil que conecta dos hélices. Al rigidizar esa región, reducen el desenfoque causado por el movimiento molecular y proporcionan formas reconocibles que ayudan a los algoritmos a alinear las partículas. Los estudios muestran que la posición y orientación exactas del fragmento de fusión pueden decidir el éxito del proyecto: en un receptor, una etiqueta PGS colocada en un sitio diferente mejoró la resolución de unos borrosos 6 angstroms a unos mucho más claros 3,7 angstroms.
Tomar prestadas anticuerpos y ligandos diseñados como asas
Una segunda vía evita añadir grandes fusiones al receptor y, en su lugar, conecta "asas" de alta afinidad desde el exterior. Fragmentos diminutos de anticuerpos llamados nanocuerpos y ligandos relacionados pueden generarse para reconocer GPCRs inactivos y fijarse a bucles internos flexibles. Un ejemplo destacado es Nanobody-6, que se creó inicialmente como sensor para un receptor opioide y luego se reutilizó, con ajustes modestos, para estabilizar varios otros GPCRs en sus formas inactivas. Como se une fuera del centro, proporciona a cada partícula una clara pista de orientación, lo que hace que el promediado de imágenes sea más fiable. Los investigadores suelen extender esta idea añadiendo una segunda capa: un fragmento de anticuerpo convencional que reconoce al nanocuerpo, creando así un complejo más voluminoso y rígido que aparece nítidamente en cryo-EM. Otros ligandos diseñados, como los DARPins, pueden usarse como espaciadores modulares o como conectores a jaulas proteicas mayores, incrementando aún más la señal de objetivos muy pequeños.
Diseño de muestras más inteligente y procesamiento de imágenes potenciado por IA
Fusionar ayudantes o añadir ligandos es solo parte de la historia. La revisión subraya que las buenas estructuras comienzan con constructos de receptor cuidadosamente diseñados: recortar regiones terminales flexibles, introducir mutaciones estabilizadoras y emplear herramientas modernas de predicción estructural para identificar partes que puedan causar problemas. En la parte de imagen, trucos más antiguos como las placas de fase, que aumentan el contraste de partículas débiles, se complementan o incluso son reemplazados por herramientas basadas en inteligencia artificial. Programas de aprendizaje profundo pueden detectar pequeñas partículas ocultas en micrografías ruidosas, y nuevos algoritmos pueden clasificar imágenes en diferentes conformaciones cuando los receptores exploran múltiples formas. Junto con auxiliares de referencia, estos avances empujan a la cryo-EM hacia la resolución confiable de proteínas de membrana que antes se consideraban demasiado pequeñas o demasiado dinámicas para estudiar.
Qué implica esto para los fármacos del futuro
El artículo concluye que no existe un único "ayudante mágico" que funcione para todos los receptores, pero una caja de herramientas en expansión de socios de fusión, ligandos tipo anticuerpo y métodos impulsados por IA está abriendo de manera constante el paisaje inactivo de los GPCRs a la cryo-EM. Para los no expertos, la idea clave es que, haciendo que los receptores pequeños parezcan más grandes y ordenados para el microscopio, los científicos pueden por fin obtener instantáneas detalladas de las formas exactas que muchos fármacos prefieren unir. Estos planos estructurales deberían acelerar el diseño de medicamentos que apaguen con mayor precisión estos interruptores celulares—o ajusten finamente su actividad—con menos efectos secundarios.
Cita: Singh, S.K., Agrawal, M., Pattanayak, A. et al. Strategic advances for cryo-EM structural studies of small (<100 kDa) GPCRs. Commun Biol 9, 237 (2026). https://doi.org/10.1038/s42003-026-09516-y
Palabras clave: Receptores acoplados a proteína G, Criomicroscopía electrónica, Descubrimiento de fármacos, Biología estructural, Andamios de nanocuerpos