Clear Sky Science · es
Vincular la tensión molecular y las tracciones celulares: un enfoque multiescala para la mecánica de las adhesiones focales
Cómo las células notan y tiran de su entorno
Cada vez que una célula se mueve, se divide o remodela un tejido, está tirando silenciosamente de su entorno. Estas pequeñas fuerzas mecánicas son cruciales en la cicatrización, la diseminación del cáncer y el desarrollo de los órganos, pero son difíciles de ver y aún más difíciles de medir. Este estudio presenta una nueva forma de observar esas fuerzas desde dos ángulos a la vez: cuánto tira una célula entera sobre un material blando y cuánta fuerza soportan los “resortes moleculares” individuales dentro de los puntos de anclaje de la célula. Al vincular estas perspectivas, el trabajo ayuda a explicar cómo las células detectan la rigidez y regulan su agarre sobre el mundo que las rodea.
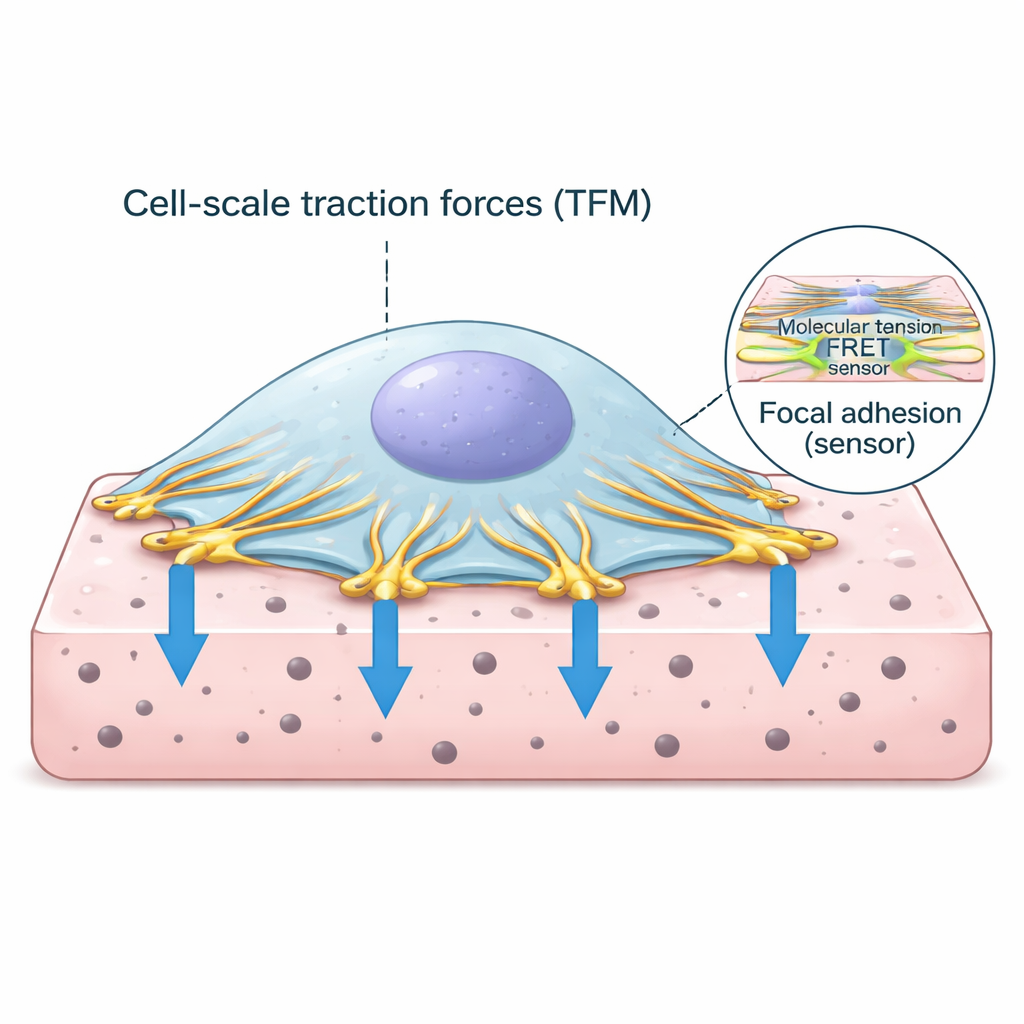
Los puntos de agarre de la célula con el mundo exterior
Las células no flotan simplemente en los tejidos; se anclan mediante puntos de contacto especializados llamados adhesiones focales. En estos sitios, el armazón interno de fibras de actina de la célula se conecta a proteínas que atraviesan la membrana celular y se enganchan a la matriz circundante. Una de las proteínas clave en este complejo de anclaje es la vinculina, que actúa como un enlace sensible a la fuerza. Cuando la maquinaria contráctil de la célula tira de la actina, la vinculina percibe la carga y ayuda a fortalecer la conexión. Comprender cuánta fuerza pasa por estos enlaces y cómo se relaciona con el tirón global de la célula es esencial para descifrar cómo los tejidos se mantienen sanos o se vuelven patológicos.
Dos ventanas a la fuerza celular
Los investigadores combinaron dos técnicas potentes en un único flujo de trabajo. Primero, la microscopía de fuerzas de tracción mide cuánto deforma una célula un sustrato blando tipo gel rastreando el movimiento de pequeñas partículas fluorescentes en el gel. A partir de estos desplazamientos de las partículas se puede calcular la distribución de fuerzas de empuje y tracción bajo la célula. Segundo, una versión de la proteína vinculina especialmente diseñada lleva un sensor de tensión fluorescente que cambia su señal lumínica cuando se estira. Mediante imágenes avanzadas de tiempo de vida (lifetime imaging), el equipo convirtió esa señal luminosa en una medida de la tensión molecular sobre la vinculina. Diseñaron hidrogeles delgados y planos que podían imaginarse a alta resolución y escribieron software personalizado para alinear, segmentar y analizar ambos conjuntos de datos hasta el nivel de adhesiones individuales.
Cómo la rigidez cambia el esfuerzo de la célula
Cuando las células se cultivaron sobre geles blandos frente a más rígidos, su comportamiento global cambió de forma clara. En sustratos más rígidos, las células se extendieron más y ejercieron fuerzas de tracción más fuertes sobre la superficie del gel. Al mismo tiempo, la lectura fluorescente del sensor de vinculina indicó una mayor tensión molecular dentro de las adhesiones focales. Curiosamente, las características estructurales básicas de estas adhesiones —como su número o tamaño medio— no cambiaron mucho entre geles blandos y rígidos. En cambio, cambió la organización de las fuerzas. Adhesiones grandes, orientadas radialmente y con más vinculina tendían a soportar mayores tracciones, lo que sugiere que tanto la geometría como la composición molecular de estos sitios contribuyen a determinar con qué fuerza tira la célula.
Una relación compleja entre fuerzas locales y moleculares
Al observar más de cerca adhesiones individuales se reveló que el vínculo entre la tracción local y la tensión en la vinculina no es universal. En algunas células, las adhesiones que generaban mayores tracciones también mostraban mayor tensión en la vinculina, lo que implica que los contactos comprometidos y portadores de carga comparten la fuerza más directamente a través de sus enlaces moleculares. En otras células apareció el patrón opuesto: regiones de fuerte tracción se asociaron con menor tensión en la vinculina, mientras que otras adhesiones soportaban más carga molecular sin producir grandes tirones hacia el exterior. Muchas células no mostraron patrón claro alguno. Estos comportamientos distintos probablemente reflejan diferentes estados celulares —como extensión activa, adhesión estable o retracción— y sugieren que las células pueden redistribuir fuerzas en su red de adhesiones de múltiples maneras.
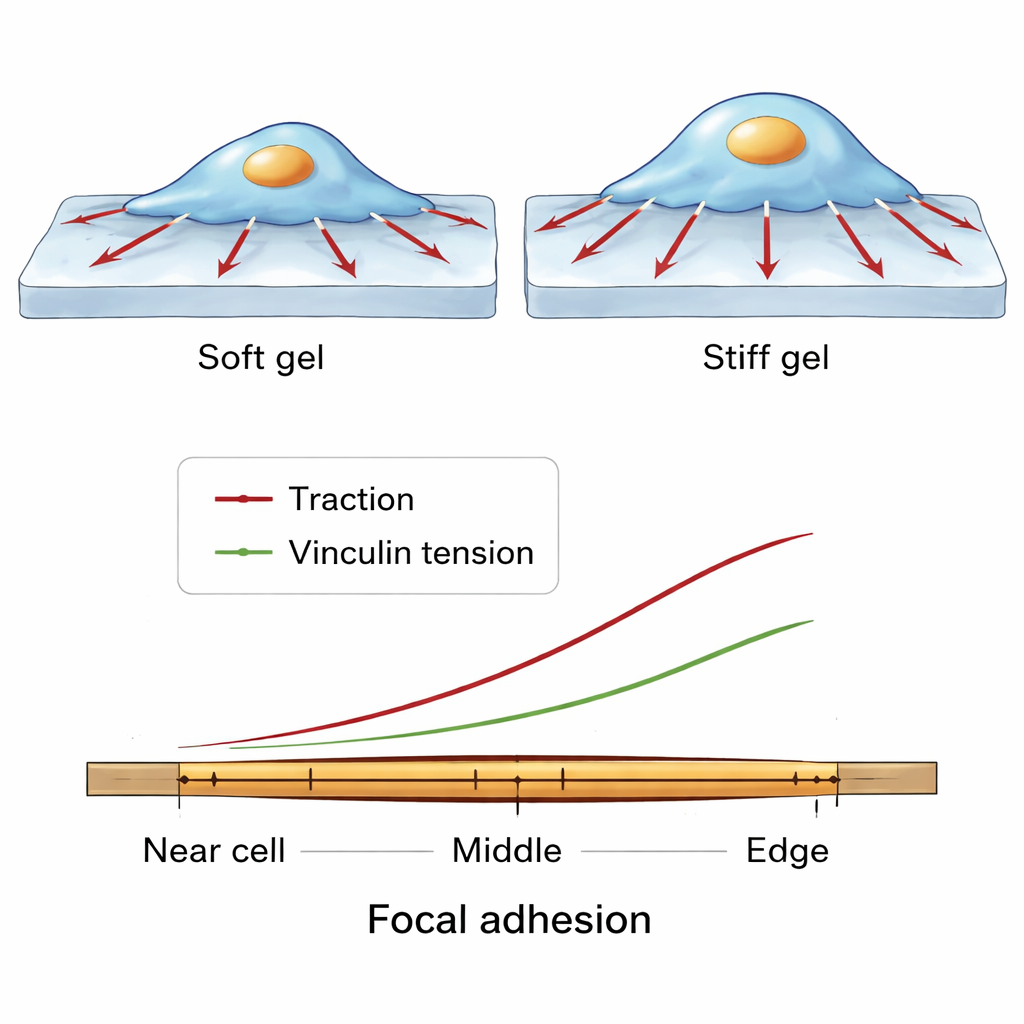
Patrones de fuerza a escala fina a lo largo de un único punto de agarre
El equipo amplió aún más el enfoque, examinando cómo cambian las fuerzas a lo largo de un solo punto de adhesión focal, desde el lado más cercano al centro celular hasta el borde próximo al perímetro. A través de muchas células y condiciones emergió un patrón consistente. Las moléculas de vinculina estaban más densamente agrupadas hacia el centro de la adhesión. Sin embargo, tanto la tracción ejercida sobre el sustrato como la tensión molecular sobre la vinculina aumentaban hacia el extremo exterior, más periférico. Esto sugiere un acto de equilibrio: en las regiones centrales, muchas moléculas de vinculina pueden compartir la carga, de modo que cada una siente menos tensión, mientras que en el borde exterior menos moléculas soportan relativamente más fuerza, permitiendo un fuerte tirón local a la vez que se mantiene la integridad de la adhesión.
Qué significa esto para la salud y la enfermedad
Al fusionar mapas de tracción a escala celular con medidas de tensión a nivel proteico, este estudio ofrece una imagen multiescala de cómo las células gestionan su agarre mecánico. El trabajo muestra que, a medida que el entorno se vuelve más rígido, las células tanto tiran con más fuerza como cargan más sus enlaces de vinculina, pero que la relación detallada entre las fuerzas exteriores y la tensión molecular varía de adhesión en adhesión y de célula a célula. Al mismo tiempo, parece conservarse un patrón espacial robusto de distribución de fuerzas dentro de adhesiones individuales. Para un público no especialista, el mensaje clave es que las células ajustan finamente tanto dónde como cómo tiran, redistribuyendo la fuerza entre muchas pequeñas “muelles” moleculares para adaptarse a distintos entornos mecánicos —un principio que puede subyacer a procesos tan diversos como el desarrollo tisular, la fibrosis y la invasión tumoral.
Cita: Aytekin, S., Kimps, L., Coucke, Q. et al. Linking molecular tension and cellular tractions: a multiscale approach to focal adhesion mechanics. Commun Biol 9, 236 (2026). https://doi.org/10.1038/s42003-026-09514-0
Palabras clave: mecánica celular, adhesiones focales, vinculina, microscopía de fuerzas de tracción, mecanotransducción