Clear Sky Science · es
Dinámica temporal de la escisión colateral de ARN por LbuCas13a en células humanas
Convertir una defensa bacteriana en un eliminador celular de precisión
Los investigadores han descubierto cómo transformar una proteína inmune bacteriana en un interruptor de “autodestrucción” altamente selectivo para células humanas. Aprovechando una enzima CRISPR llamada LbuCas13a, pueden reconocer un mensaje de ARN elegido dentro de una célula y luego destrozar casi todo el resto del ARN de esa célula. Para lectores no especializados, esto resulta fascinante porque los mensajes de ARN controlan qué proteínas produce una célula; aprender a borrarlos a voluntad abre puertas a nuevos tratamientos contra el cáncer, estrategias antivirales y potentes herramientas de investigación.
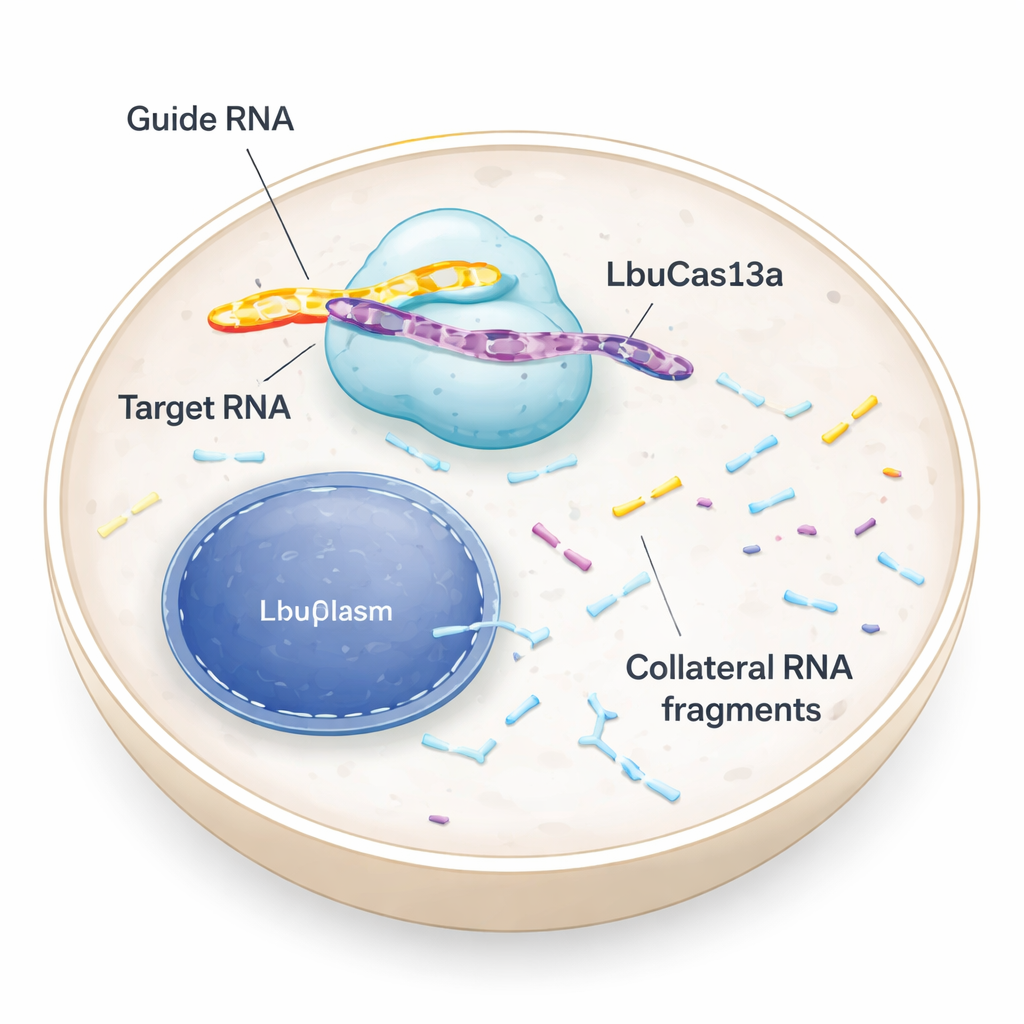
Tijeras moleculares que atacan ARN, no ADN
La mayoría conoce las herramientas CRISPR que cortan ADN y reescriben el código genético. LbuCas13a es diferente: reconoce y corta ARN, los mensajes temporales que llevan instrucciones desde el ADN hasta las fábricas de proteínas de la célula. En bacterias, las enzimas Cas13 forman parte de una defensa antiviral. Una vez que detectan un ARN viral, no solo cortan ese invasor, sino que también empiezan a cortar muchos otros ARN cercanos. Esta actividad “colateral” puede empujar a las células infectadas hacia la latencia o la muerte, ayudando a proteger a la comunidad bacteriana. Pruebas iniciales en células animales y humanas sugerían que el corte colateral de Cas13 era débil o inexistente, por lo que la enzima se usaba principalmente como un “interruptor” preciso para apagar ARN. El nuevo estudio revisita esa suposición y muestra que, en las condiciones adecuadas, la actividad colateral en células humanas puede ser tanto intensa como útil.
Desencadenando el corte colateral en células humanas
El equipo comparó varias variantes de Cas13 y encontró que LbuCas13a era especialmente potente. Introdujeron proteína LbuCas13a purificada pre‑cargada con un ARN guía corto directamente en células humanas, una forma de “inyección” molecular de proteína conocida como entrega de ribonucleoproteína (RNP). Cuando la guía coincidía con un ARN objetivo —como un gen marcador fluorescente o mensajes naturales abundantes como GAPDH y el ARN ribosómico 18S— la enzima primero cortaba ese objetivo y luego comenzaba a devorar muchos otros ARN. En unos 50 minutos, el perfil global de ARN de la célula cambiaba drásticamente, con la aparición de fragmentos de corte característicos. Este efecto colateral se observó con distintos métodos de entrega y en una variedad de tipos celulares, lo que indica que no era una rareza de una línea celular o de un objetivo artificial.
Del destrozo de ARN a la muerte celular y la selección
¿Qué le ocurre a una célula cuyos mensajes de ARN desaparecen de repente? Mediante imágenes de células vivas, los investigadores observaron que las células que expresaban el ARN objetivo entraban gradualmente en apoptosis, una forma ordenada de muerte celular programada marcada por señales de “alarma” tempranas antes de que la célula se desintegre. Es importante que las células vecinas que no expresaban el ARN objetivo permanecieron en gran medida sin afectarse, demostrando que la autodestrucción es específica. El grupo explotó luego esta propiedad como herramienta de selección. Al mezclar células portadoras del objetivo con células normales y activar LbuCas13a, las células con el objetivo se vieron selectivamente eliminadas a lo largo de varios días. Repetir el tratamiento varias veces redujo aún más su fracción. Mostraron que esto podía enriquecer células editadas con éxito y que también podía ajustarse para atacar células cancerosas que sobreproducen un oncogén —aquí CDK4— mientras se respetaban células relacionadas que generan mucho menos de ese ARN.
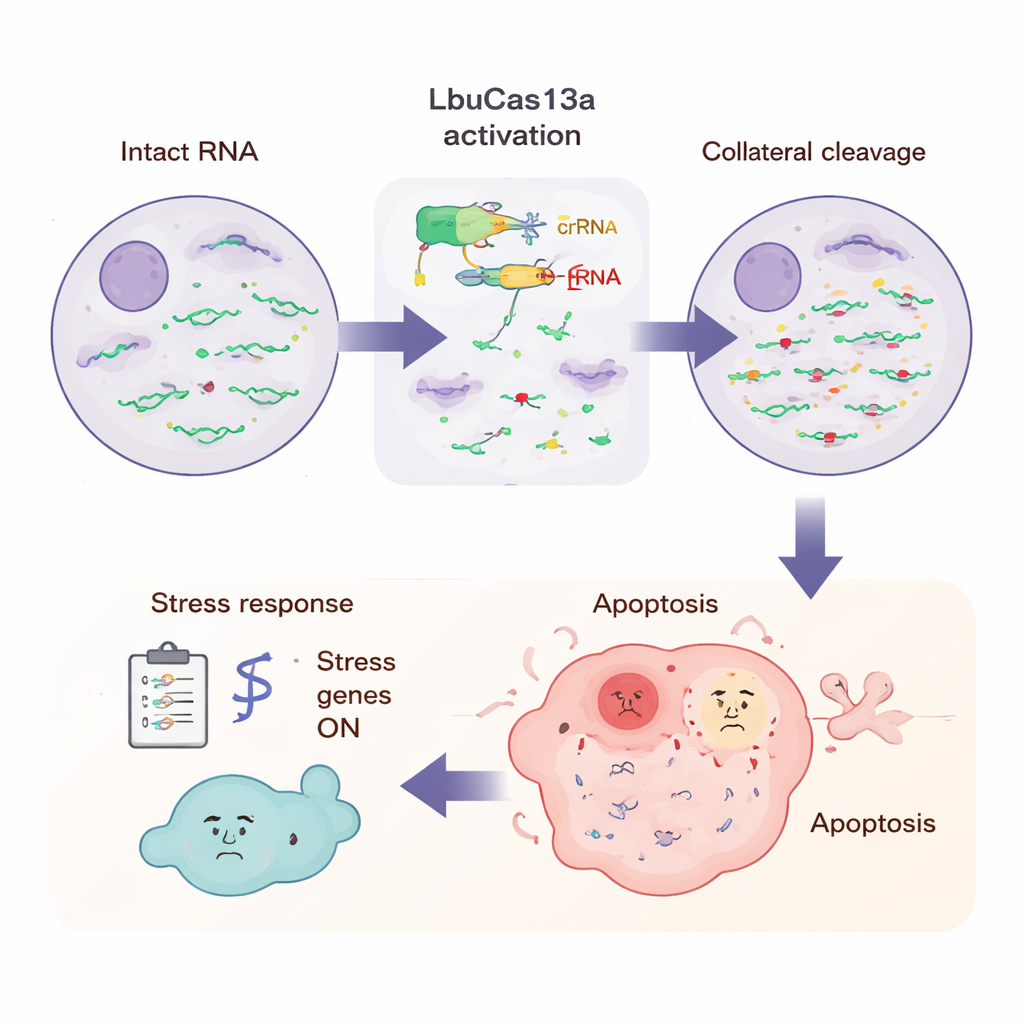
Qué experimenta la célula durante el ataque
Para ver el panorama completo, los científicos midieron todos los ARN de la célula en varios puntos temporales tras la activación de LbuCas13a. Al añadir estándares de ARN conocidos pudieron determinar que la mayoría de los ARN codificantes de proteínas en el citoplasma caían más de la mitad en pocas horas, mientras que ciertos ARN —como los mensajeros mitocondriales y algunos ARN nucleares no codificantes— quedaban en gran medida a salvo. El secuenciamiento de lecturas largas reveló que el corte ocurría en posiciones de nucleótidos repetidas y específicas, a menudo en regiones de lazo flexibles del ARN ricas en la base uracilo, lo que coincide con patrones observados en experimentos in vitro. En puntos temporales posteriores, muchos genes relacionados con el estrés y la respuesta inmunitaria innata se activaron, incluidos los vinculados a señales inflamatorias y defensas antivirales. Este patrón sugiere que la célula detecta el súbito aluvión de extremos de ARN rotos de manera similar a cómo percibe una infección viral, desencadenando un programa de alarma que culmina en apoptosis.
Por qué importa y hacia dónde puede conducir
En términos simples, el estudio muestra que LbuCas13a puede convertirse en un “interruptor de muerte” guiado por ARN: si una célula produce demasiado de un ARN concreto, activar LbuCas13a contra ese ARN provoca una pérdida casi global de ARN, una alarma tipo inmunitaria y, finalmente, muerte celular controlada. Dado que el proceso depende en gran medida de la abundancia del ARN objetivo, podría usarse para eliminar células que sobreexpresan genes dañinos —como ciertas células cancerosas— o para limpiar células no deseadas en cultivos mixtos durante investigación o fabricación de terapias celulares. Al mismo tiempo, el trabajo es una advertencia: las herramientas CRISPR dirigidas al ARN pueden tener efectos secundarios potentes que deben manejarse con cuidado. Comprender cuándo y cómo ocurre la escisión colateral de ARN es fundamental para usar con seguridad las tecnologías Cas13 en medicina y biotecnología.
Cita: Bot, J.F., Zhao, Z., Li, M. et al. Temporal dynamics of collateral RNA cleavage by LbuCas13a in human cells. Commun Biol 9, 233 (2026). https://doi.org/10.1038/s42003-026-09511-3
Palabras clave: CRISPR-Cas13, Escisión de ARN, muerte celular, orientación contra el cáncer, herramientas de edición génica