Clear Sky Science · es
Modulación de las GPCR de clase B1 humanas por los lípidos de la membrana plasmática
Grasas que afinan los receptores de mensajes de nuestras células
Nuestras células dependen de pequeñas antenas proteicas, llamadas receptores, para detectar hormonas y neurotransmisores. Muchos fármacos de éxito actúan dirigiéndose a estos receptores. Este estudio revela que las grasas comunes en la capa externa de nuestras células hacen mucho más que formar un telón de fondo pasivo: se adhieren directamente y moldean toda una familia de receptores clave, orientando de forma sutil cómo se activan o apagan las señales. Comprender esta capa oculta de control podría ayudar a diseñar medicamentos más inteligentes con menos efectos secundarios.
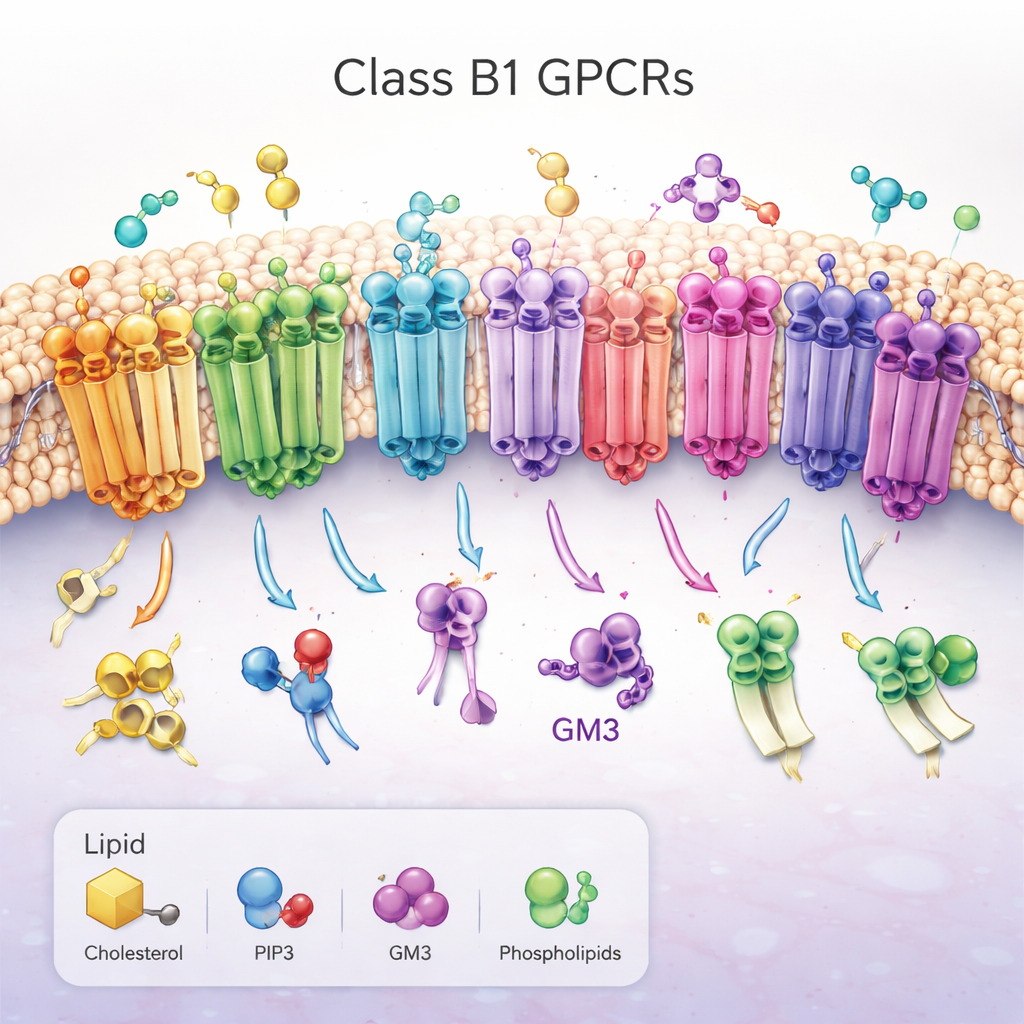
Una familia de importantes antenas moleculares
El trabajo se centra en las receptores acoplados a proteína G (GPCR) de la clase B1, un conjunto de 15 receptores estrechamente relacionados que ayudan a controlar el azúcar en sangre, el metabolismo, el crecimiento y las respuestas al estrés. Están insertados en la membrana externa de la célula, con una gran “cabeza” fuera de la célula que captura moléculas tipo hormona y un haz de siete hélices que atraviesan la membrana lipídica. Cuando se activan, estos receptores cambian de forma en el interior celular, abriendo una hendidura que recluta proteínas asociadas y desencadena cascadas de señalización. Debido a su papel central en enfermedades como la diabetes y la obesidad, las GPCR de clase B1 son objetivos farmacológicos prioritarios, pero sigue siendo en gran medida misterioso cómo los lípidos de la membrana circundante las regulan.
Simular receptores en su entorno natural
En lugar de estudiar los receptores en burbujas detergentes artificiales, los investigadores colocaron las 15 GPCR humanas de clase B1 en membranas construidas por ordenador que imitan la mezcla compleja de grasas de las células reales. Usando una técnica llamada dinámica molecular con representación coarse-grained, realizaron múltiples simulaciones largas de cada receptor tanto en su estado activo como inactivo, sumando aproximadamente un milisegundo de tiempo simulado. Rastrearon cómo tres lípidos “reguladores”—el colesterol, el lípido señalizador PIP2 y la grasa glucosilada GM3—se acercaban, se unían y se desprendían de distintas regiones de cada receptor. Para asegurar que otros puedan reproducir y ampliar este enorme conjunto de datos, capturaron cada paso de la preparación y el análisis usando una herramienta de flujo de trabajo abierta llamada aiida-gromacs, y compararon sus resultados basados en física con predicciones de un nuevo modelo de IA (Chai‑1) que estima cómo las proteínas unen pequeñas moléculas.
Huecos ocultos y una sujeción lipídica conservada
Las simulaciones revelaron patrones de unión recurrentes en toda la familia de receptores. El colesterol, conocido popularmente por su papel en la dieta, se observó alojándose no solo en un sitio previamente conocido en una de las hélices sino también en “bolsillos profundos de membrana” entre hélices, con su cabeza polar enterrada inusualmente lejos dentro de la membrana. Un receptor, el receptor de la secretina, mostró uniones de colesterol especialmente duraderas en bolsillos distintivos en sus formas activa e inactiva, lo que sugiere que el colesterol podría sesgar fuertemente su manera de señalizar. PIP2 mostró un comportamiento notablemente conservado: se agrupó alrededor de la cara interna de los receptores en la unión de dos hélices y un segmento de cola corta (TM6, TM7 y H8), especialmente cuando los receptores estaban en el estado activo. En ese sitio, redes de aminoácidos con carga positiva sujetaban el grupo fosfato negativo de PIP2, lo que sugiere una forma en que este lípido podría estabilizar la conformación activa o ayudar a reclutar proteínas señalizadoras en el interior de la célula.
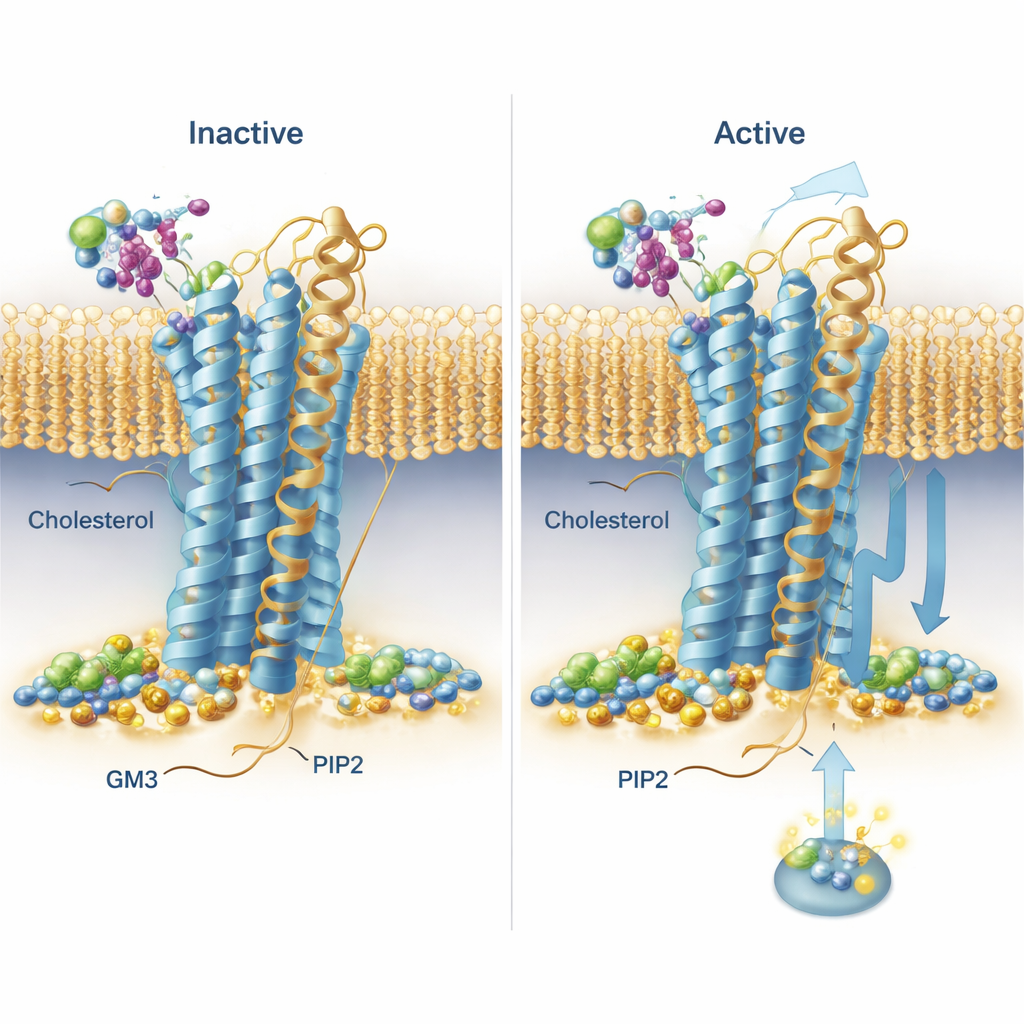
Un lípido recubierto de azúcar que empuja el movimiento del receptor
GM3, un lípido complejo con una cabeza azucarada, interaccionó mayoritariamente con las grandes cabezas externas de los receptores. El equipo observó que los dominios externos de algunos receptores se movían y doblaban mucho respecto a la membrana, mientras que otros eran más rígidos. Para dos receptores relevantes para fármacos—GLP‑1R y GIPR—examinaron en detalle el papel de GM3. En simulaciones con GM3 presente, el lípido se acomodaba bien junto a la base del dominio externo y del bolsillo de unión al ligando (GLP‑1R) o se prendía en la punta más alejada del dominio externo (GIPR), en ambos casos influyendo en la libertad de movimiento de esos dominios. Para poner a prueba estas predicciones en células vivas, los investigadores usaron una técnica basada en luz (TR‑FRET) que informa de la proximidad entre una cabeza de receptor marcada y la membrana. Cuando redujeron los niveles de GM3 con un inhibidor de pequeña molécula, observaron cambios medibles en cómo se desplazaban las cabezas del receptor tras la estimulación, coherentes, en términos generales, con la idea de que GM3 modula la flexibilidad del receptor de forma específica según el receptor y su estado.
Por qué importan estas asociaciones lípido–receptor
En conjunto, el estudio dibuja una imagen de las GPCR de clase B1 no solo como interruptores hormonales sino como partes de una danza estrechamente coreografiada con los lípidos circundantes. El colesterol puede ocupar bolsillos ocultos y favorecer sutilmente ciertos resultados de señalización, PIP2 forma una “asa” interna conservada que puede bloquear los receptores en su forma activa y guiar a las proteínas asociadas, y GM3 ajusta cómo se mueven las regiones externas de los receptores y cómo encuentran a sus ligandos. Para los no especialistas, el mensaje clave es que la membrana es una capa reguladora activa: pequeñas diferencias en la composición lipídica podrían cambiar cómo se comporta el mismo receptor en distintos tejidos o estados de enfermedad. Al mapear estas interacciones en detalle y compartir los datos de simulación subyacentes, este trabajo sienta las bases para diseñar futuros fármacos que exploten u eviten contactos lipídicos específicos, lo que podría hacer los tratamientos más selectivos y eficaces.
Cita: Chao, K.W., Wong, L., Oqua, A.I. et al. Human class B1 GPCR modulation by plasma membrane lipids. Commun Biol 9, 317 (2026). https://doi.org/10.1038/s42003-025-09445-2
Palabras clave: Receptores acoplados a proteína G, lípidos de membrana, colesterol, PIP2, GM3