Clear Sky Science · es
Perspectivas estructurales sobre el transporte de metacúmulos en el andamio de ensamblaje de la nitrogenasa NifEN
Cómo la naturaleza construye una herramienta química potente
El nitrógeno está a nuestro alrededor en el aire, pero la mayoría de los seres vivos no puede utilizarlo en esa forma. Una enzima especial llamada nitrogenasa resuelve este problema al convertir el nitrógeno atmosférico en amoníaco, un ingrediente clave para la vida y para los fertilizantes. En el corazón de la nitrogenasa se encuentra un denso “clúster” metálico que realiza la química exigente, pero cómo ensamblan las células esta pieza intrincada ha sido hasta ahora poco claro. Este artículo examina ese proceso constructivo, revelando cómo una proteína andamio llamada NifEN actúa como muelle de carga flexible y sistema de transporte para la carga metálica del clúster.
Una fábrica molecular detrás de fertilizantes y combustibles
La nitrogenasa es la contraparte natural de los procesos industriales que producen amoníaco y combustibles líquidos. En lugar de reactores gigantes, los microbios usan una máquina proteica compacta impulsada por la energía celular. Su rendimiento depende de un centro metálico singularmente complejo, construido a partir de hierro, azufre, molibdeno, carbono y un grupo lateral orgánico. El ensamblaje de este núcleo es demasiado delicado para dejarse al azar, por lo que las células emplean un equipo de proteínas auxiliares en relevo. Una de las más importantes es NifEN, que recibe un precursor casi terminado compuesto solo por hierro (llamado L‑clúster), ayuda a convertirlo en la forma madura (el M‑clúster) y luego se lo entrega a la enzima nitrogenasa activa. Comprender cómo NifEN gestiona este tráfico podría orientar esfuerzos para diseñar microbios que produzcan fertilizantes más limpios o nuevos combustibles basados en carbono.
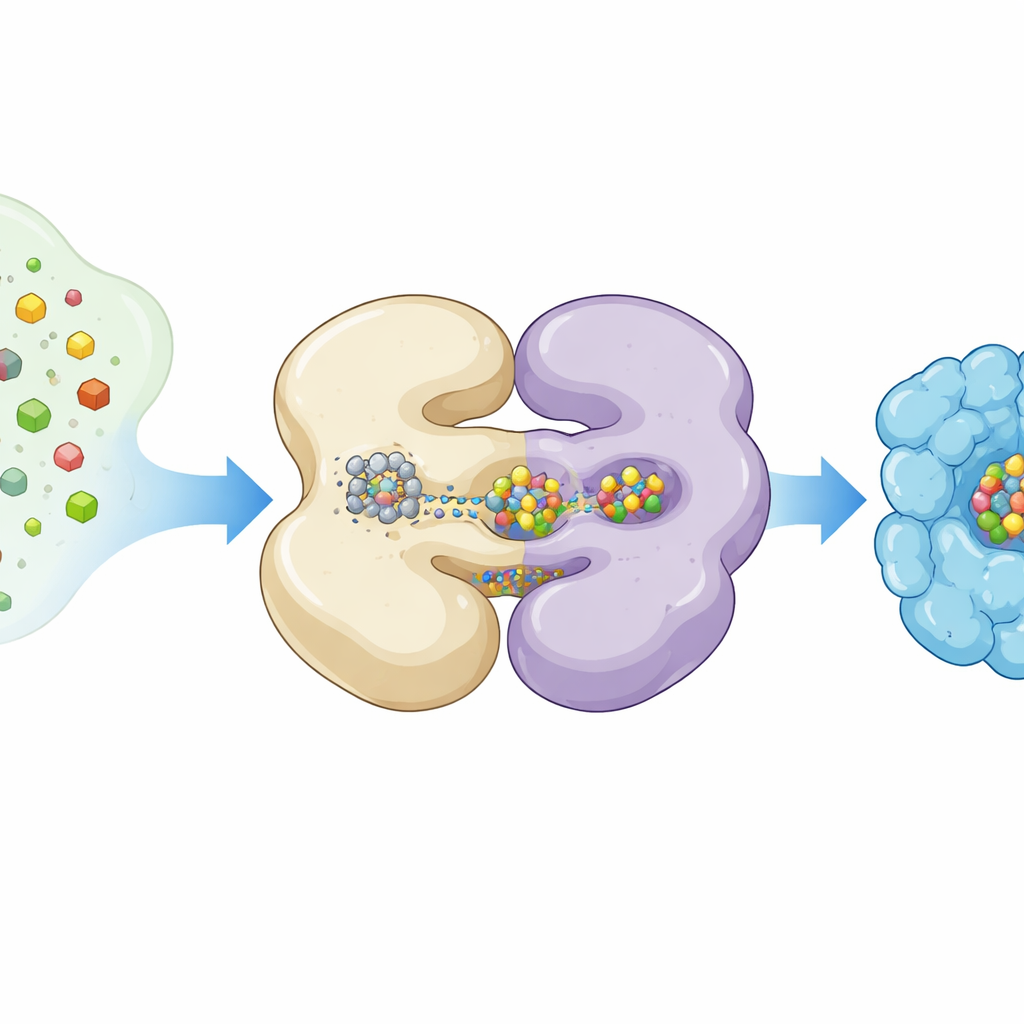
Ver una máquina en movimiento con instantáneas congeladas
Los autores utilizaron crio microscopía electrónica, una técnica que imagen proteínas a temperaturas extremadamente bajas, para capturar a NifEN en diferentes posturas funcionales. Expresaron NifEN en bacterias de laboratorio de modo que algunas copias de la proteína llevaran un L‑clúster y otras estuvieran vacías. Al ordenar millones de imágenes de partículas individuales, reconstruyeron dos formas principales: una forma “apo” carente del clúster móvil y una forma “holo” con el clúster unido en un sitio interno. Ambas formas comparten un núcleo formado por cuatro subunidades dispuestas en dos pares, pero cuando el L‑clúster está presente, una mitad de NifEN se vuelve notablemente más ordenada y varias hélices se pliegan hacia el interior, ajustándose alrededor de la carga metálica.
Un túnel oculto para la carga metálica
Comparar las estructuras vacía y cargada reveló una característica llamativa: un túnel largo que atraviesa el dímero de NifEN. En el estado vacío, este pasaje está ancho y abierto; después de la unión del clúster se estrecha a medida que la proteína sujeta a su pasajero. Estructuras cristalinas anteriores habían mostrado una posición alternativa “exterior” para el L‑clúster cerca de la superficie proteica. Al combinar todas las vistas, los investigadores dedujeron que el clúster puede ocupar al menos dos estaciones en NifEN—una enterrada en el interior y otra expuesta—y desplazarse entre ellas a lo largo de una trayectoria curva regulada por desplazamientos en un dominio flexible. Este movimiento parece ser más relajado que en la enzima nitrogenasa final, cuyo clúster activo se mantiene rigidamente en su lugar, lo que sugiere que NifEN está diseñado para la entrega más que para la catálisis a largo plazo.
Sitios de acoplamiento y una ruta continua
Para entender cómo NifEN se conecta con sus socios aguas arriba y aguas abajo, el equipo combinó sus estructuras experimentales con modelos computacionales de AlphaFold 3 y microscopía electrónica de menor resolución de complejos proteicos. Los modelos sugieren que la enzima NifB, que fabrica el L‑clúster a partir de piezas más pequeñas de hierro‑azufre, se acopla en un valle en una cara de NifEN. Allí, puede trazarse un túnel continuo desde los propios centros metálicos de NifB directamente hacia el túnel de NifEN y hasta la estación interna del L‑clúster. En la cara opuesta de NifEN, un sitio de acoplamiento diferente acoge a NifH, la proteína que inserta el molibdeno y un grupo lateral orgánico para completar el cofactor. En esta configuración, el L‑clúster se sitúa en el sitio superficial, idealmente posicionado para su modificación. Mutar aminoácidos clave que recubren la ruta propuesta altera la carga, el movimiento o la maduración del clúster, lo que aporta apoyo experimental a este modelo de cinta transportadora.
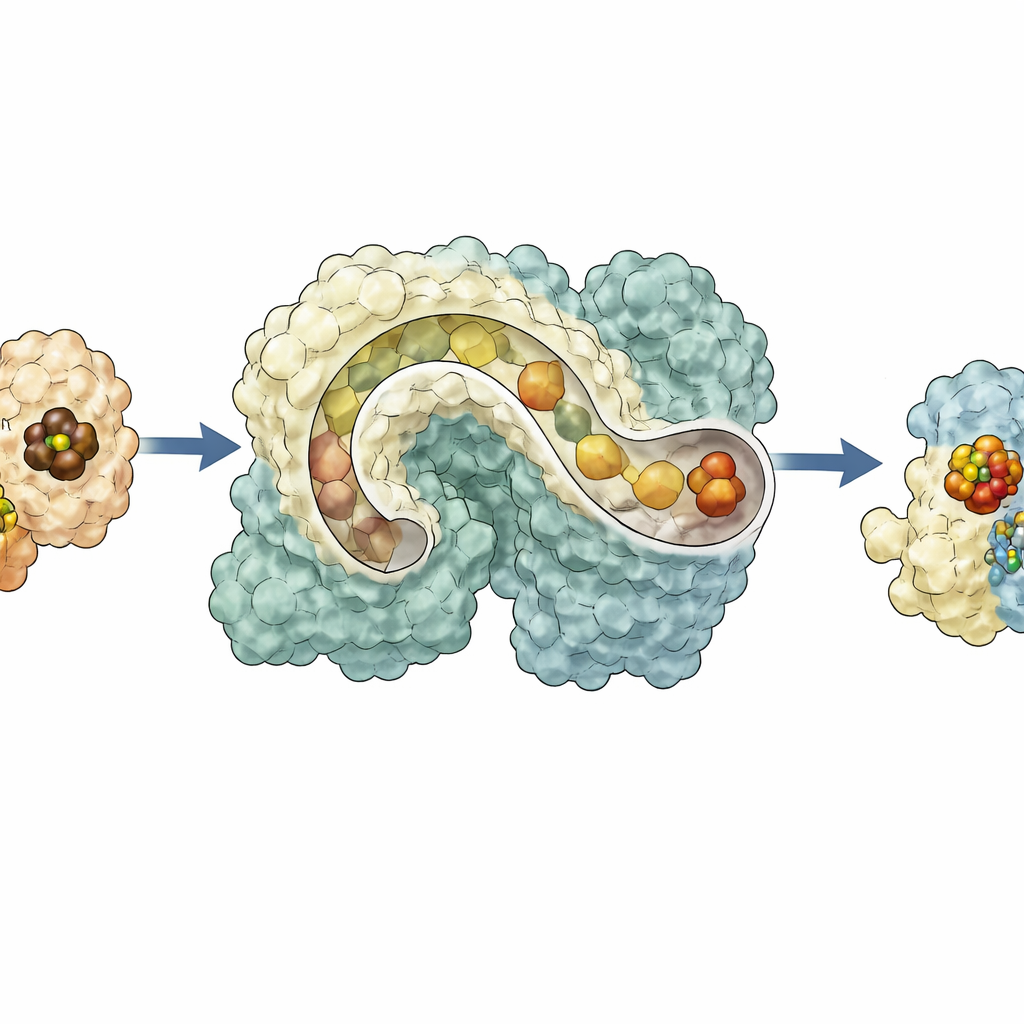
Por qué importa un andamio flexible
En conjunto, los resultados dibujan a NifEN como un centro dinámico que recibe un núcleo metálico de NifB por un lado, lo desplaza a una bahía interior de almacenamiento, luego lo presenta en la superficie opuesta para que NifH lo termine antes de guiar el clúster maduro de vuelta al interior para su entrega a la nitrogenasa. Este esquema de tráfico gobernado por conformaciones explica cómo múltiples pasos delicados pueden coordinarse dentro de un único marco proteico y sugiere cómo enzimas antiguas podrían haber evolucionado desde andamios más flexibles hasta los catalizadores altamente especializados de hoy. Para el público general, el trabajo muestra que incluso a escala nanométrica la naturaleza recurre a líneas de montaje, túneles y piezas móviles para construir las herramientas moleculares que sostienen los ciclos globales del nitrógeno, la producción de alimentos y, potencialmente, futuras tecnologías verdes.
Cita: Neumann, B., Brandon, K.A., Quechol, R. et al. Structural insights into metallocluster trafficking in the nitrogenase assembly scaffold NifEN. Nat Catal 9, 281–294 (2026). https://doi.org/10.1038/s41929-026-01489-9
Palabras clave: nitrogenasa, ensamblaje de metacúmulos, andamio NifEN, crio microscopía electrónica, fijación biológica del nitrógeno