Clear Sky Science · es
Combinar aprendizaje federado y modelo itinerante mejora el rendimiento y abre oportunidades para la equidad digital en salud
Por qué importa compartir conocimientos médicos sin compartir datos
La medicina moderna depende cada vez más de la inteligencia artificial para detectar patrones en exploraciones y registros de salud. Pero los datos de los pacientes son sensibles y, con frecuencia, no pueden salir del hospital donde se recogieron. Esto crea una tensión: ¿cómo pueden colaborar hospitales de todo el mundo para entrenar potentes herramientas de IA sin enviar datos de pacientes en bruto a través de fronteras o a grandes servidores centrales? Este estudio presenta una nueva forma de hacerlo, con el objetivo no solo de lograr precisión, sino también de promover la equidad entre hospitales bien dotados y clínicas más pequeñas y con menos recursos.
Dos maneras de entrenar una IA sin mover los datos
Hoy existen dos estrategias principales que permiten a los hospitales entrenar IA conjuntamente manteniendo los datos localmente. En el aprendizaje federado, cada hospital entrena su propia copia local de un modelo en paralelo; esos modelos locales se combinan luego en un modelo “global” compartido en un servidor central. En el enfoque de modelo itinerante, hay un único modelo que se desplaza de hospital en hospital, entrenándose en cada centro por turno. Ambos métodos protegen la privacidad, pero cada uno tiene inconvenientes. El aprendizaje federado puede tener dificultades cuando algunos hospitales disponen de muy pocos datos o no ven todos los tipos de pacientes; combinar modelos locales débiles o desequilibrados puede dar lugar a un modelo global pobre que refleje principalmente a los centros grandes y acomodados. El modelo itinerante es más robusto frente a esos desequilibrios pero puede ser más lento y más difícil de gestionar.
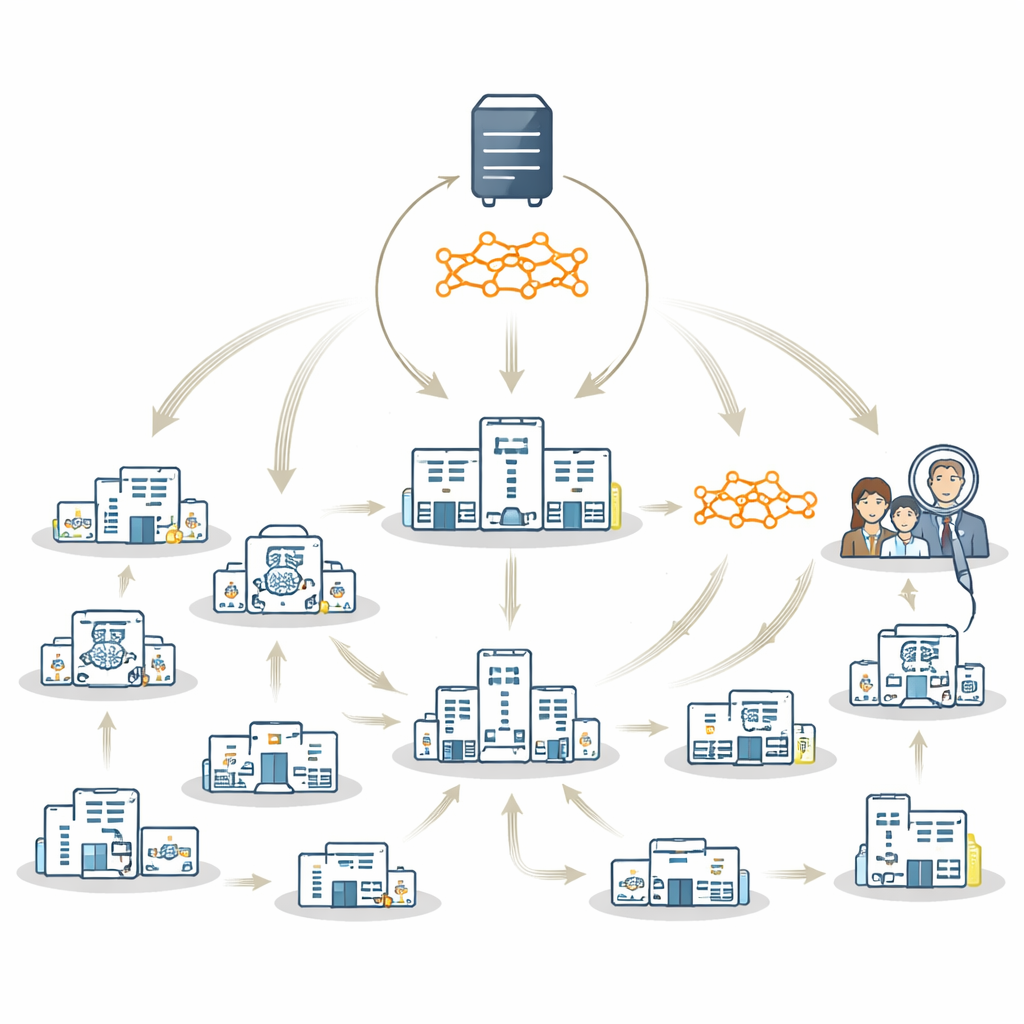
Una estrategia híbrida que aprovecha lo mejor de ambos mundos
Los autores proponen FedTM, un esquema híbrido de entrenamiento que combina las fortalezas del aprendizaje federado y del modelo itinerante. El entrenamiento se realiza en dos fases. Primero viene una fase de “calentamiento” en la que solo los hospitales más grandes, con conjuntos de datos más completos y equilibrados, entrenan el modelo en paralelo usando técnicas estándar de aprendizaje federado. Esto crea un modelo inicial potente. Luego llega una fase de “refinamiento”, en la que ese modelo precalentado visita todos los centros por secuencia, incluidas clínicas muy pequeñas que pueden tener solo unas pocas resonancias cerebrales o incluso un único paciente. En esta segunda fase, el modelo se actualiza gradualmente a medida que viaja, incorporando el conocimiento de cada sitio sin necesidad de que sus datos abandonen el control local.
Probar el método con resonancias cerebrales de la enfermedad de Parkinson
Para poner a prueba FedTM, los investigadores usaron 1.817 resonancias magnéticas cerebrales procedentes de 83 centros de imagen a nivel mundial para entrenar un sistema de IA que distinguiera a personas con enfermedad de Parkinson de individuos sanos. Se trata de un escenario particularmente desafiante: más de la mitad de los centros aportaron menos de diez exploraciones, solo alrededor de un tercio disponía de datos tanto de pacientes como de controles sanos, y los protocolos de adquisición variaban ampliamente. En estas condiciones del mundo real, el aprendizaje federado puro no logró aprender bien la tarea, mientras que un modelo itinerante puro rindió mejor pero aún dejaba margen de mejora. FedTM, especialmente cuando el calentamiento involucró a los siete centros más grandes y equilibrados, superó claramente a ambos: el área bajo la curva ROC, una medida estándar de la calidad de clasificación, aumentó del 77% con el modelo itinerante solo a aproximadamente el 82% con FedTM, con ganancias similares en otras métricas clínicamente relevantes como sensibilidad, especificidad y F1.
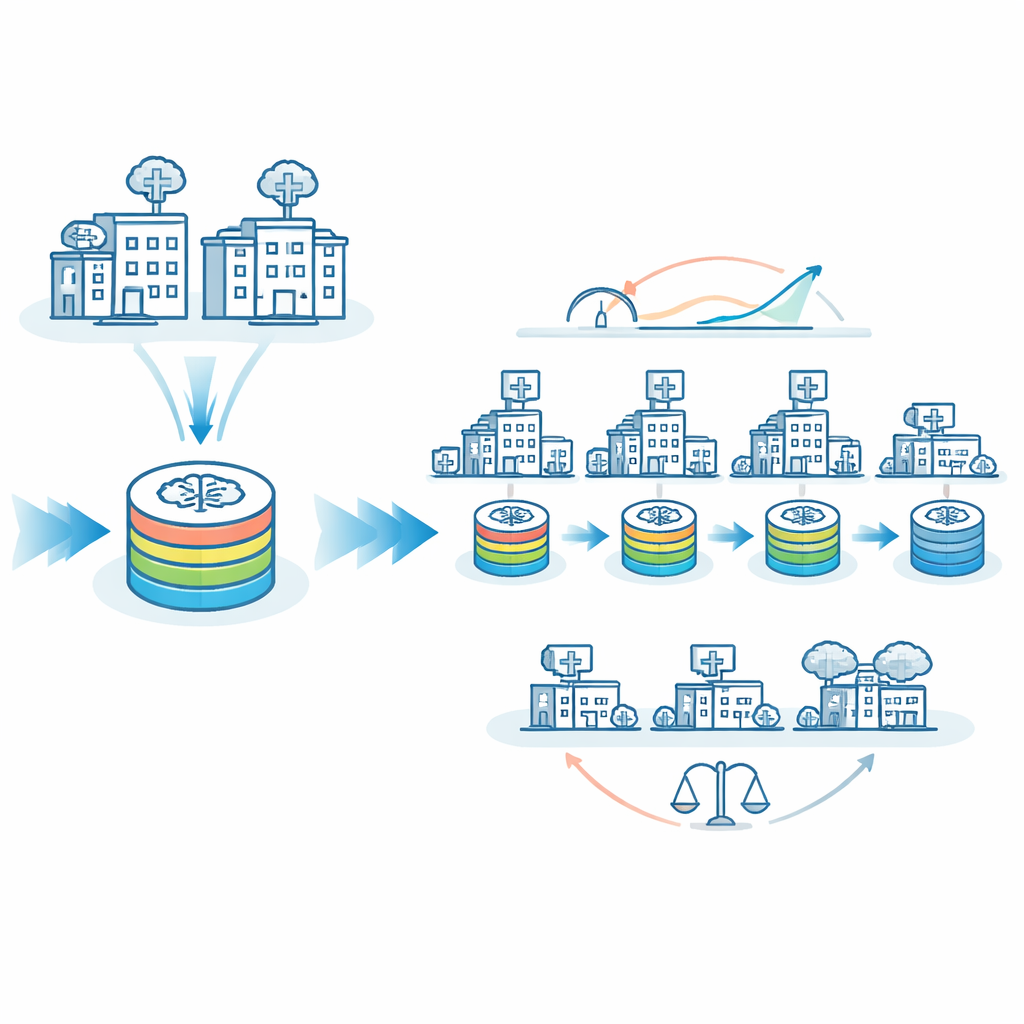
Hacer la IA más justa entre hospitales grandes y pequeños
Una preocupación importante en la IA médica es la equidad: ¿funciona un modelo igual de bien para pacientes de hospitales pequeños, rurales o con pocos recursos que para los de grandes centros académicos? El equipo examinó con qué frecuencia la IA cometía predicciones erróneas en sitios “más grandes” frente a “más pequeños”. Con el modelo itinerante solo, las tasas de clasificación errónea diferían en aproximadamente 8 puntos porcentuales entre estos grupos. Con FedTM ajustado adecuadamente, las tasas de clasificación errónea para los sitios grandes y pequeños se volvieron casi idénticas, alrededor del 26%. En otras palabras, el modelo no solo mejoró la precisión global, sino que también se volvió más imparcial. FedTM también trasladó la mayor parte del cómputo pesado a la fase de calentamiento en los sitios mejor dotados, reduciendo casi a la mitad el número de ciclos de entrenamiento que los sitios pequeños tuvieron que ejecutar, mientras mantenía el tiempo total de entrenamiento similar.
Qué significa esto para la salud digital global
FedTM ofrece una vía práctica hacia herramientas de IA que respetan la privacidad, mejoran el rendimiento y comparten beneficios de forma más equitativa en todo el mundo. Al permitir que incluso los centros con muy pocos datos influyan en el modelo final, este marco puede ayudar a garantizar que las personas en entornos remotos o con pocos recursos no se queden atrás cuando se desarrollen nuevas herramientas diagnósticas. Aunque el estudio se centró en un tipo de exploración cerebral y en una enfermedad concreta, el enfoque puede, en principio, adaptarse a muchos otros problemas médicos. A medida que los sistemas de salud adopten cada vez más dispositivos móviles y wearables, y que las regulaciones enfatizan la soberanía de los datos, las estrategias híbridas como FedTM podrían convertirse en clave para construir una IA médica confiable, inclusiva y responsable.
Cita: Souza, R., Stanley, E.A.M., Ohara, E.Y. et al. Combining federated learning and travelling model boosts performance and opens opportunities for digital health equity. npj Digit. Med. 9, 294 (2026). https://doi.org/10.1038/s41746-026-02483-y
Palabras clave: aprendizaje federado, modelo itinerante, enfermedad de Parkinson, IA en imagen médica, equidad en salud