Clear Sky Science · es
Descodificando el eje inmunorregulador ERS–CAF mediante IA multimodal y su valor pronóstico y predictivo terapéutico pan‑cáncer
Ver los tumores sin bisturí
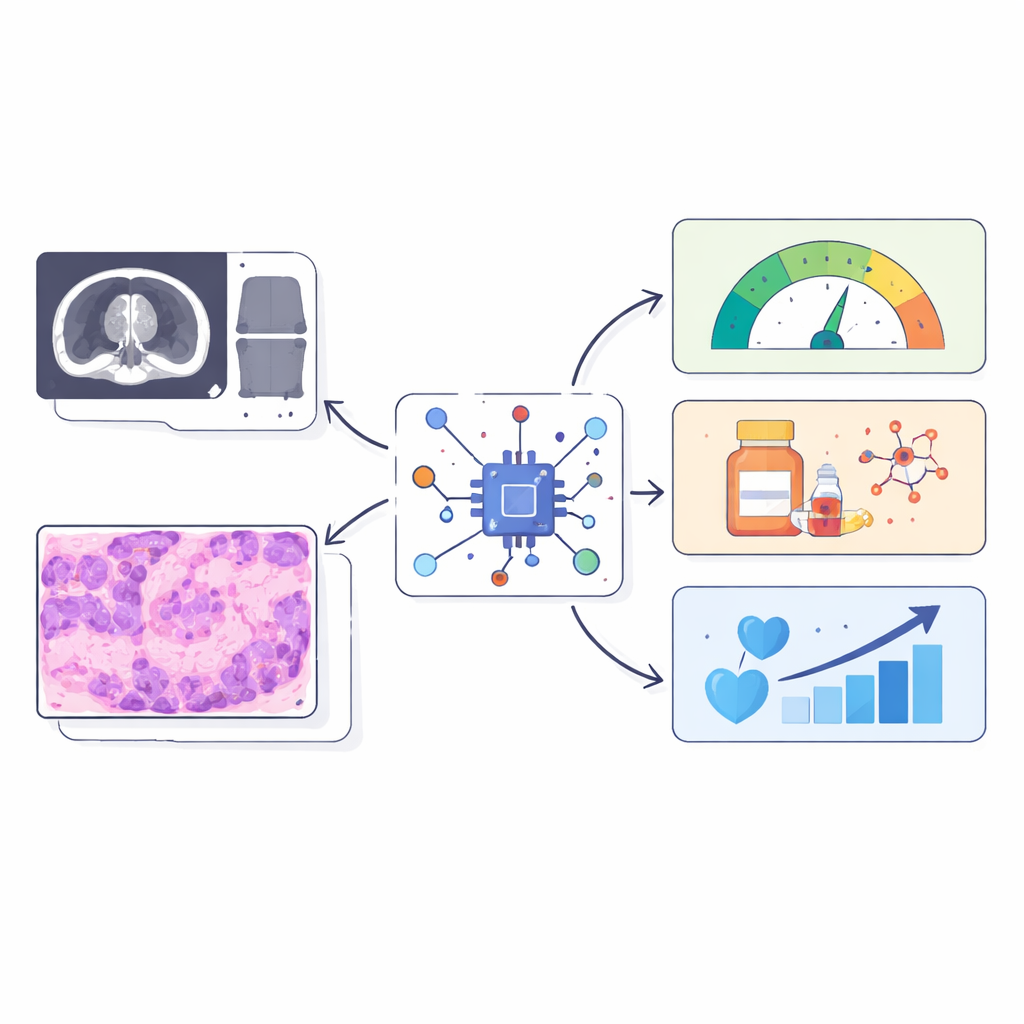
Los oncólogos reconocen cada vez más que lo que rodea a un tumor puede importar tanto como el propio tumor. Pero muestrear repetidamente este vecindario oculto con biopsias es invasivo y a menudo poco práctico. Este estudio muestra cómo la inteligencia artificial (IA) puede leer exploraciones médicas de rutina y imágenes de microscopio para inferir procesos inmunitarios y cicatriciales difíciles de medir dentro de los tumores, convirtiendo potencialmente la imagenología cotidiana en una especie de “biopsia digital” aplicable a distintos cánceres.
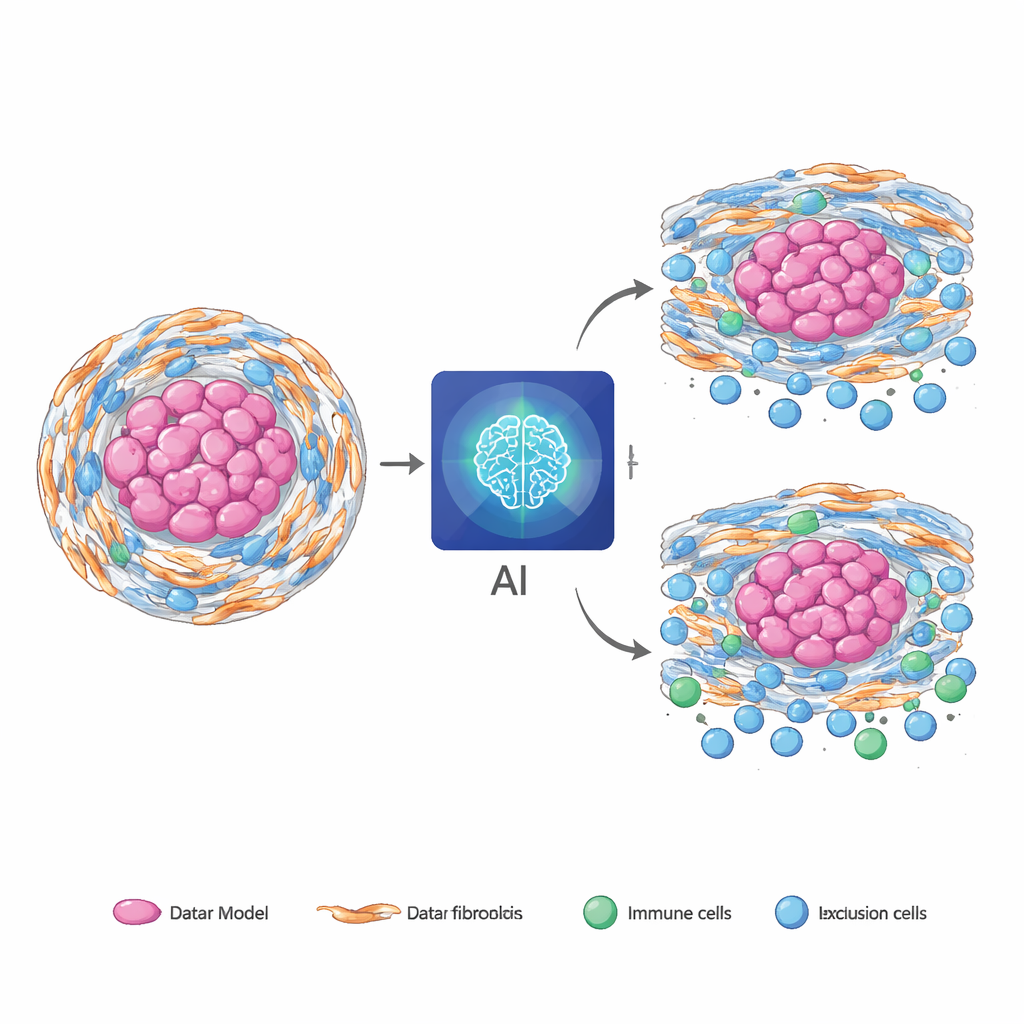
Las células de soporte ocultas que moldean el cáncer
Muchos tumores sólidos están envueltos en una capa resistente y fibrótica creada por células de soporte especializadas llamadas fibroblastos. Cuando estas células sufren estrés dentro de la fábrica de proteínas celular (el retículo endoplásmico), adoptan un estado agresivo que ayuda al cáncer. En el cordoma, un cáncer óseo raro, estos fibroblastos estresados forman una matriz densa y contribuyen a mantener fuera a las células inmunitarias, haciendo que los tratamientos sean menos efectivos. Entornos similares, fibróticos y pobres en células inmunitarias, aparecen en otros cánceres como los pancreáticos y colorrectales, lo que sugiere que esta biología no es exclusiva de una sola enfermedad. El problema es que las formas actuales de medir estos fibroblastos estresados y su comportamiento de bloqueo inmunitario dependen de muestras de tejido y pruebas moleculares complejas, que son difíciles de repetir y pueden pasar por alto regiones importantes del tumor.
Enseñar a la IA a ver biología invisible
Los investigadores se preguntaron si las resonancias magnéticas estándar previas a la cirugía y las láminas patológicas rutinarias teñidas con H&E ya contenían pistas visuales sobre esta barrera inmunitaria formada por fibroblastos estresados. Crearon tres “puntuaciones de referencia” numéricas a partir de la secuenciación de ARN tumoral: una que captura cuán activo está el programa de estrés en los fibroblastos, otra que resume cuánto parecen estas células señalizar a las células inmunitarias y una tercera que describe la diversidad de las poblaciones inmunes y de soporte circundantes. En lugar de predecir miles de genes, su IA se entrenó para predecir solo estas tres puntuaciones biológicamente significativas a partir de las imágenes. Para ello, el equipo combinó dos ramas: una que analiza texturas y formas en la RM y otra que explora miles de pequeñas regiones en la lámina digital y usa un mecanismo de atención guiado por lenguaje para centrarse en áreas que coinciden con descripciones de expertos sobre tejido fibrótico y pobre en inmunidad.
Fusionar exploraciones y láminas para señales más fuertes
En 126 pacientes con cordoma con RM, láminas patológicas, datos de ARN y seguimiento emparejados, el modelo de IA fusionado superó a los modelos que usaban solo RM o solo láminas. Sus predicciones de las tres puntuaciones moleculares concordaron estrechamente con las medidas basadas en ARN y se mantuvieron bien calibradas entre distintos hospitales y escáneres. Cuando los patólogos marcaron de forma independiente regiones fibróticas y excluyentes de inmunidad, los “puntos calientes” de la IA tendieron a activarse en esas mismas áreas, lo que sugiere que estaba rastreando biología auténtica y no solo el tamaño del tumor. El modelo también captó prognóstico: puntuaciones más altas predichas de estrés‑fibroblasto y de señalización se asociaron con peor supervivencia, mientras que una mayor diversidad microambiental predicha ofreció una protección parcial. Añadir estas puntuaciones derivadas por IA a factores clínicos de rutina mejoró la capacidad de separar a pacientes de alto y bajo riesgo a lo largo del tiempo.
De tumores raros a cánceres comunes
Una prueba clave fue si un modelo entrenado íntegramente en cordoma podía usarse “tal cual” en otros cánceres más comunes. Aplicado sin reentrenamiento a tumores pancreáticos, gástricos y colorrectales de grandes conjuntos de datos públicos, la versión basada solo en láminas del modelo mostró aún una alineación significativa entre sus predicciones por imagen y las puntuaciones recién calculadas a partir de ARN. En algunos de estos cánceres, las puntuaciones de la IA mejoraron la predicción de la supervivencia del paciente más allá de la información clínica estándar y ayudaron a distinguir qué pacientes tenían más probabilidades de beneficiarse de la quimioterapia. Para facilitar el despliegue donde la patología digital es limitada, el equipo destiló el modelo multimodal completo en una versión solo RM que conservó la mayor parte del poder predictivo mientras funcionaba más rápido y con menos recursos computacionales.
Qué podría significar esto para los pacientes
En conjunto, los resultados respaldan la idea de que las imágenes médicas de rutina codifican de forma discreta información sobre células de soporte estresadas, exclusión inmunitaria y diversidad del microambiente —rasgos que normalmente requieren pruebas moleculares costosas. Aunque el trabajo actual es retrospectivo y necesita validación prospectiva, apunta hacia un futuro en el que una exploración y una lámina estándar pueden señalar de forma no invasiva tumores con una barrera inmunitaria fibrótica hostil, guiar qué pacientes podrían beneficiarse de pruebas adicionales o terapias personalizadas, y hacerlo en múltiples tipos de cáncer sin carga adicional para los pacientes.
Cita: Zheng, BW., Xia, C., Tang, M. et al. Decoding the ERS–CAF immunoregulatory axis via multimodal AI and its pan-cancer prognostic and therapeutic predictive value. npj Digit. Med. 9, 199 (2026). https://doi.org/10.1038/s41746-026-02388-w
Palabras clave: microambiente tumoral, imagenología del cáncer, inteligencia artificial, fibroblastos, inmunoterapia