Clear Sky Science · es
Toma de decisiones algorítmica sobre antibióticos en infección del tracto urinario mediante predicción, informada por el prescriptor, de la utilidad del tratamiento
Antibióticos más inteligentes para infecciones comunes
Las infecciones del tracto urinario (ITU) son una de las razones más frecuentes por las que se prescriben antibióticos. Elegir el fármaco adecuado es, sin embargo, un acto de equilibrio: los médicos deben curar la infección, evitar efectos adversos serios y proteger a la sociedad del empeoramiento de la resistencia a los antibióticos. Este estudio presenta un nuevo tipo de algoritmo de toma de decisiones que pretende apoyar a los clínicos combinando datos hospitalarios a gran escala con las prioridades reales de los médicos, ayudando a seleccionar antibióticos que sean eficaces para el paciente y más seguros para la comunidad en general.
El problema de los fármacos potentes
La medicina moderna depende de los antibióticos, pero el uso excesivo de fármacos de amplio espectro, los llamados “armas grandes”, está impulsando una crisis mundial de resistencia antimicrobiana. Las Naciones Unidas han fijado un objetivo: para 2030, el 70 % del uso de antibióticos en todo el mundo debería corresponder a medicamentos más estrechos y de primera línea conocidos por la Organización Mundial de la Salud como antibióticos de la categoría “Access”. En la práctica, muchos clínicos se inclinan por fármacos más amplios, etiquetados como “Watch” o “Reserve”, porque temen que una opción más estrecha pueda fracasar frente a bacterias resistentes, especialmente cuando los pacientes están muy graves. Como resultado, a menudo cambiamos riesgos de resistencia a largo plazo por tranquilidad a corto plazo, sin herramientas claras para juzgar cuándo un fármaco más seguro y estrecho funcionaría igual de bien.
Enseñar a un algoritmo a pensar como un clínico
Los investigadores desarrollaron un algoritmo de decisión sobre antibióticos centrado en ITU usando historiales electrónicos detallados de casi 94 000 pacientes hospitalizados en Boston. Primero entrenaron modelos predictivos para estimar, para 13 antibióticos distintos, la probabilidad de que las bacterias causantes de la ITU fueran susceptibles y la probabilidad de que el tratamiento desencadenara problemas como infección por Clostridioides difficile o toxicidad farmacológica grave. A continuación, pidieron a 49 clínicos del Reino Unido, de varias especialidades, que completaran un ejercicio de clasificación en línea, eligiendo entre antibióticos ficticios que diferían en características como riesgo de efectos secundarios, idoneidad para ITU, coste, si eran fármacos Access o Watch/Reserve, y si se administraban por vía oral o intravenosa. Analizando estas clasificaciones, el equipo cuantificó cuánto valoraban los médicos cada característica—por ejemplo, cuánto preferían fármacos orales, con baja toxicidad y orientados a ITU frente a opciones más arriesgadas o más potentes.
Añadir una red de seguridad para pacientes muy graves
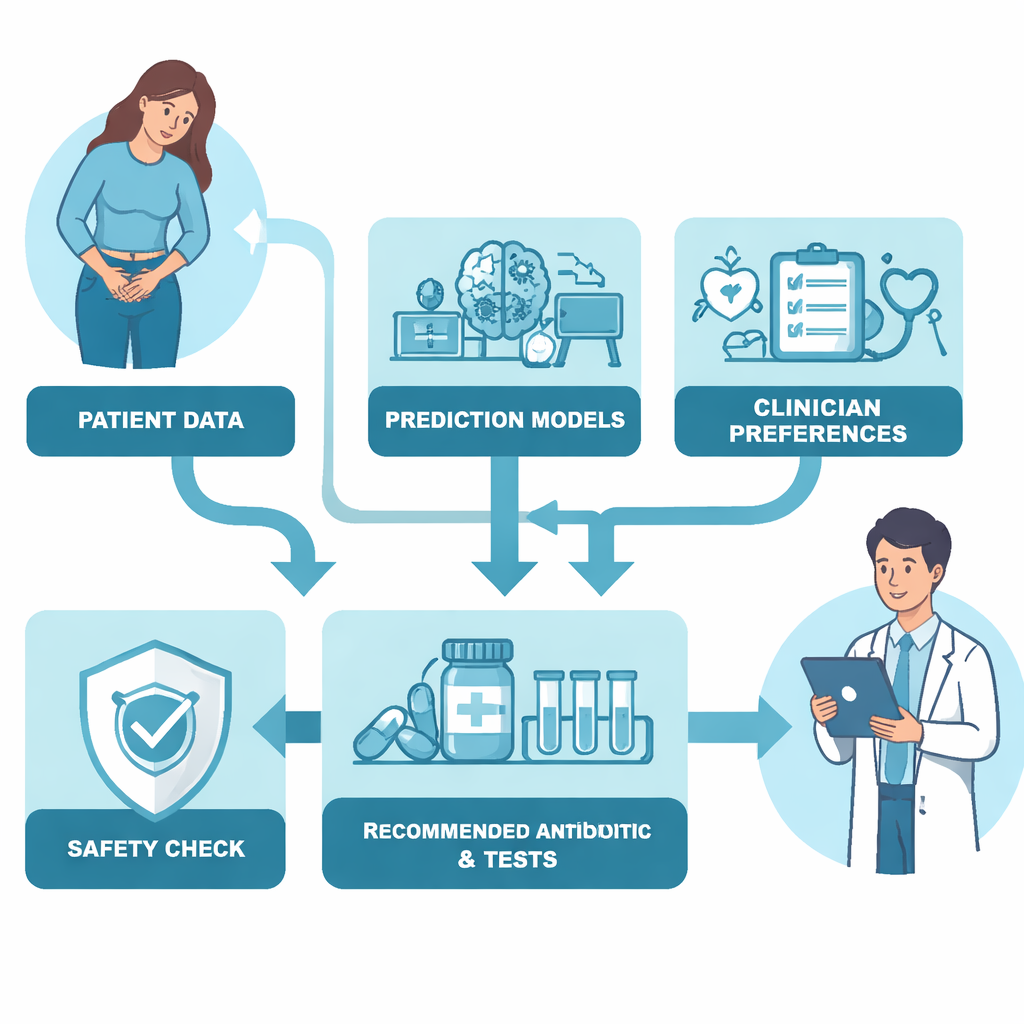
El algoritmo final combinó estos dos ingredientes: predicciones basadas en datos y juicios de valor de los clínicos. Para cada paciente calculó un “valor de tratamiento” para cada antibiótico, teniendo en cuenta la probabilidad predicha de que el fármaco funcionara, las probabilidades de efectos secundarios graves, su categoría Access/Watch/Reserve y si era oral o intravenoso. De forma crucial, el algoritmo incluyó también un mecanismo de seguridad basado en el estado de gravedad con el que el paciente se presentaba en urgencias. A medida que aumentaba la gravedad de la enfermedad, el algoritmo daba automáticamente más peso a atacar la infección con fuerza y a disponer de una opción intravenosa. En otras palabras, para pacientes con enfermedad leve intentaba favorecer fármacos estrechos y orales, pero a medida que los pacientes se agravaban, se mostraba progresivamente más dispuesto a usar antibióticos más potentes e intravenosos para protegerlos frente al fallo del tratamiento.
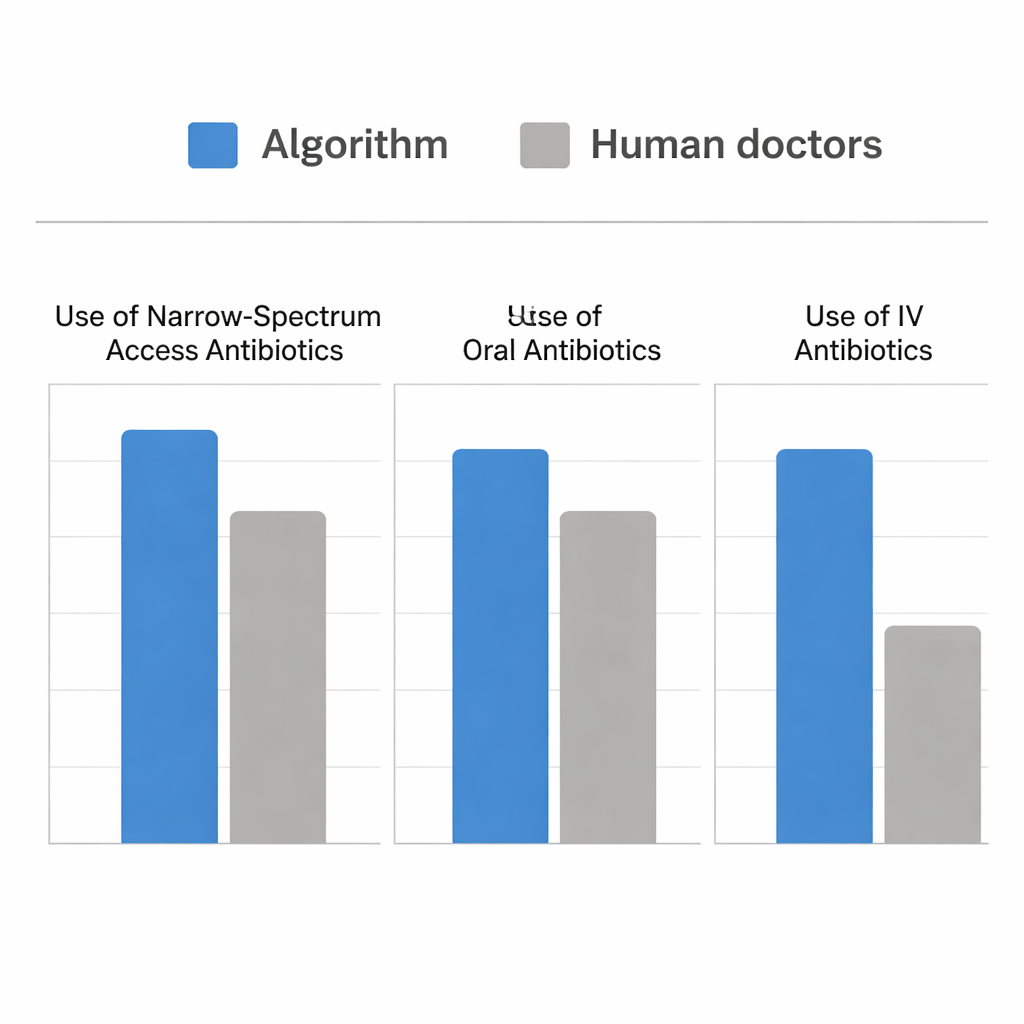
Cómo se comparó el algoritmo con los médicos
El equipo ejecutó luego una simulación con casos reales de urgencias en los que los pacientes tenían ITU y cultivos de orina. Compararon los antibióticos que los clínicos humanos habían administrado con los fármacos que el algoritmo habría elegido en el momento en que se envió el cultivo. Ambos enfoques fueron igualmente buenos para escoger un antibiótico que cubriera la bacteria del paciente. Sin embargo, el algoritmo lo consiguió eligiendo muchos más fármacos de espectro estrecho de la categoría Access y muchas más opciones orales, y usando menos antibióticos intravenosos. Para los pacientes más graves, el algoritmo se comportó como los prescriptores humanos, desplazándose de forma apropiada hacia fármacos intravenosos y más potentes. Donde difirió fue en reconocer oportunidades adicionales—especialmente en pacientes moderadamente enfermos—para tratar de forma segura con fármacos orales de la categoría Access, como nitrofurantoína y ampicilina-sulbactam, en lugar de recurrir por defecto a opciones más amplias.
Qué significa esto para la atención cotidiana
Para un lector no especializado, el mensaje clave es que este sistema no sustituye a los médicos; actúa más bien como una calculadora para los complejos balances riesgo–beneficio que los clínicos ya tienen en cuenta pero no pueden calcular con precisión en su cabeza. Al casar las prioridades de los propios clínicos con la evidencia a gran escala sobre el rendimiento de los antibióticos, el algoritmo puede sugerir tratamientos que son igual de eficaces para pacientes individuales pero más respetuosos con el organismo y con la salud pública—favoreciendo pastillas sobre sueros cuando sea seguro, y fármacos más estrechos sobre los de último recurso siempre que sea posible. Si se valida en más entornos, este tipo de herramientas podría ayudar a hospitales y sistemas de salud a acercarse a los objetivos globales de uso responsable de antibióticos, sin sacrificar la seguridad de las personas que llegan críticamente enfermas por infección.
Cita: Howard, A., Green, P.L., Zhong, Y. et al. Algorithmic antibiotic decision-making in urinary tract infection using prescriber-informed prediction of treatment utility. npj Digit. Med. 9, 136 (2026). https://doi.org/10.1038/s41746-026-02369-z
Palabras clave: infección del tracto urinario, gestión de antibióticos, soporte a la decisión clínica, resistencia a los antimicrobianos, aprendizaje automático en medicina