Clear Sky Science · es
Integración de multi-ómicas y aprendizaje automático descifra sistemáticamente la heterogeneidad celular y las redes regulatorias fibróticas en la progresión de MASLD a MASH
Por qué importa esta investigación sobre el hígado
La enfermedad hepática grasa asociada a la obesidad y a la diabetes tipo 2 es hoy uno de los problemas hepáticos más comunes en el mundo. Para muchas personas la afección permanece leve, pero en una proporción considerable progresa silenciosamente hacia una forma agresiva con inflamación y cicatrización que puede conducir a cirrosis y cáncer de hígado. Los médicos aún tienen dificultades para predecir quién progresará y para detectar esta etapa peligrosa de forma temprana sin una biopsia. Este estudio emplea herramientas avanzadas de “multi-ómicas” y la inteligencia artificial para observar células hepáticas individuales, revelando un tipo de célula inmunitaria y una vía de señalización recién reconocidos que parecen impulsar la cicatrización nociva, y propone marcadores en sangre que podrían algún día identificar a pacientes de alto riesgo de forma no invasiva.

Del simple depósito de grasa al daño hepático peligroso
Los investigadores se centraron en la transición de la enfermedad hepática esteatósica asociada a disfunción metabólica (MASLD), frecuentemente llamada hígado graso, a su pariente más grave, la esteatohepatitis asociada a disfunción metabólica (MASH). MASLD es extremadamente común, afectando a más de un tercio de los adultos a nivel mundial, especialmente a quienes tienen obesidad o diabetes. La mayoría de las personas con MASLD tienen depósitos de grasa en el hígado pero poco daño. En la MASH, sin embargo, las células hepáticas se lesionan, aumenta la inflamación y se forma tejido cicatricial. Aproximadamente entre una de cada cinco y una de cada tres personas con MASH desarrollarán eventualmente cirrosis o cáncer de hígado. Las pruebas de sangre y las exploraciones actuales no pueden identificar con precisión qué cambios celulares microscópicos están ocurriendo dentro del órgano, por lo que a menudo se pierde la ventana para una intervención temprana.
Mirar el hígado una célula a la vez
Para abordar este problema, el equipo combinó varios tipos de datos potentes procedentes de estudios públicos. Reunieron datos de secuenciación de ARN a nivel de célula única de más de medio millón de células hepáticas individuales, transcriptómica espacial que conserva la localización de esas células en el tejido, perfiles de actividad génica a granel de biopsias completas y mapas de accesibilidad de la cromatina que muestran qué tramos de ADN están abiertos y activos. Con software sofisticado, agruparon las células en siete tipos amplios, incluyendo células hepáticas, células inmunitarias y células de sostén llamadas células estrelladas hepáticas. A continuación compararon hígados sanos, MASLD y MASH en estadios temprano y avanzado, y cartografiaron cómo cambiaba la mezcla celular y sus redes de comunicación a medida que la enfermedad empeoraba.
Células inmunitarias y de sostén que impulsan la cicatrización trabajando en conjunto
Surgió un patrón llamativo: las células inmunitarias conocidas como monocitos y macrófagos, junto con las células estrelladas hepáticas, eran mucho más abundantes en MASH que en etapas anteriores, y tendían a agruparse en las mismas regiones del tejido enfermo. Al profundizar, los científicos subdividieron las células estrelladas en cinco subtipos que van desde formas en reposo hasta formas totalmente activadas y semejantes al músculo liso. A medida que los hígados pasaban de MASLD a MASH, las células estrelladas en reposo disminuyeron y aumentaron las células estrelladas activadas productoras de cicatrices, trazando una trayectoria clara desde un estado de reposo hacia un estado fibrótico. Los análisis espaciales mostraron que estas células estrelladas activadas se ubicaban cerca de los macrófagos enriquecidos, lo que sugiere una asociación íntima en la formación de las cicatrices hepáticas.
Un tipo de macrófago recién destacado y un eje de señalización fibrótico
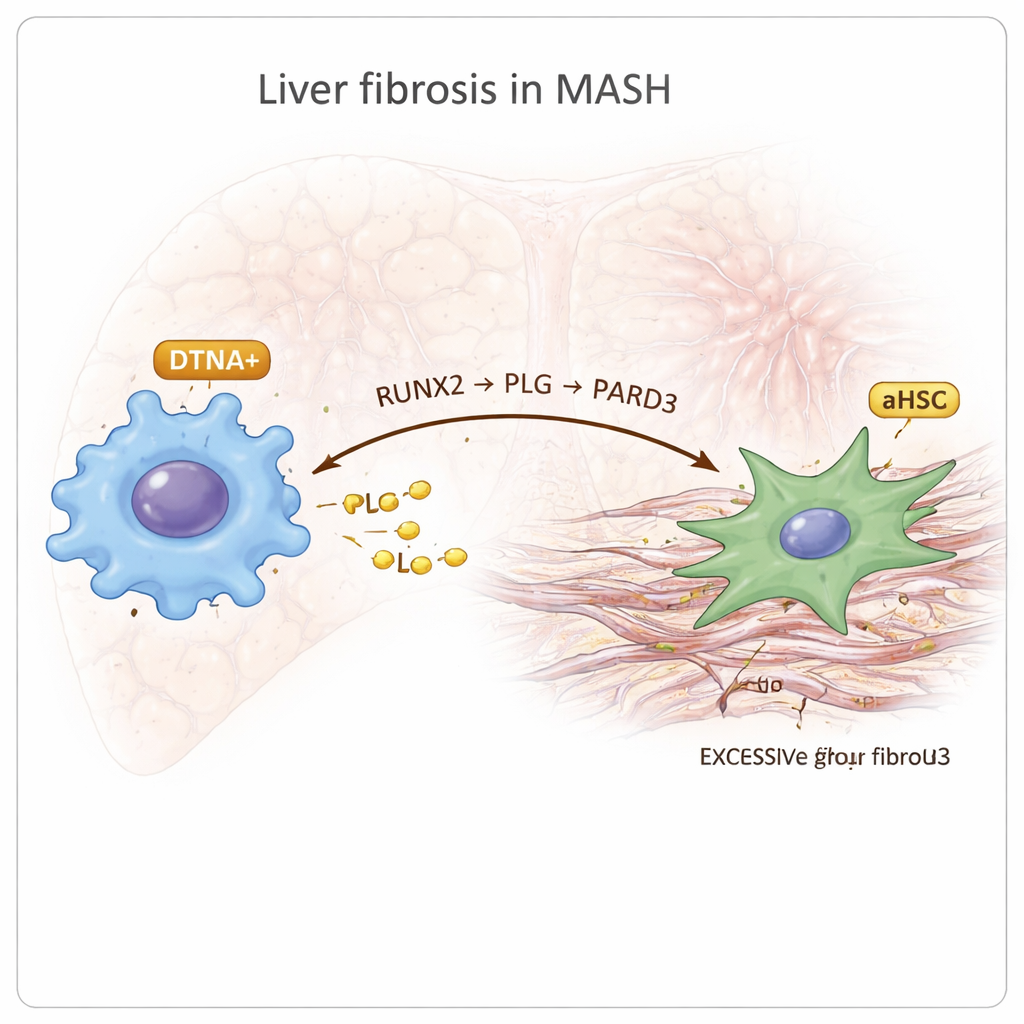
Entre las células inmunitarias, los investigadores identificaron un subgrupo distintivo de macrófagos marcado por un gen llamado DTNA que estaba específicamente enriquecido en MASH. Estos macrófagos DTNA-positivos mostraron rasgos de la llamada polarización M2, que a menudo se asocia con inflamación crónica y remodelado tisular, junto con signos de hipoxia y señalización inflamatoria intensa. Reconstruyendo “trayectorias” de desarrollo, infirieron que estas células se originan a partir de las células residentes Kupffer en el hígado. El análisis de redes regulatorias señaló a un factor de transcripción llamado RUNX2 como un interruptor maestro en estos macrófagos. Un mapeo adicional de la comunicación célula–célula sugirió que los macrófagos DTNA-positivos se comunican con las células estrelladas activadas mediante una cadena que denominan eje RUNX2–PLG–PARD3: RUNX2 aumenta la producción de la proteína PLG en los macrófagos, PLG luego señaliza a las células estrelladas que expresan PARD3, y esta interacción se vincula con una fibrosis más intensa y una actividad alterada de la coagulación sanguínea.
De los mapas celulares a posibles pruebas y tratamientos
Para evaluar si estos descubrimientos podrían ayudar a los pacientes, el equipo entrenó y probó 113 modelos diferentes de aprendizaje automático sobre grandes conjuntos de datos de expresión génica a granel de personas con MASLD o MASH. Un modelo Elastic Net fue el que mejor desempeño obtuvo, y en múltiples cohortes independientes un gen destacó como el predictor más potente: DTNA. Una mayor actividad de DTNA y de sus genes asociados, incluido RUNX2, marcó de forma consistente a los pacientes con MASH frente al hígado graso simple. Los autores también exploraron bases de datos de fármacos existentes y encontraron varios medicamentos que podrían actuar sobre la recientemente descrita vía RUNX2–PLG–PARD3, lo que apunta a oportunidades de reposicionamiento, si bien estas ideas aún requieren pruebas en laboratorio y ensayos clínicos.
Qué significa esto para las personas con enfermedad del hígado graso
En términos cotidianos, este estudio muestra que no todas las células inmunitarias y de sostén del hígado son iguales, y que una asociación particular entre un subtipo de macrófago recién destacado y las células estrelladas formadoras de cicatrices puede ser un motor clave que impulsa el hígado graso hacia una cicatrización peligrosa. El trabajo sugiere que medir marcadores como DTNA en sangre o tejido podría algún día ayudar a los médicos a identificar qué pacientes con hígado graso tienen mayor riesgo de progresar a MASH, sin depender únicamente de biopsias invasivas. También pone el foco en una ruta de señalización específica, el eje RUNX2–PLG–PARD3, como un objetivo prometedor para fármacos destinados a frenar o revertir la fibrosis hepática. Aunque estos hallazgos aún están en la fase de investigación y necesitan validación adicional, proporcionan una hoja de ruta más clara para convertir datos celulares complejos en herramientas prácticas para el diagnóstico temprano y tratamientos dirigidos.
Cita: Wen, W., Liu, Z., Tan, W. et al. Integrating multi-omics and machine learning systematically deciphers cellular heterogeneity and fibrotic regulatory networks in the progression from MASLD to MASH. npj Digit. Med. 9, 167 (2026). https://doi.org/10.1038/s41746-026-02352-8
Palabras clave: enfermedad del hígado graso, MASH, macrófagos, fibrosis hepática, multi-ómicas