Clear Sky Science · es
Autoenmascaramiento, preentrenamiento generalizable e “expertos” integrados para mejorar la segmentación de gliomas
Por qué importan exploraciones más inteligentes para los tumores cerebrales
Los tumores cerebrales llamados gliomas están entre los cánceres más letales, y sin embargo los médicos siguen dedicando mucho tiempo a trazar manualmente los bordes tumorales en las resonancias magnéticas. Ese contorneado guía la cirugía y la radioterapia, pero puede llevar entre 15 y 20 minutos por paciente y debe repetirse con el tiempo. El estudio presenta MAGPIE, un sistema de inteligencia artificial que aprende de decenas de miles de exploraciones cerebrales sin etiquetas humanas y que luego necesita apenas unos pocos casos etiquetados por expertos para mapear los gliomas de forma fiable. Para los pacientes, esto podría traducirse en una planificación del tratamiento más rápida y consistente, incluso en hospitales que no disponen de grandes conjuntos de datos curados.
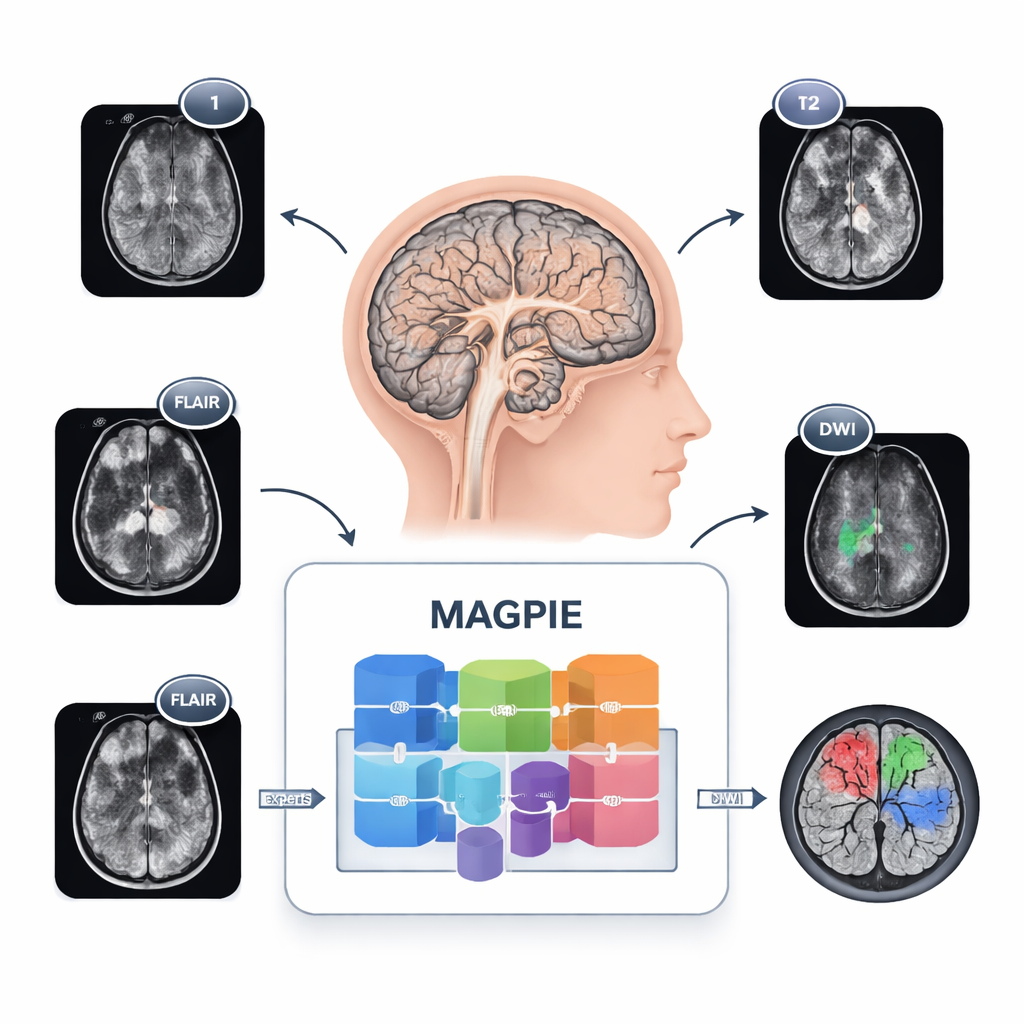
Ver los tumores de una manera nueva
Los gliomas son difíciles de mapear porque no forman esferas nítidas. Las células cancerosas se diseminan a lo largo de las conexiones cerebrales, creando márgenes difusos y pequeñas lesiones satélite que son difíciles de ver. Además, distintos hospitales usan ajustes de resonancia magnética y combinaciones de secuencias diferentes, por lo que una herramienta entrenada en un lugar puede fallar en otro. MAGPIE afronta todo esto a la vez. Se expuso primero a 43.505 exploraciones cerebrales no etiquetadas procedentes de muchos estudios y tipos de escáner. Durante esa fase, aprendió patrones generales de tejido cerebral sano y enfermo intentando reconstruir partes faltantes de las imágenes y comparando distintas vistas aumentadas del mismo cerebro, obligándolo a centrarse en rasgos estables y significativos en lugar de en detalles frágiles de píxeles.
Permitir que varios expertos compartan el trabajo
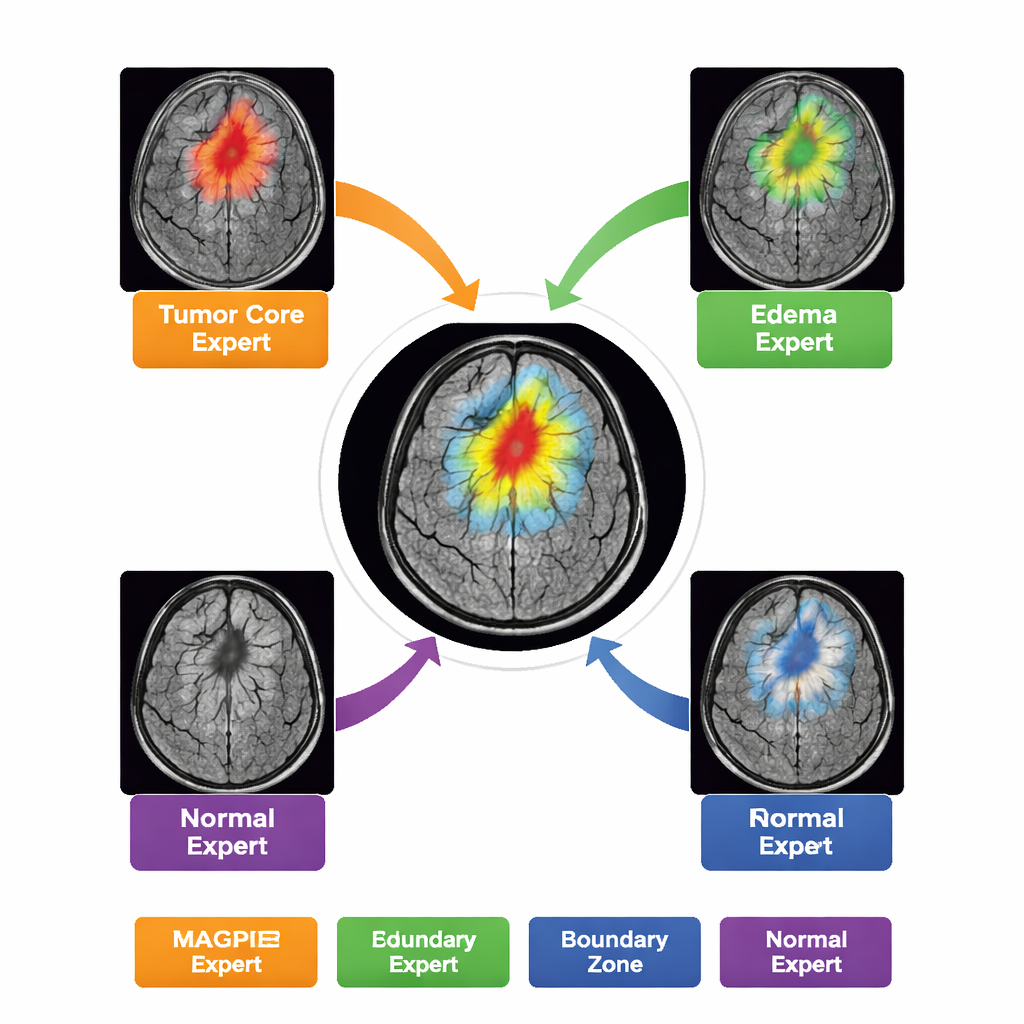
En lugar de actuar como un modelo monolítico único, MAGPIE contiene una “mezcla de expertos” en su interior. Cuando analiza una exploración nueva, solo activa un pequeño subconjunto de ocho subredes especializadas para cada región de la imagen. Durante el entrenamiento, esos expertos se dividen la tarea de forma natural: unos se vuelven sensibles al anillo brillante y activo de crecimiento tumoral; otros se centran en el núcleo necrótico; otros aprenden el halo difuso de edema alrededor del tumor; y algunos se ocupan principalmente del fondo cerebral y los límites normales. Los autores demuestran esto midiendo en qué medida la actividad de cada experto se solapa con las distintas zonas tumorales marcadas por los radiólogos. Esta división del trabajo mejora la precisión manteniendo la computación manejable: solo alrededor de la mitad de los parámetros del modelo están activos para cualquier parche dado.
Manejar exploraciones del mundo real y desordenadas
Los protocolos clínicos de RM no son uniformes. Algunos pacientes tienen cuatro secuencias, otros menos; las máquinas de distintos fabricantes producen imágenes con sutiles diferencias. El diseño de MAGPIE trata cada secuencia de RM como un “token” separado y aprende sobre la marcha cuánto peso otorgar a cada una, en lugar de esperar un conjunto fijo de entradas en un orden fijo. Este enfoque agnóstico respecto al canal permite que el sistema se adapte si, por ejemplo, falta una secuencia con contraste pero está presente FLAIR. El modelo también utiliza mecanismos de atención avanzados que le permiten tanto “ver lejos”, capturando la diseminación a larga distancia a lo largo de los tractos de materia blanca, como “ver con precisión”, detectando lesiones muy pequeñas de apenas unos milímetros.
Hacer más con muchas menos etiquetas
Tras el preentrenamiento, los investigadores afinaron MAGPIE con solo 20 casos de glioma completamente etiquetados y lo compararon con modelos estándar entrenados desde cero en las mismas condiciones. En un importante benchmark de tumores cerebrales (BraTS21), MAGPIE alcanzó una puntuación Dice —una medida de solapamiento común en imagen médica— de aproximadamente 61 %, superando a la mejor versión entrenada desde cero por unos 2,6 puntos porcentuales y rindiendo mejor que un método auto-supervisado anterior potente sin mostrar un “transfer negativo” perjudicial. En datos desafiantes fuera de la distribución —exploraciones de distintas enfermedades, tipos de escáner y ajustes de imagen— también se mantuvo mejor, alcanzando más del 70 % de Dice en un conjunto de lesiones de la materia blanca sin ajuste adicional. Crucialmente, este nivel de rendimiento normalmente exige del orden de 400 casos etiquetados; MAGPIE lo logra con solo cerca del 5 % de ese esfuerzo.
Qué podría significar esto para pacientes y clínicas
Para quienes no son expertos, el mensaje central es que MAGPIE convierte una montaña de exploraciones de RM sin etiquetar en un asistente potente que necesita muy poco entrenamiento experto para ser clínicamente útil. Puede delinear tumores cerebrales complejos con límites realistas, detectar pequeñas lesiones satélite que otros sistemas pasan por alto y seguir funcionando de forma fiable cuando las exploraciones proceden de máquinas desconocidas o carecen de ciertas secuencias. Esa combinación podría reducir el tiempo de anotación de los radiólogos en alrededor de un 95 %, bajar la barrera para que hospitales más pequeños desplieguen IA avanzada en imagen y apoyar una planificación más precisa de cirugía y radioterapia. Aunque sigue siendo necesaria más validación en tipos tumorales raros y en casos de bajo grado, este estudio demuestra cómo un diseño cuidadoso del aprendizaje auto-supervisado puede acercar la segmentación robusta y eficiente de tumores cerebrales a la práctica clínica cotidiana.
Cita: Xie, M., Xiao, Q., Wu, H. et al. Masked autoencoding, generalizable pretraining, and integrated experts for enhanced glioma segmentation. npj Digit. Med. 9, 163 (2026). https://doi.org/10.1038/s41746-026-02347-5
Palabras clave: segmentación de gliomas, resonancia magnética cerebral, aprendizaje auto-supervisado, mezcla de expertos, IA en imagen médica