Clear Sky Science · es
¿Modelos guiados clínicamente o modelos de base? predicción de la mielopatía cervical espondilótica a partir de registros electrónicos de salud
Por qué importa detectar este problema espinal antes
La mielopatía cervical espondilótica (MCE) es un término largo, pero para muchos adultos mayores representa una amenaza silenciosa para la médula espinal. Puede empezar con torpeza, una marcha arrastrada o problemas para ir al baño y, de forma gradual, progresar hasta una discapacidad grave o incluso la parálisis. Los médicos a menudo la pasan por alto durante años porque los signos son sutiles y se parecen a problemas más comunes como la artrosis o el síndrome del túnel carpiano. Este estudio plantea una cuestión oportuna: ¿pueden los patrones ocultos en los registros electrónicos de salud ayudar a identificar a personas en riesgo de MCE años antes del diagnóstico formal, y qué tipo de inteligencia artificial (IA) es la más adecuada para esa tarea?
Una enfermedad oculta en una población que envejece
La MCE se produce cuando el desgaste relacionado con la edad estrecha el canal espinal en el cuello y comprime la médula espinal. La afección es habitual en adultos mayores; las pruebas de imagen cervical muestran compresión medular en aproximadamente un tercio de las personas mayores de 60 años, y una parte sustancial de ellas desarrollará síntomas. Sin embargo, los estudios indican que los pacientes suelen esperar entre dos y seis años entre los primeros signos y un diagnóstico correcto, perdiendo tiempo valioso en el que la cirugía u otras intervenciones podrían prevenir un daño permanente. A medida que las poblaciones envejecen y los clínicos de atención primaria lidian con consultas sobrecargadas y una exposición limitada a los trastornos de la columna, crece la necesidad de métodos escalables para detectar la MCE de forma temprana.
Convertir los registros médicos en un sistema de alerta temprana
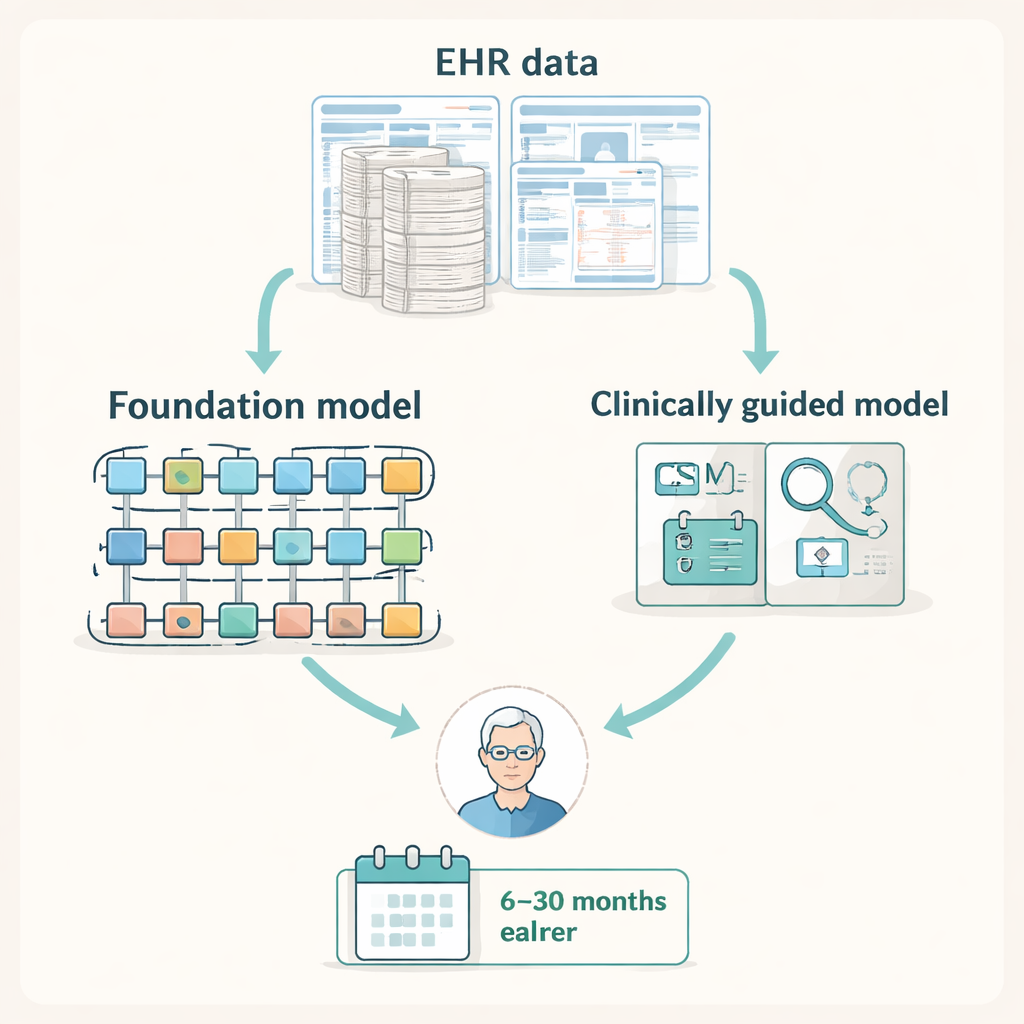
Los registros electrónicos de salud (EHR) modernos capturan una traza detallada de diagnósticos, pruebas de laboratorio, procedimientos y visitas clínicas. Los investigadores razonaron que esa traza probablemente contiene pistas sobre la MCE temprana —como caídas repetidas, pruebas neurofisiológicas o fisioterapia— mucho antes de que alguien solicite imágenes especializadas de la columna. Reunieron datos de aproximadamente 2 millones de pacientes en dos grandes conjuntos de datos de EE. UU.: una base nacional de reclamaciones de seguros y los registros de un sistema de salud regional. Dentro de estos, identificaron decenas de miles de personas que finalmente recibieron un diagnóstico de MCE y las emparejaron con pacientes similares que no lo hicieron, creando un banco de pruebas a gran escala para ver si la IA podía predecir quién recibiría más adelante un diagnóstico de MCE en ventanas temporales de 6 a 30 meses de antelación.
IA general de gran tamaño frente a herramientas ligeras guiadas clínicamente
El equipo comparó varios tipos de modelos de aprendizaje automático que procesan datos de EHR. En un extremo estaban los grandes “modelos de base”: sistemas potentes basados en transformadores entrenados originalmente con millones de registros de pacientes para aprender patrones generales en datos sanitarios. En el otro extremo estaban modelos más pequeños construidos únicamente a partir de una lista concisa de 497 códigos de diagnóstico, procedimiento y medicamentos seleccionados a mano por especialistas en columna como altamente relevantes para la MCE. Los investigadores midieron el rendimiento usando estadísticas adecuadas para enfermedades raras, preguntando cuánto mejor era cada modelo que el azar al identificar a pacientes que más tarde desarrollarían MCE en diferentes ventanas de predicción.
Precisión local, fiabilidad al trasladarse
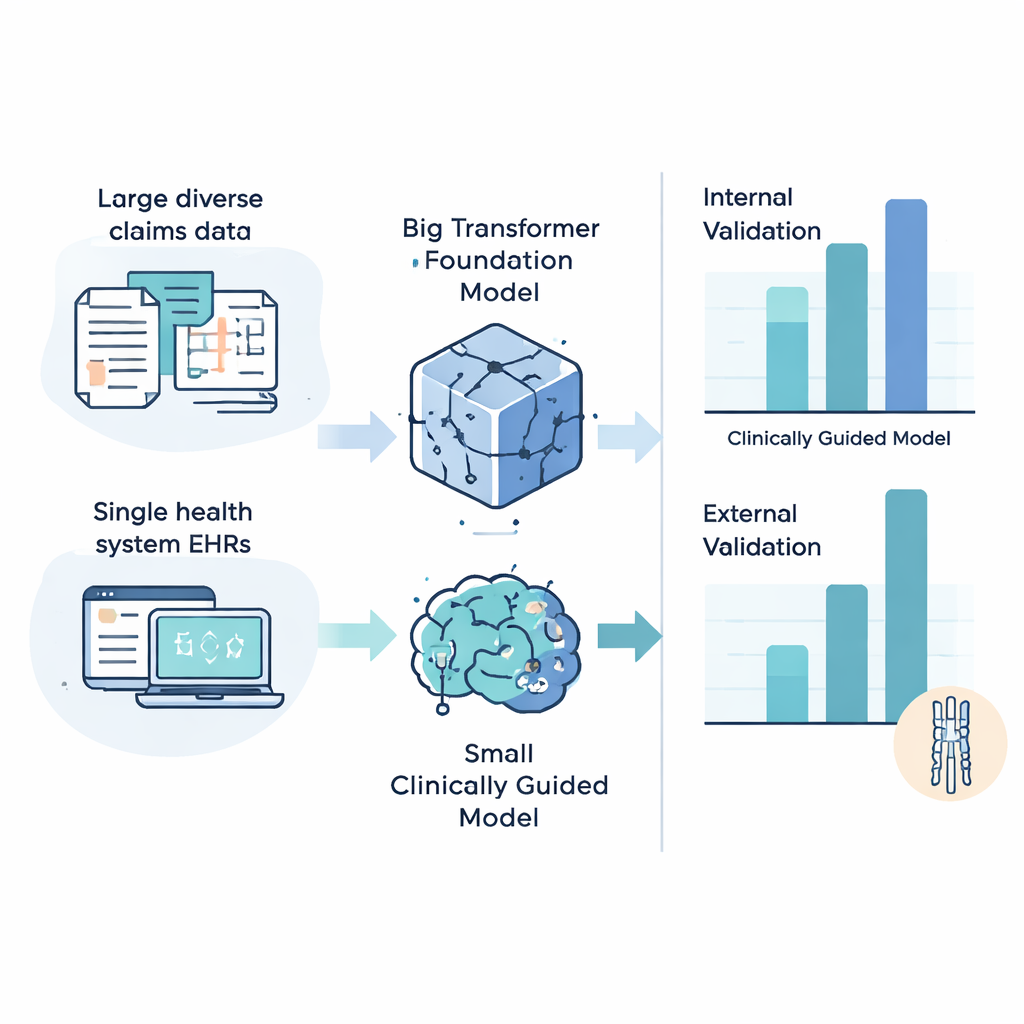
Cuando los modelos se entrenaron y evaluaron dentro del mismo conjunto nacional de seguros, el mayor modelo de base normalmente rindió mejor, alcanzando hasta unas seis o siete veces la precisión de un clasificador no informativo. Sin embargo, el panorama cambió al evaluar los modelos en el sistema de salud independiente. Allí, los modelos más simples y guiados clínicamente en general superaron a los transformadores complejos y, en algunos casos, lograron hasta 13 veces mejor rendimiento que la casualidad para predecir qué pacientes recibirían pronto un diagnóstico de MCE. Un experimento inverso —entrenar en el sistema de salud único y probar en el conjunto nacional— contó una historia similar: los modelos más pequeños y centrados clínicamente tendían a trasladarse mejor entre instituciones. Los análisis por subgrupos también revelaron que todos los modelos funcionaban mejor para pacientes con visitas sanitarias más frecuentes, lo que plantea preguntas sobre equidad para quienes ven al médico con menos regularidad.
Qué significa esto para pacientes y médicos
Los hallazgos sugieren que la IA podría ayudar a señalar a personas con alto riesgo de MCE hasta dos años y medio antes del diagnóstico, orientando potencialmente a los clínicos hacia exámenes neurológicos y estudios de imagen de la columna más tempranos. Sin embargo, el estudio también subraya un intercambio: mientras que los modelos de IA grandes y sofisticados pueden sobresalir con los datos con los que se entrenan, los modelos más pequeños y diseñados con criterio clínico pueden ser más fiables al implementarlos en hospitales y poblaciones de pacientes distintas. Para los pacientes, la conclusión es esperanzadora pero matizada: el uso inteligente de los datos rutinarios de salud podría acortar la larga odisea diagnóstica que muchos con MCE enfrentan, pero el éxito dependerá no solo de algoritmos potentes, sino también de un diseño de modelos reflexivo, pruebas cuidadosas en entornos diversos y atención a la equidad para que los beneficios de la detección temprana se compartan ampliamente.
Cita: Yakdan, S., Warner, B., Ghogawala, Z. et al. Clinically-guided models or foundation models? predicting cervical spondylotic myelopathy from electronic health records. npj Digit. Med. 9, 153 (2026). https://doi.org/10.1038/s41746-026-02337-7
Palabras clave: mielopatía cervical espondilótica, registros electrónicos de salud, aprendizaje automático, modelos de base, diagnóstico temprano