Clear Sky Science · es
Fusión multimodal de modelos básicos de patología y radiología para la subclasificación de gliomas según la OMS 2021
Unir Dos Perspectivas de los Tumores Cerebrales
Cuando a una persona se le diagnostica un tumor cerebral, los médicos necesitan saber no solo que existe un tumor, sino qué tipo exacto es. Los distintos tipos de tumor responden de manera muy diferente a la cirugía, la radiación y los fármacos. Hoy, esta “subclasificación” detallada suele requerir pruebas genéticas que pueden ser lentas, costosas y no estar disponibles en todos los sitios. Este estudio explora si un sistema informático inteligente que analiza tanto las exploraciones cerebrales como las imágenes al microscopio del tejido tumoral puede inferir con fiabilidad estos subtipos, acelerando y ampliando potencialmente el acceso a tratamientos de precisión.
Por Qué Importa el Tipo de Tumor
Los gliomas difusos en adultos están entre los cánceres cerebrales más letales, aunque a menudo se parecen en las exploraciones estándar y en las preparaciones histológicas. Las guías modernas los agrupan en tres subtipos genéticos que difieren mucho en agresividad y en la supervivencia media de los pacientes. El estándar actual para distinguir estos subtipos depende de pruebas moleculares del ADN tumoral. Estas pruebas requieren tejido adicional, laboratorios especializados y esperar días o semanas por los resultados. Los autores plantean si las resonancias magnéticas (RM) de uso rutinario y las laminillas digitales de patología podrían combinarse para extraer suficiente información que compense parte de este trabajo genético.
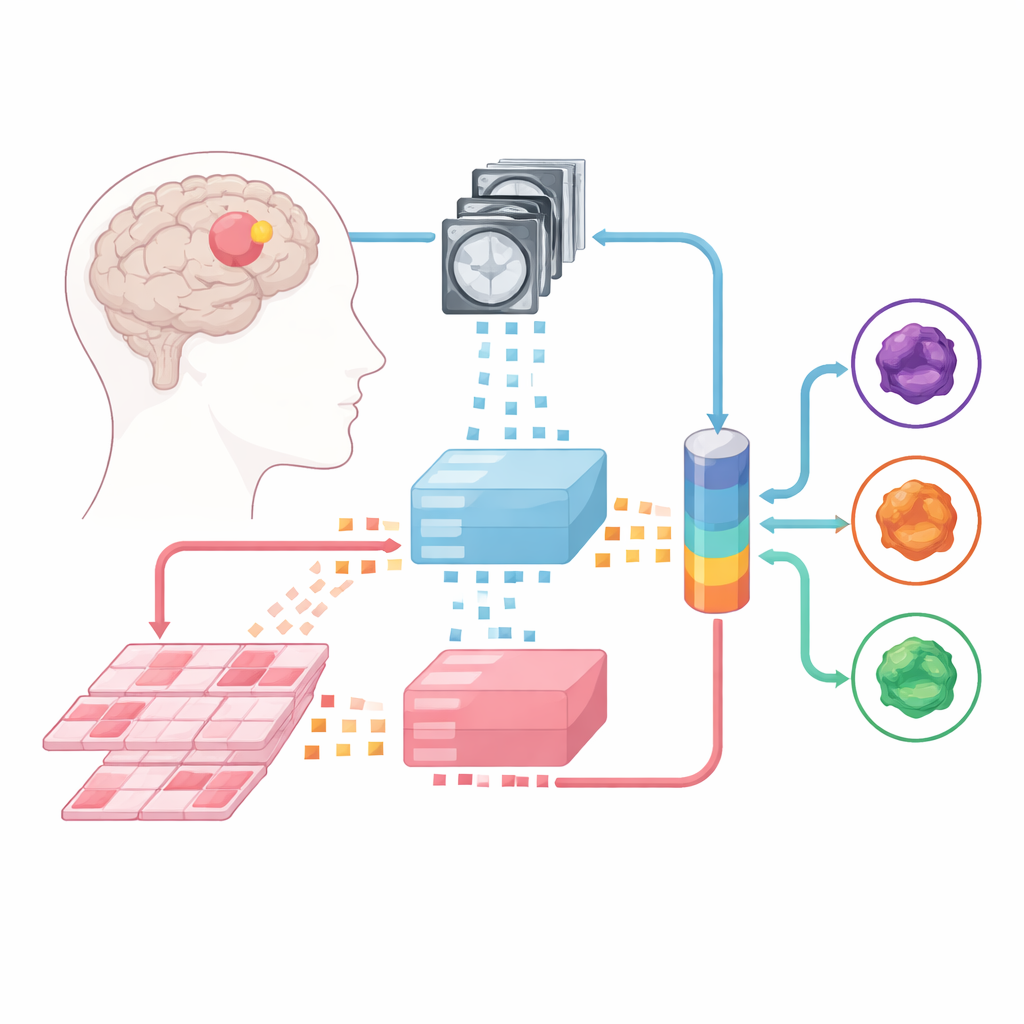
Enseñar a las Máquinas a Leer Escáneres y Laminillas
El equipo se basó en grandes “modelos base” —potentes analizadores de imágenes preentrenados con enormes colecciones de imágenes médicas. Uno de esos modelos procesa RM multiparamétricas y otro maneja laminillas de patología de alta resolución obtenidas del tejido tumoral. Cada caso entrante se divide en pequeños parches de imagen, que los modelos base convierten en huellas numéricas. Sobre estos “expertos” fijos, los investigadores entrenaron tres tipos de modelos de fusión que aprenden a combinar la información de RM y patología: un diseño de fusión tardía, un diseño de fusión temprana y una arquitectura más flexible de mezcla de expertos que puede decidir dinámicamente cuánto apoyarse en cada fuente.
Mezclar Modalidades Sin Emparejar Pacientes
Un obstáculo práctico para estos métodos multimodales es que los hospitales rara vez disponen de grandes conjuntos de datos donde cada paciente tenga RM y patología perfectamente emparejadas. En lugar de depender de datos perfectamente coincidentes, los autores reunieron colecciones separadas: cientos de casos de RM de varios centros y cientos de casos de patología de otro recurso, más un conjunto más pequeño de 171 pacientes de un proyecto público de cáncer que tenían ambos. Durante el entrenamiento, a menudo emparejaban una RM de una persona con una laminilla de patología de otra, siempre que los tumores pertenecieran al mismo subtipo. Sorprendentemente, los modelos entrenados con esos datos “no emparejados” funcionaron tan bien como los entrenados con pares verdaderos y claramente mejor que simplemente promediar dos modelos monomodales separados.
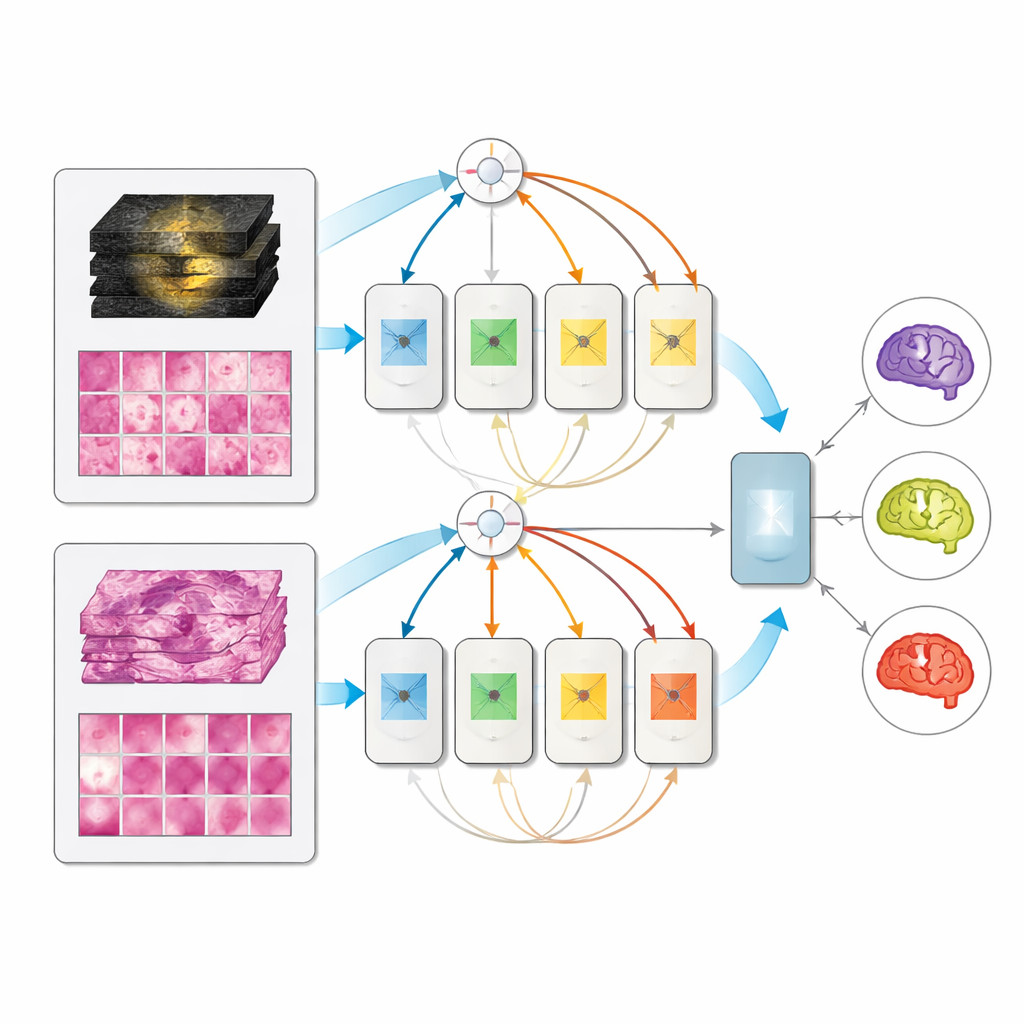
Un Modelo Único que se Adapta a lo Disponible
En el conjunto de validación compuesto por 171 pacientes totalmente caracterizados, todos los modelos multimodales superaron a sus homólogos de entrada única, y el diseño de mezcla de expertos fue el mejor, alcanzando puntuaciones muy altas en la distinción de los tres subtipos. En particular, cuando en la fase de prueba solo se proporcionó RM o solo patología, el modelo multimodal no colapsó; rindió aproximadamente igual que los modelos dedicados a una sola modalidad. Esto significa que una clínica podría desplegar un sistema unificado que use la información disponible —solo exploraciones preoperatorias, solo tejido postoperatorio o ambas— en lugar de mantener herramientas separadas para cada escenario.
Ver Lo que el Modelo Ve
Para generar confianza en las decisiones del sistema, los investigadores examinaron dónde “mira” el modelo y qué características de la imagen importan más. Los mapas de atención mostraron que el modelo conjunto reparte su foco más ampliamente por el tumor y sus alrededores, tanto en RM como en laminillas, y que una atención más difusa tendía a coincidir con predicciones correctas. Un análisis más profundo de las características aprendidas reveló patrones que coinciden con pistas médicas conocidas: por ejemplo, las características de RM que resaltan núcleos tumorales que realzan con contraste y espacios fluidos distorsionados ayudaron a separar tumores más agresivos, mientras que las características tisulares que capturan formas celulares y texturas clásicas ayudaron a reconocer subtipos específicos de glioma. También surgieron lagunas interesantes: el modelo no codificó fuertemente algunos signos de libro de texto de los tumores más agresivos, lo que apoya la idea de que a menudo trata a ese grupo como un “por defecto” salvo que exista evidencia fuerte de un subtipo más favorable.
Qué Podría Significar para los Pacientes
En términos sencillos, este trabajo muestra que un sistema de IA que combina exploraciones cerebrales e imágenes al microscopio puede clasificar tumores cerebrales con más precisión que los sistemas que solo analizan un tipo de imagen, y que puede entrenarse incluso cuando los dos tipos de imagen no provienen de los mismos pacientes. Si se valida adicionalmente en cohortes más grandes y diversas, estas herramientas podrían ayudar a los médicos a estimar el subtipo tumoral antes y en un ámbito más amplio, especialmente donde las pruebas genéticas son limitadas. Aunque no reemplazan las pruebas moleculares, pueden servir como guías rápidas y de bajo costo que orienten a cirujanos y oncólogos hacia el diagnóstico más probable y la vía de tratamiento más adecuada.
Cita: Saueressig, C., Scholz, D., Raffler, P. et al. Multimodal fusion of pathology and radiology foundation models for WHO 2021 glioma subtyping. npj Precis. Onc. 10, 118 (2026). https://doi.org/10.1038/s41698-026-01366-5
Palabras clave: subclasificación de glioma, imágenes multimodales, inteligencia artificial, RM y patología, diagnóstico de cáncer cerebral