Clear Sky Science · es
Perfil cuantitativo de HER2 en tejido y plasma predice la actividad de trastuzumab deruxtecan en cáncer de mama
Por qué esta investigación importa a los pacientes
Para las personas con cáncer de mama metastásico, los fármacos nuevos pueden aportar esperanza, pero no funcionan igual de bien en todos. Este estudio plantea una pregunta práctica: ¿podemos predecir mejor quién se beneficiará más, y durante más tiempo, de un fármaco dirigido ampliamente utilizado llamado trastuzumab deruxtecan (a menudo abreviado T-DXd)? Al examinar con mayor precisión las muestras tumorales y la sangre, los investigadores muestran que la medición detallada de una molécula llamada HER2 —y de ciertos marcadores de ADN y proteínas— puede revelar qué cánceres tienen más probabilidades de responder a este tratamiento.
Un fármaco dirigido con resultados desiguales
T-DXd es un “conjugado anticuerpo-fármaco”, una especie de misil guiado que busca las células que expresan la proteína HER2 y les entrega directamente un cargamento similar a la quimioterapia. Originalmente se usaba para tumores con niveles muy altos de HER2; ahora está aprobado para cerca de nueve de cada diez pacientes con cáncer de mama metastásico, incluidos quienes muestran HER2 bajo o incluso ausente según las pruebas estándar. Sin embargo, en la práctica diaria algunos pacientes disfrutan de largos periodos de control de la enfermedad con T-DXd, mientras que otros ven progresar su cáncer tras solo unos meses. Los métodos de laboratorio tradicionales, que clasifican los tumores en HER2-positivo, HER2-bajo o HER2-cero, han explicado poco estas diferencias.
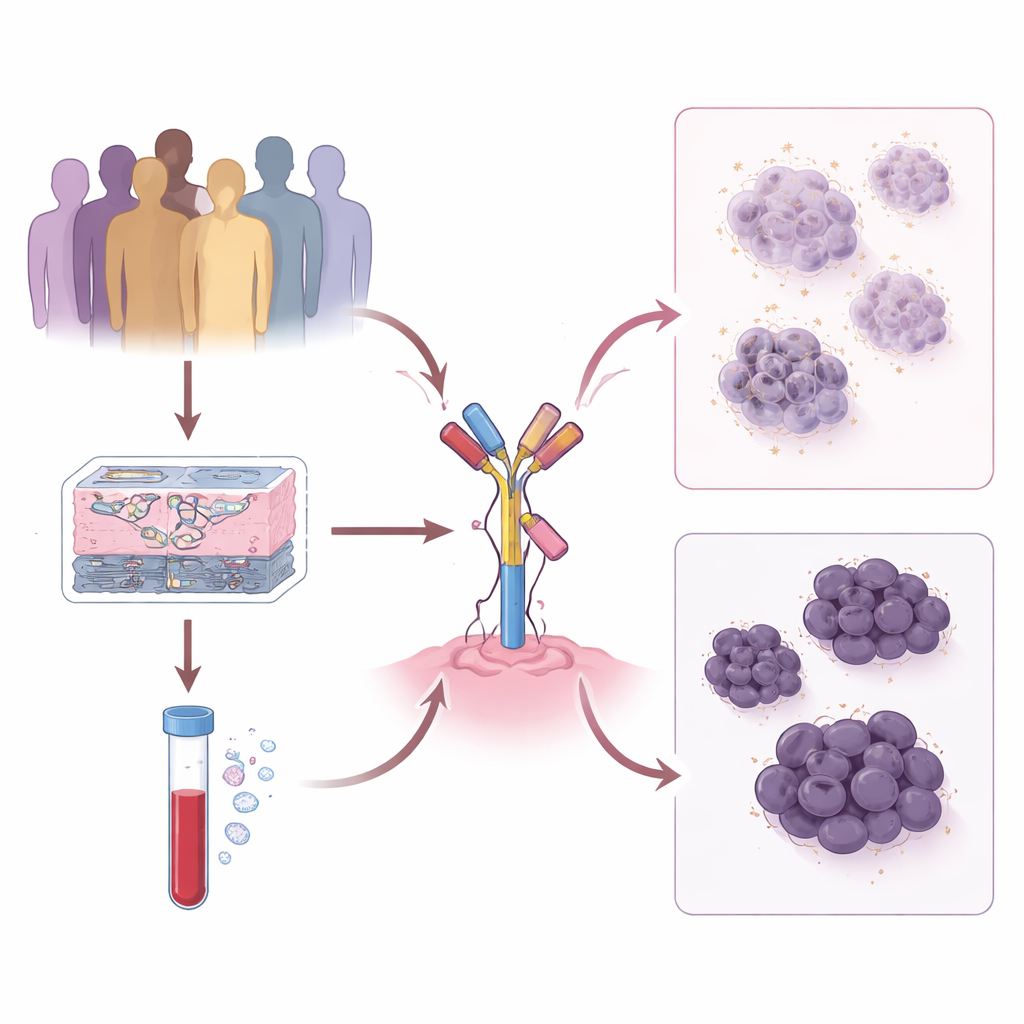
Rastreando cambios en el tumor a lo largo del tiempo
El equipo examinó a 191 pacientes tratados con T-DXd en dos grandes centros oncológicos de EE. UU., revisando cómo se comportaron sus cánceres y cómo cambiaron los niveles de HER2 desde el tumor primario hasta metástasis posteriores. Encontraron que etiquetar una vez un tumor como HER2-bajo o HER2-cero pasaba por alto dinámicas importantes. Los pacientes cuyos cánceres permanecieron claramente HER2-positivos vivieron más tiempo con T-DXd, seguidos por aquellos cuyos tumores mostraron niveles bajos pero estables de HER2. En contraste, cuando HER2 fluctuó entre bajo y cero con el tiempo, el beneficio de T-DXd fue notablemente menor. Estos patrones sugieren que cuanto más establemente dependa un tumor de HER2, mejor puede funcionar este fármaco.
Midiendo HER2 con una regla más fina
Para ir más allá de las categorías gruesas, los investigadores aplicaron una batería de pruebas modernas al tejido tumoral. Una usó inmunofluorescencia cuantitativa para contar con precisión la proteína HER2; otra empleó una matriz proteica de alto rendimiento; una tercera leyó perfiles de expresión génica relacionados con la región del genoma que incluye HER2. En las tres, el mensaje fue consistente: niveles cuantitativos más altos de HER2 —ya sea medidos como proteína en la superficie celular, formas activadas (fosforiladas) o ARN mensajero— se asociaron con mayor tiempo hasta la siguiente terapia y mejor supervivencia global con T-DXd. En los mismos pacientes, la lectura patológica habitual (HER2-positivo, bajo o cero) apenas distinguió los resultados, lo que subraya que “cuánto” HER2 hay importa más que en qué casilla se marca.
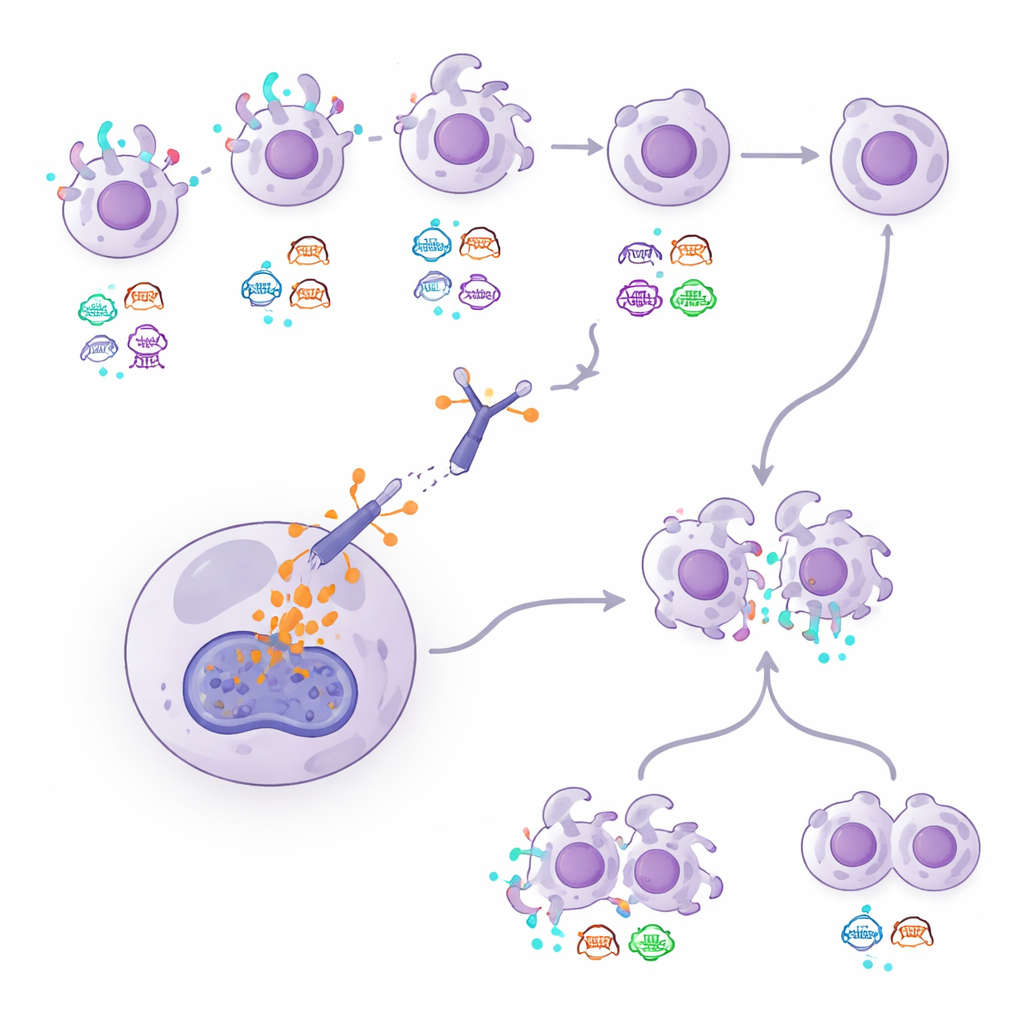
Pistas a partir de pruebas sanguíneas y otros marcadores tumorales
Dado que las biopsias repetidas pueden ser invasivas, el estudio también probó un enfoque basado en sangre que analiza fragmentos de ADN tumoral circulante en el torrente sanguíneo. Usando un método llamado DNADX, los investigadores agruparon las muestras sanguíneas en clústeres biológicos y calcularon una firma de ADN relacionada con HER2. Los pacientes cuya sangre mostró señales más fuertes de HER2 tendieron a permanecer más tiempo con T-DXd, mientras que aquellos con patrones de ADN vinculados a enfermedad más agresiva y de crecimiento rápido tuvieron peores resultados. Los investigadores también observaron que, en cánceres etiquetados como HER2-negativos, niveles altos de una proteína llamada topoisomerasa 1 dentro de las células tumorales se asociaron con peores desenlaces, lo que sugiere que la forma en que la célula maneja la carga del fármaco puede influir en el éxito. Ciertas pérdidas o mutaciones genéticas, como cambios en ERBB2 y TP53 y el enriquecimiento de mutaciones en ARID1B tras el tratamiento, surgieron como posibles marcadores de resistencia.
Qué significa esto para pacientes y clínicos
En conjunto, el estudio muestra que T-DXd es un tratamiento eficaz en el mundo real, especialmente para pacientes cuyos tumores están impulsados de forma fuerte y consistente por HER2. Pero también deja claro que las pruebas tradicionales de HER2 son un instrumento demasiado burdo para guiar este fármaco potente. Al usar mediciones más sensibles en tejido y sangre, los médicos podrían, en el futuro, identificar con mayor precisión a los pacientes con más probabilidades de beneficiarse de T-DXd, salvar a otros de terapias ineficaces y planificar mejor el orden en que se emplean distintos conjugados anticuerpo-fármaco. Aunque estas pruebas avanzadas todavía no son de uso rutinario y requieren validación en cohortes más amplias, apuntan hacia un futuro en el que las decisiones de tratamiento para el cáncer de mama metastásico se basen en retratos moleculares detallados, no solo en etiquetas generales.
Cita: Tarantino, P., Kim, SE., Hughes, M.E. et al. Quantitative HER2 tissue and plasma profiling predicts the activity of trastuzumab deruxtecan for breast cancer. npj Precis. Onc. 10, 141 (2026). https://doi.org/10.1038/s41698-026-01365-6
Palabras clave: Prueba de HER2, trastuzumab deruxtecan, cáncer de mama metastásico, biopsia líquida, conjugados anticuerpo-fármaco