Clear Sky Science · es
La respuesta a midostaurin en LMA está determinada por un estado celular similar a progenitor que es selectivamente atacado por miméticos de SMAC
Por qué algunos fármacos contra la leucemia dejan de funcionar
Para muchas personas con un tipo de cáncer de la sangre llamado leucemia mieloide aguda (LMA), los nuevos fármacos dirigidos han traído esperanza, pero no todos se benefician y las respuestas a menudo se desvanecen. Este estudio plantea una pregunta simple pero crucial: ¿por qué algunas células leucémicas ignoran un fármaco de uso común, el midostaurin, y podemos encontrar una combinación inteligente que obligue a estas células persistentes a morir?
Mirando más allá de la mutación principal
Aproximadamente uno de cada tres pacientes con LMA presenta una alteración en un gen llamado FLT3, que impulsa el crecimiento de la leucemia y es la razón por la que se prescribe midostaurin. Los investigadores probaron muestras de médula ósea y sangre de 63 pacientes con LMA con mutación en FLT3, exponiendo las células a midostaurin y a más de 500 otros fármacos contra el cáncer en el laboratorio. Encontraron que la sensibilidad de las células de un paciente al midostaurin ex vivo se correspondía estrechamente con la respuesta clínica posterior de ese paciente. Sorprendentemente, el tipo exacto de mutación en FLT3 o su abundancia no predijeron de forma fiable el éxito del midostaurin, lo que sugiere que la genética por sí sola no explica quién se beneficia.
Un reservorio oculto de «semillas» resistentes
Profundizando, el equipo comparó los patrones globales de proteínas y actividad génica entre las células sensibles al midostaurin y las que no lo eran. Las muestras no respondedoras estaban enriquecidas en rasgos de progenitores inmaduros y con características de células madre: células más próximas a la raíz de la formación sanguínea y que se consideran «semillas» capaces de reiniciar la leucemia. En contraste, las muestras respondedoras se asemejaban más a células inmunitarias y mieloides parcialmente maduras. Usando métodos avanzados de análisis unicelular, los científicos identificaron una población específica de células leucémicas marcada por las proteínas de superficie CD38 y CD45RA que se comportaba como estas semillas similares a progenitores. Estas células mostraban una organización inusual de su membrana externa, lo que sugiere que moléculas de señalización clave se disponían de formas que favorecían la supervivencia.
Instalación de supervivencia: un cambio en las vías de señalización
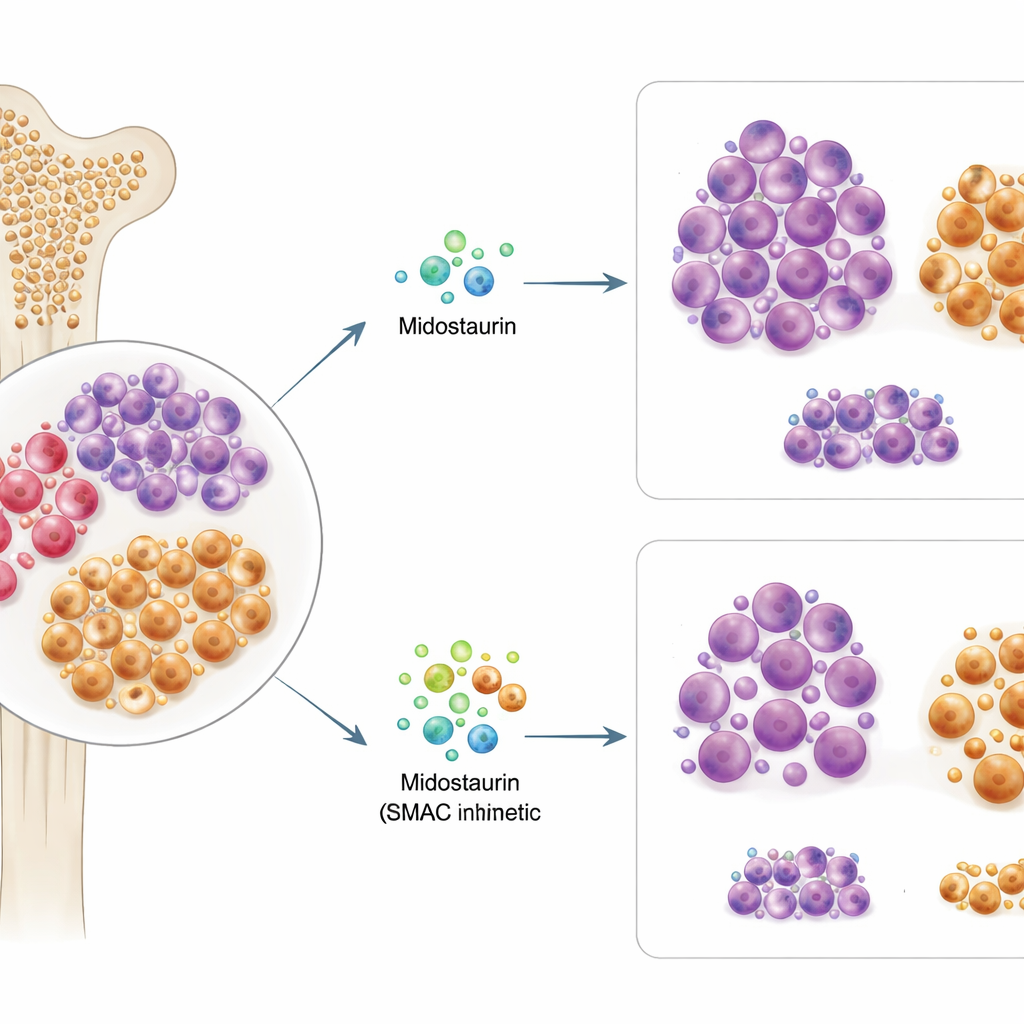
El midostaurin está diseñado para bloquear la señalización de FLT3, que normalmente alimenta una cadena de señales que incluye a la molécula STAT5 y puede impulsar el crecimiento celular. Cuando el equipo examinó la señalización en líneas celulares y muestras de pacientes tras el tratamiento con midostaurin, observaron dos patrones distintos. En las células sensibles al midostaurin, la actividad de STAT5 cayó rápidamente, coherente con un apagado efectivo de FLT3. Sin embargo, en las células resistentes predominaba otra vía: PI3K/AKT, una ruta clásica de supervivencia que ayuda a las células a resistir la muerte. Estas células resistentes mantenían o incluso aumentaban la actividad de AKT tras el tratamiento y mostraban niveles más altos de proteínas que bloquean la apoptosis (muerte celular programada). En otras palabras, el cableado interno de estas células similares a progenitor parecía reconducido para favorecer la supervivencia incluso cuando FLT3 estaba inhibido.
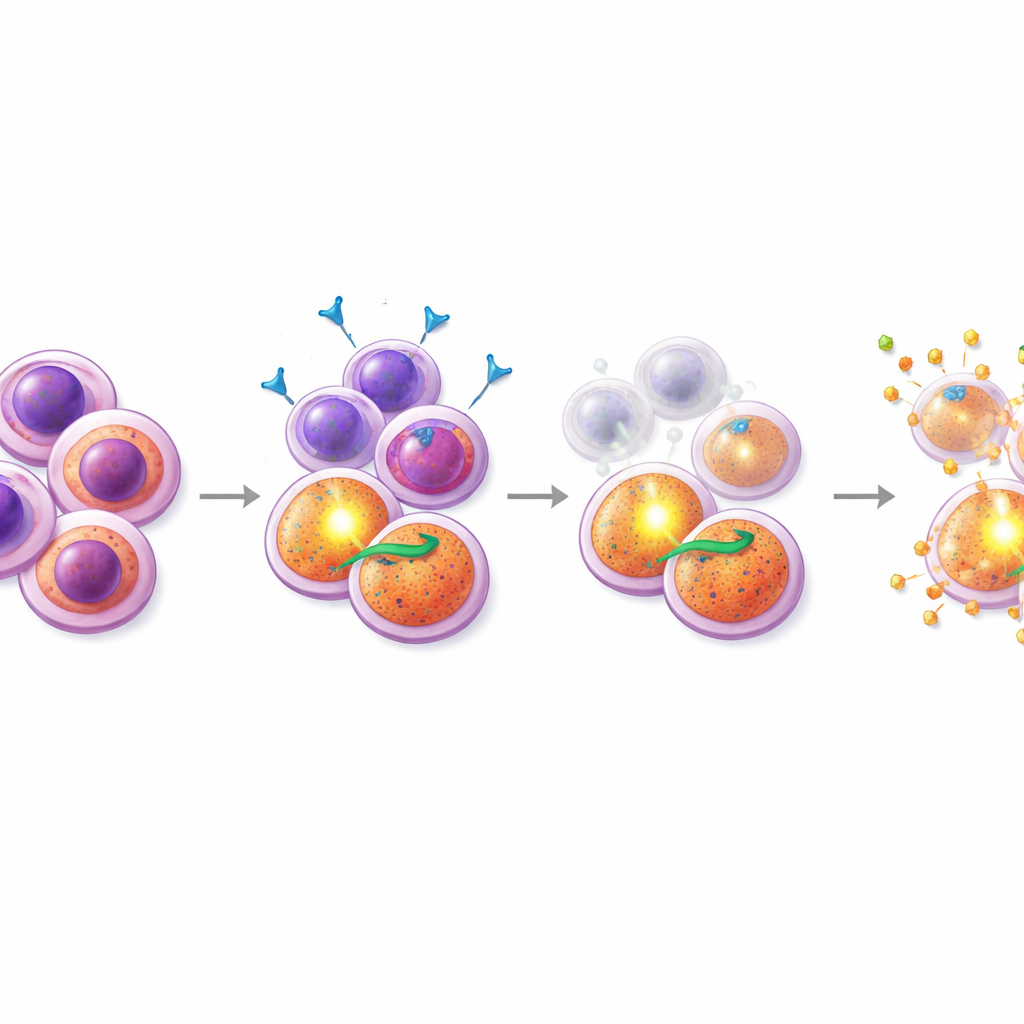
Encontrar un fármaco compañero que golpee el punto débil
Con este conocimiento, los investigadores estudiaron combinaciones de midostaurin con cientos de otros compuestos, centrándose en fármacos que influyen en la muerte celular. Un grupo destacado fueron los miméticos de SMAC, fármacos que inhabilitan a las proteínas inhibidoras de la apoptosis de las que dependen las células impulsadas por PI3K/AKT. En muestras de pacientes resistentes y en una línea celular resistente con mutación en FLT3, añadir miméticos de SMAC como birinapant al midostaurin produjo una fuerte sinergia: juntos, los fármacos mataron muchas más células que cualquiera de ellos por separado. De forma crucial, experimentos detallados de citometría de flujo mostraron que la combinación midostaurin–mimético de SMAC agota selectivamente la población similar a progenitor CD38+CD45RA+ y redujo sus niveles característicos de marcadores de superficie, lo que sugiere que esta terapia apunta específicamente a las semillas difíciles de eliminar. En contraste, las combinaciones con el inhibidor aprobado de BCL‑2, venetoclax, fueron más eficaces contra un subconjunto diferente, con alto CD34, y no mostraron el mismo efecto focalizado sobre las células resistentes.
Qué significa esto para los pacientes
Este trabajo sugiere que la resistencia al midostaurin no depende solo de la mutación en FLT3, sino también del «estado» de las células leucémicas: su nivel de madurez, la organización de la membrana y las vías de supervivencia preferidas. Un subconjunto similar a progenitor CD38+CD45RA+ parece ser un reservorio clave de resistencia, cambiando su señalización desde la ruta habitual de STAT5 hacia un programa de supervivencia PI3K/AKT. Al combinar midostaurin con miméticos de SMAC, los investigadores lograron resensibilizar estas células y llevarlas a la muerte en el laboratorio. Aunque todavía se necesitan estudios clínicos más amplios, los hallazgos apuntan hacia un futuro en el que los médicos podrían usar pruebas funcionales y perfiles del estado celular, no solo la secuenciación del ADN, para elegir combinaciones dirigidas a FLT3 que eliminen tanto la leucemia en masa como sus semillas más resistentes.
Cita: Struyf, N., Gezelius, H., Lundmark, A. et al. Midostaurin response in AML is shaped by a progenitor-like cell state selectively targeted by SMAC mimetics. npj Precis. Onc. 10, 117 (2026). https://doi.org/10.1038/s41698-026-01363-8
Palabras clave: leucemia mieloide aguda, inhibidores de FLT3, resistencia a fármacos, células madre leucémicas, miméticos de SMAC