Clear Sky Science · es
Fibroblastos asociados al cáncer con alta expresión de COL3A1 orquestan microambientes metabólicos e inmunitarios para conferir quimiorresistencia en cáncer de mama
Por qué algunos tumores de mama resisten la quimioterapia
La quimioterapia puede salvar vidas en el cáncer de mama, sin embargo muchos pacientes descubren que sus tumores dejan de responder o nunca respondieron bien desde el principio. Este estudio mira más allá de las propias células cancerosas hacia el vecindario en el que viven y se pregunta: ¿qué células cercanas ayudan a los tumores a sobrevivir al tratamiento, y cómo lo hacen? La respuesta se centra en un grupo especial de células de soporte que reconfiguran tanto la nutrición tumoral como la inmunidad local para proteger a las células cancerosas de la quimioterapia.
Los ayudantes ocultos alrededor del tumor
Los tumores de mama son más que solo células cancerosas; son comunidades mixtas que incluyen vasos sanguíneos, células inmunitarias y células del tejido conectivo llamadas fibroblastos. Cuando los fibroblastos habitan en un tumor se les conoce como fibroblastos asociados al cáncer, o CAFs, y pueden tanto frenar como promover el cáncer. Combinando varias técnicas potentes de perfilado genético en muestras de pacientes—análisis unicelular, espacial y a granel—junto con experimentos de laboratorio y en animales, los investigadores identificaron un subgrupo de CAFs que produce altos niveles de una molécula llamada COL3A1, un componente del armazón tisular. Los pacientes cuyos tumores contenían más de estos CAFs con alta COL3A1 tenían mayor probabilidad de mostrar respuestas pobres a la quimioterapia y una supervivencia peor.
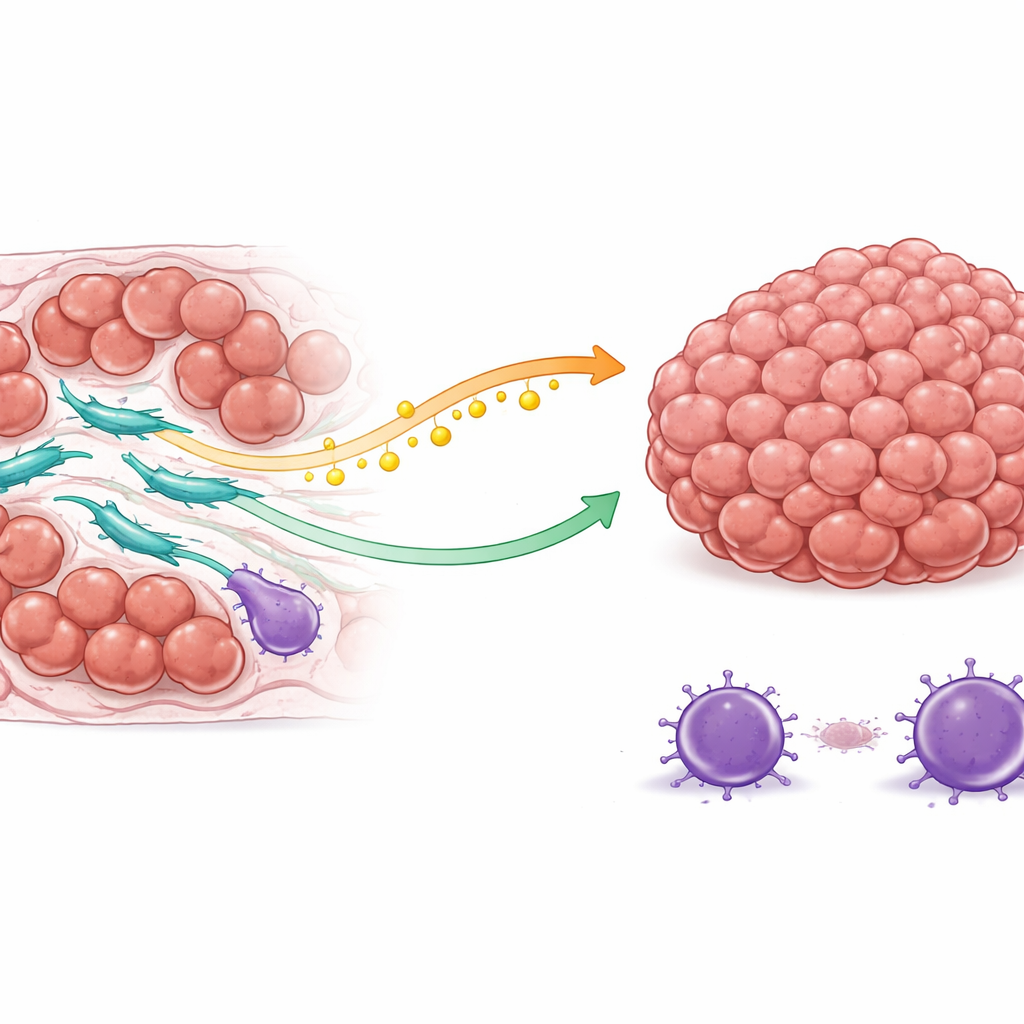
Un escudo en dos frentes: combustible y protección
El equipo descubrió que los CAFs con alta COL3A1 protegen a las células cancerosas de dos maneras principales. Primero, cambian su manejo de las grasas. Estos fibroblastos aumentan la actividad de una enzima que sintetiza ácido oleico, un tipo de grasa. En lugar de conservar este combustible, lo liberan en el entorno tumoral. Las células cancerosas captan este ácido oleico a través de una proteína de superficie y, en respuesta, activan una vía interna de supervivencia conocida por ayudar a las células a resistir señales de muerte. Como resultado, cuando la quimioterapia intenta activar los programas de autodestrucción de las células cancerosas, esas células están mejor equipadas para resistir y seguir dividiéndose.
Moldeando un vecindario inmunitario poco favorable
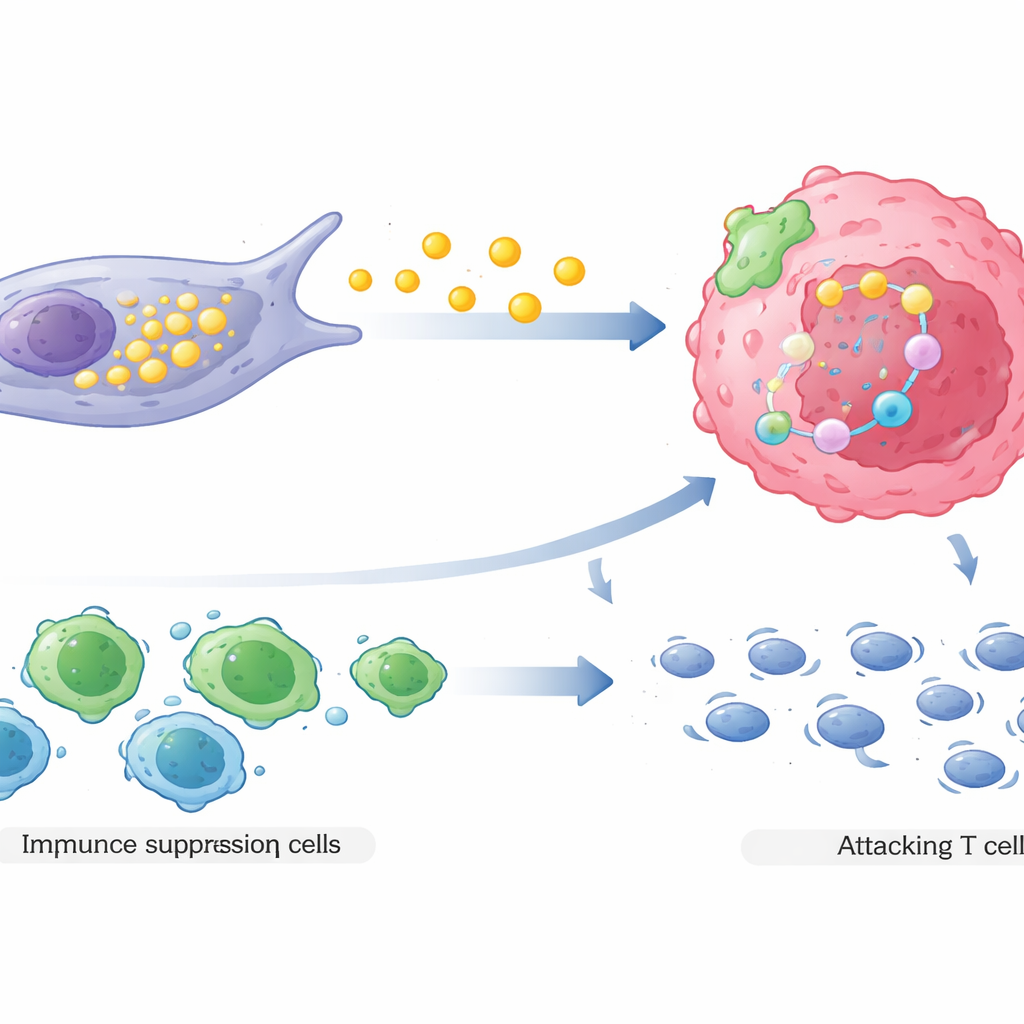
Segundo, los CAFs con alta COL3A1 remodelan el paisaje inmunitario local a favor del tumor. Mediante interacciones de señalización complejas, atraen a células T reguladoras, un tipo de célula inmunitaria que atenúa los ataques inmunitarios, y al mismo tiempo desaniman o debilitan a las células T citotóxicas que normalmente atacarían al cáncer. El mapeo espacial de tumores reales de pacientes mostró que estos fibroblastos tienden a situarse cerca tanto de células cancerosas resistentes a fármacos como de células inmunes supresoras, mientras que las células T citotóxicas efectivas quedan desplazadas a mayor distancia. Esta disposición crea una zona protegida donde las células cancerosas enfrentan menos amenazas inmunitarias justo cuando también se vuelven más difíciles de matar con fármacos.
Pruebas en células, ratones y pacientes
Para probar causa y efecto, los investigadores redujeron COL3A1 en CAFs cultivados en el laboratorio. Cuando células de cáncer de mama se desarrollaron junto a estos fibroblastos alterados, formaron menos estructuras invasivas, fueron más fácilmente eliminadas por el fármaco quimioterápico paclitaxel y mostraron más señales de muerte celular programada. En ratones implantados con mezclas de células de cáncer de mama y CAFs, bloquear COL3A1 en los fibroblastos ralentizó el crecimiento tumoral bajo quimioterapia y disminuyó los niveles de la enzima productora de lípidos y del receptor de las células cancerosas vinculado al ácido oleico. En un grupo de 72 pacientes tratados con quimioterapia antes de la cirugía, niveles más altos de COL3A1 y de sus asociados en el metabolismo de lípidos se correlacionaron fuertemente con peores respuestas al tratamiento y con un tiempo más corto antes de la recurrencia del cáncer.
Qué significa esto para tratamientos futuros
En términos sencillos, el estudio muestra que un conjunto particular de células de soporte en los tumores de mama actúa como una unidad de guardaespaldas: alimentan a las células cancerosas con una dieta protectora basada en grasas y reclutan aliados inmunitarios que atenúan las defensas del organismo. Juntas, estas acciones hacen que la quimioterapia sea menos eficaz. Medir la abundancia de fibroblastos con alta COL3A1 mejora la capacidad de los médicos para predecir quién responderá o no al tratamiento, y las vías que emplean—producción de lípidos, señalización de supervivencia dentro de las células cancerosas y supresión inmune—ofrecen nuevas dianas para fármacos. En el futuro, terapias que desarmen o reprograme n estos fibroblastos podrían combinarse con la quimioterapia estándar para evitar que los tumores desarrollen resistencia.
Cita: Jiang, P., Li, X., Wang, Z. et al. COL3A1high cancer-associated fibroblasts orchestrate metabolic and immune microenvironments to confer chemoresistance in breast cancer. npj Precis. Onc. 10, 139 (2026). https://doi.org/10.1038/s41698-026-01338-9
Palabras clave: cáncer de mama, quimiorresistencia, microambiente tumoral, fibroblastos asociados al cáncer, metabolismo de lípidos