Clear Sky Science · es
Integración de la biopsia líquida y las firmas mutacionales para avanzar en la oncología de precisión
Por qué importa un análisis de sangre para la “huella” del cáncer
El cáncer suele describirse como una enfermedad del ADN, pero el tumor de cada persona es genéticamente distinto y puede cambiar con el tiempo. Esto dificulta que los médicos elijan el tratamiento adecuado y sepan cuándo un cáncer reaparece o se vuelve resistente a los fármacos. Este artículo explica un enfoque prometedor que combina una sencilla prueba de sangre, llamada biopsia líquida, con patrones detallados de daño en el ADN conocidos como firmas mutacionales. Juntos, podrían permitir a los médicos seguir el comportamiento del tumor a lo largo de la enfermedad del paciente y adaptar las terapias con más precisión que nunca. 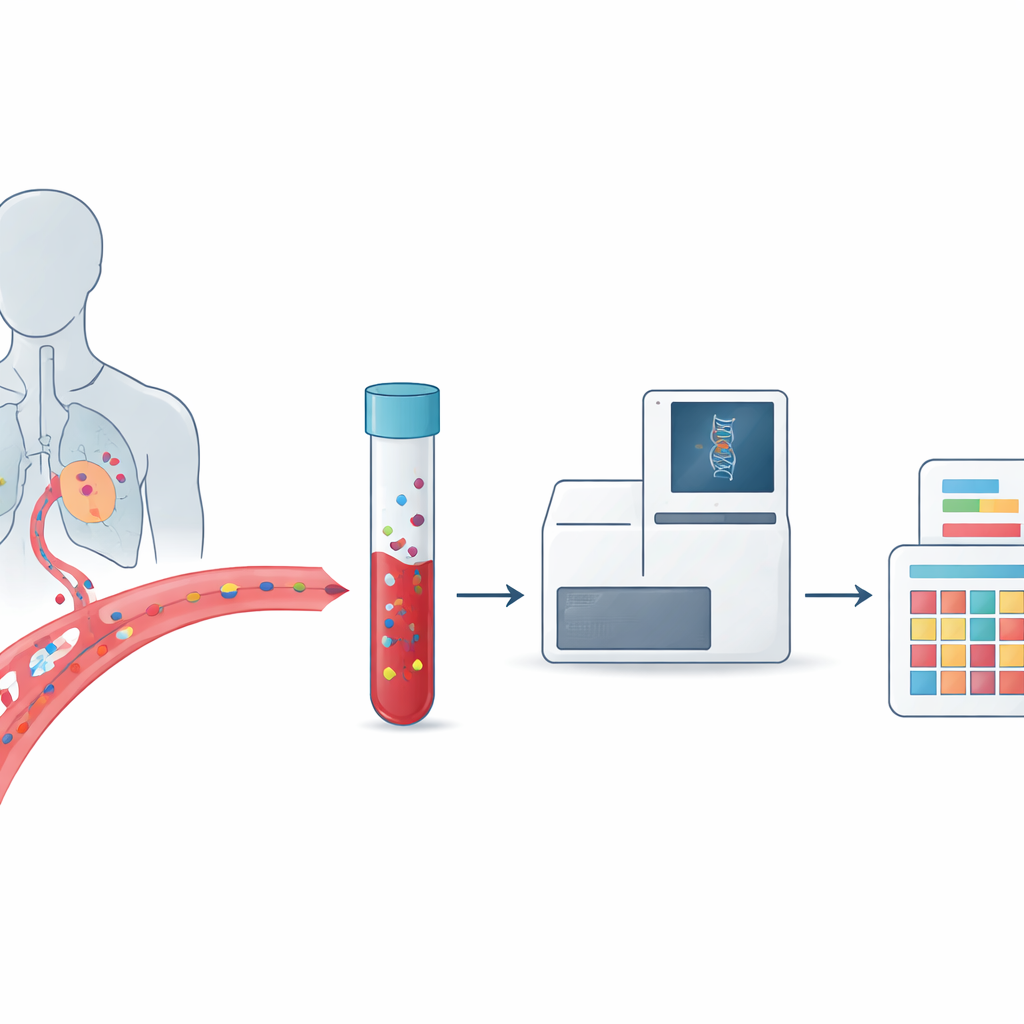
Buscando pistas del cáncer en un tubo de sangre
Las biopsias tradicionales requieren extraer un fragmento de tejido tumoral mediante cirugía o una aguja, lo que puede ser doloroso, arriesgado y difícil de repetir. La biopsia líquida toma un camino distinto: busca rastros del cáncer que los tumores liberan al torrente sanguíneo y otros fluidos corporales. Esos rastros incluyen células tumorales completas y fragmentos cortos de ADN liberados cuando las células cancerosas mueren. Como se pueden extraer muestras de sangre de forma regular y éstas capturan material de múltiples focos tumorales, la biopsia líquida ofrece una imagen en movimiento de cómo el cáncer crece, se disemina y responde al tratamiento, en lugar de una instantánea única en el tiempo.
De mutaciones individuales a patrones globales de daño
La mayoría de las pruebas de biopsia líquida actuales se centran en detectar mutaciones concretas en una lista reducida de genes que orientan el uso de fármacos dirigidos. Sin embargo, no todos los tumores presentan esos cambios “diana”, y los cánceres con muchas mutaciones pueden escapar fácilmente de paneles génicos fijos. En la última década, herramientas potentes de secuenciación del ADN han revelado que las mutaciones en un genoma tumoral no son azarosas: forman patrones reconocibles moldeados por factores como el humo del tabaco, la radiación ultravioleta, fallos en la reparación del ADN o la propia quimioterapia. Estos patrones recurrentes, llamados firmas mutacionales, actúan como huellas dactilares de los procesos que han dañado el ADN a lo largo de la vida del tumor.
Leer la historia y las debilidades del tumor
Las firmas mutacionales pueden revelar dónde pudo haberse originado un cáncer y qué sistemas internos de reparación están rotos. Por ejemplo, los carcinomas pulmonares en fumadores suelen mostrar un patrón vinculado a la exposición al tabaco, mientras que algunos cánceres de colon presentan firmas de fallo del corrector de emparejamientos (mismatch repair), un defecto que también los hace muy sensibles a ciertas inmunoterapias. Otras firmas señalan problemas en una vía de reparación del ADN llamada recombinación homóloga, que puede volver a los tumores especialmente vulnerables a fármacos a base de platino y a inhibidores de PARP. Estudios experimentales en células y modelos animales han confirmado que muchos químicos ambientales y tratamientos contra el cáncer dejan huellas mutacionales distintivas que coinciden con las observadas en pacientes, reforzando el vínculo entre firma y causa. 
Combinar el seguimiento en sangre con las huellas del ADN
La idea clave del artículo es fusionar la biopsia líquida con las firmas mutacionales en un marco único. Mediante la secuenciación amplia, a nivel del genoma, de fragmentos de ADN tumoral en sangre, los médicos podrían identificar simultáneamente mutaciones individuales y los patrones globales de daño que las generaron. Esto podría mejorar la detección temprana del cáncer, ayudar a localizar el tejido de origen en casos enigmáticos y refinar las opciones de tratamiento incluso cuando faltan las mutaciones conductoras clásicas. Extracciones sanguíneas repetidas durante meses o años podrían mostrar cuándo un tumor cambia a un nuevo proceso mutacional, por ejemplo uno inducido por la exposición continuada a un fármaco, señalando la aparición de resistencia o el riesgo de un segundo cáncer relacionado con la terapia.
Obstáculos en el camino hacia el uso cotidiano
A pesar de su potencial, este enfoque se enfrenta a desafíos prácticos. Algunos tumores liberan muy poco ADN al torrente sanguíneo, lo que dificulta detectar sus señales. Muchas firmas conocidas aún carecen de una explicación biológica clara, y algunos patrones pueden verse influenciados por peculiaridades técnicas de distintas plataformas de secuenciación. Los cambios relacionados con la edad en las células formadoras de sangre pueden introducir sus propias mutaciones en el ADN circulante, complicando aún más el panorama. Los métodos actuales para extraer firmas del plasma suelen depender de herramientas complejas de aprendizaje automático que requieren grandes conjuntos de datos de entrenamiento y se han probado principalmente en estudios retrospectivos de investigación más que en ensayos clínicos prospectivos.
Qué podría significar esto para la atención del cáncer en el futuro
Los autores concluyen que integrar la biopsia líquida con las firmas mutacionales podría, eventualmente, transformar la atención del cáncer de una serie de decisiones puntuales en un proceso actualizado de forma continua. En lugar de depender únicamente de una biopsia tisular tomada en el diagnóstico, los clínicos podrían usar algún día pruebas de sangre rutinarias para seguir la “caligrafía” en evolución del daño del ADN en el tumor de un paciente. Esto podría afinar el cribado, mejorar el diagnóstico, orientar la selección y el orden de las terapias y detectar la resistencia antes de que sea visible en las exploraciones. Hacer realidad esta visión requerirá métodos estandarizados, validación rigurosa y modelos computacionales más inteligentes, pero el concepto apunta hacia un futuro en el que el tratamiento del cáncer no solo se dirija a las mutaciones actuales del tumor, sino que también esté informado por las fuerzas que las generaron.
Cita: Carrasco, R., Dreij, K. Integrating liquid biopsy and mutational signatures to advance precision oncology. npj Precis. Onc. 10, 114 (2026). https://doi.org/10.1038/s41698-026-01337-w
Palabras clave: biopsia líquida, firmas mutacionales, ADN libre de células, oncología de precisión, evolución del cáncer