Clear Sky Science · es
Validación clínica de un ensayo de enriquecimiento del metiloma genómico independiente del tejido para monitorizar la respuesta a pembrolizumab
Vigilar el tratamiento del cáncer con una simple extracción de sangre
Las personas con cáncer avanzado y sus médicos a menudo esperan semanas o meses para saber si un fármaco de inmunoterapia está funcionando de verdad. Las exploraciones pueden ser difíciles de interpretar y las biopsias de tejido repetidas son invasivas o incluso imposibles. Este estudio explora un nuevo tipo de análisis de sangre que lee pequeñas marcas químicas en el ADN tumoral que flota en el torrente sanguíneo, ofreciendo una forma más rápida y menos invasiva de comprobar si el fármaco pembrolizumab está siendo eficaz.
Por qué las comprobaciones actuales no son suficientes
Los fármacos de inmunoterapia como el pembrolizumab pueden producir respuestas notables y duraderas, pero solo en una fracción de los pacientes. Hoy, los clínicos confían en características del tumor como los niveles de PD-L1 o el recuento de mutaciones medidos a partir de biopsias de tejido, junto con exploraciones de imagen periódicas. Estos enfoques presentan inconvenientes importantes: las muestras de biopsia no siempre están disponibles, pueden no reflejar todo el tumor y normalmente se miden solo una vez antes de iniciar el tratamiento. La imagenología puede inducir a error porque las células inmunitarias que entran en el tumor pueden hacerlo parecer temporalmente mayor, un fenómeno conocido como pseudoprogresión. En conjunto, estas limitaciones hacen que los pacientes puedan continuar con terapias ineficaces durante meses antes de que quede claro que no funcionan.
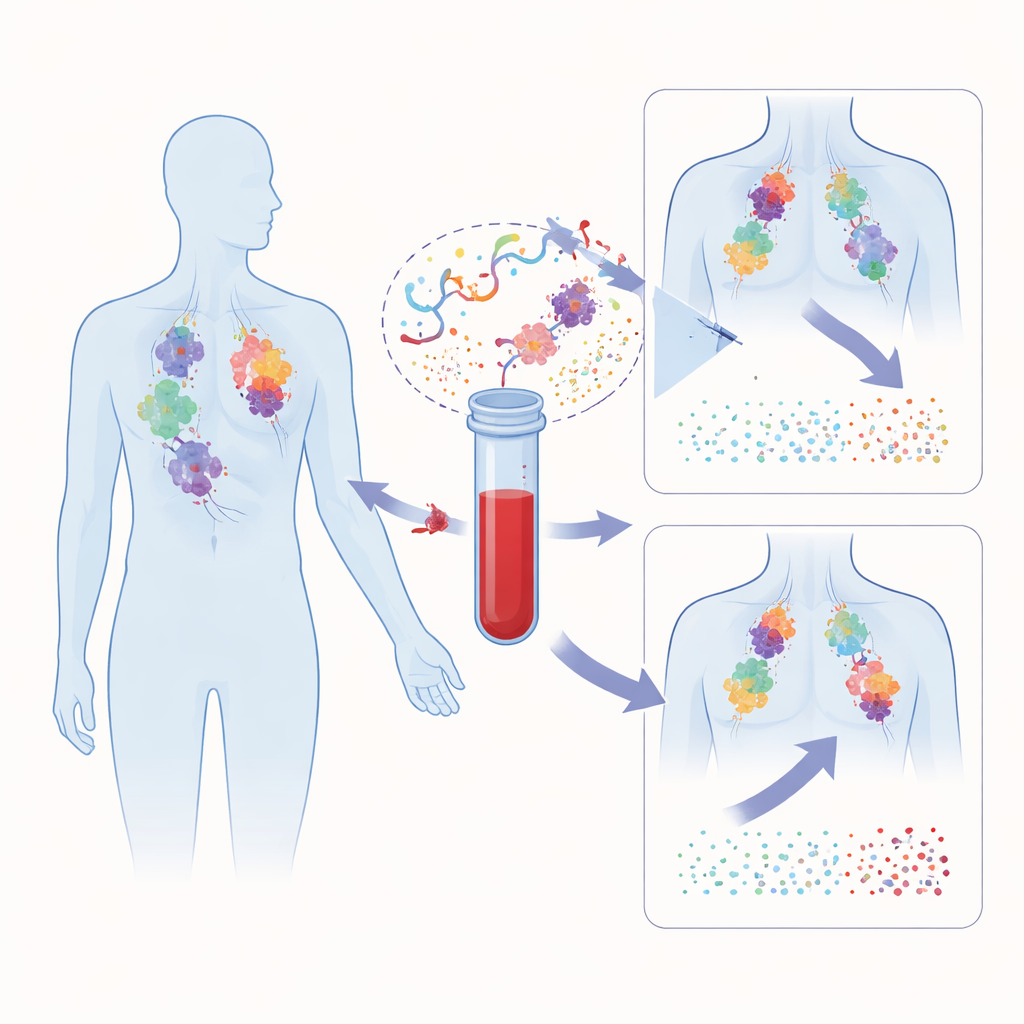
Una prueba de sangre universal en lugar de biopsias de tumor
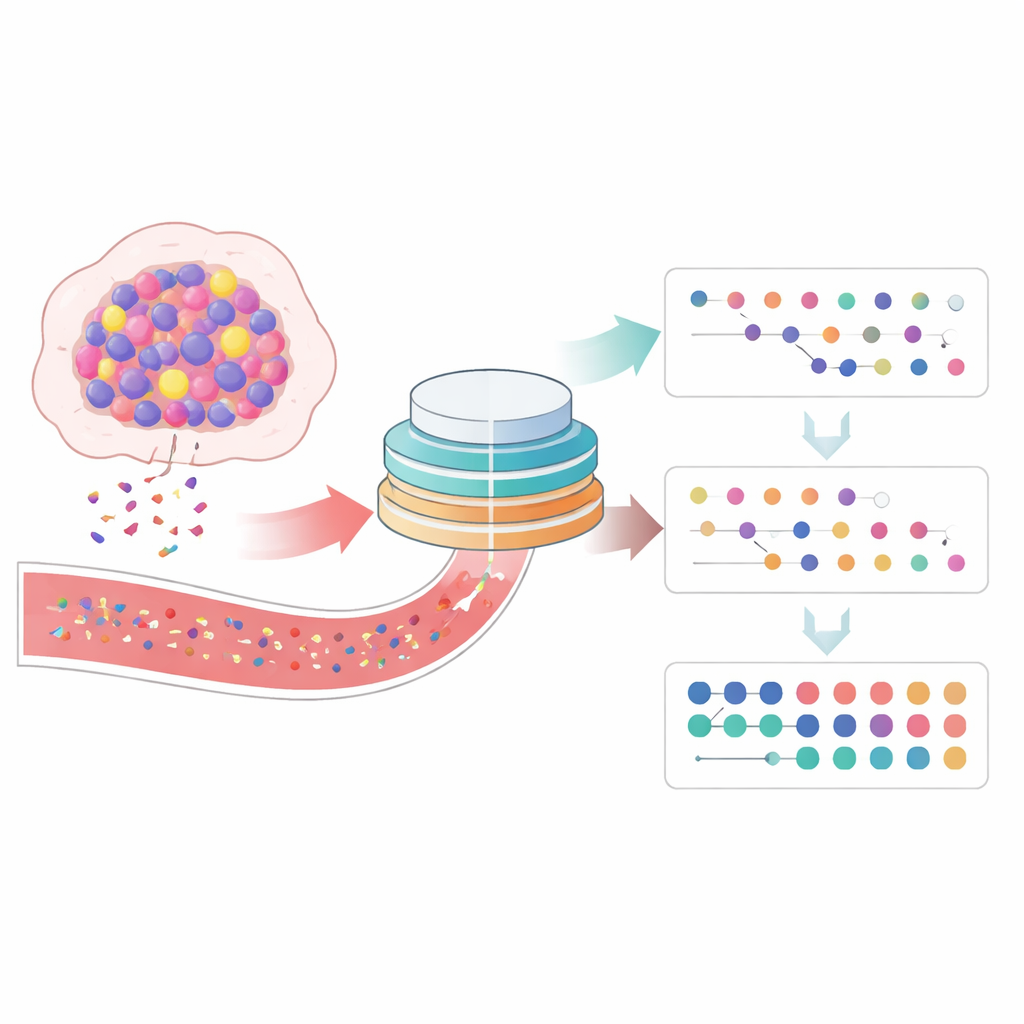
Los investigadores evaluaron un ensayo sanguíneo “independiente del tejido” que no necesita una muestra previa del tumor del paciente. En su lugar, se centra en la metilación del ADN: etiquetas químicas estables que decoran el ADN y difieren entre las células sanas y las cancerosas. Los tumores liberan constantemente fragmentos de ADN en el torrente sanguíneo, creando ADN tumoral circulante (ctDNA). Usando una técnica llamada cfMeDIP-seq, el equipo enriquece y secuencia solo los fragmentos metilados del plasma y luego aplica un clasificador entrenado con grandes conjuntos de datos de cáncer y no cáncer. Esto produce una puntuación numérica de ctDNA que refleja cuánto ADN derivado del tumor está presente en la sangre, independientemente de dónde se haya originado el cáncer en el cuerpo.
Rastreando la respuesta a pembrolizumab en varios cánceres
Para ver si esta prueba podía monitorizar la respuesta a la inmunoterapia, los científicos analizaron 241 muestras de sangre de 69 personas con diversos tumores sólidos avanzados inscritas en el ensayo INSPIRE. Los participantes, que no habían recibido inmunoterapia previamente, fueron tratados con pembrolizumab en monoterapia y les extrajeron sangre antes del tratamiento y luego cada tres ciclos, empezando alrededor del tercer tratamiento. La pregunta principal fue simple: ¿la puntuación de ctDNA sube o baja desde el inicio del tratamiento hasta el tercer ciclo? Los pacientes se agruparon en consecuencia y se siguieron para evaluar la respuesta tumoral, el tiempo hasta el empeoramiento de la enfermedad y la supervivencia global.
Lo que revelaron los cambios en el ADN tumoral
La mitad de los pacientes mostró una caída en la puntuación de ctDNA para el tercer ciclo y la otra mitad mostró un aumento. El patrón temprano fue llamativo: ninguno de los pacientes cuyo ctDNA aumentó presentó una reducción tumoral significativa, y casi todos dejaron de beneficiarse de la terapia. En contraste, casi todos los pacientes que respondieron clínicamente tuvieron una disminución del ctDNA. Una puntuación en descenso se asoció fuertemente con mayores probabilidades de reducción tumoral, periodos más largos antes de la progresión de la enfermedad y, en análisis más sencillos, mayor supervivencia global. Cuando el equipo examinó más allá de ese único punto temporal temprano, encontró que los pacientes cuyos niveles de ctDNA se mantuvieron por debajo de su línea base inicial a lo largo del tratamiento tendieron a vivir más y a permanecer libres de progresión más tiempo que aquellos cuyo ctDNA se elevó por encima de la línea base en algún momento.
Cómo se compara esta prueba con otras señales
El equipo también comparó los cambios en ctDNA con marcadores más familiares como la expresión de PD-L1 y la carga mutacional tumoral medida en tejido. Si bien niveles más altos de PD-L1 mostraron alguna relación con el beneficio en análisis básicos, estos marcadores tisulares perdieron significación una vez que las dinámicas de ctDNA se incluyeron en modelos más complejos. En contraste, los cambios tempranos en ctDNA siguieron siendo un indicador fuerte e independiente de cómo les iría a los pacientes, especialmente para la supervivencia libre de progresión. Es importante destacar que este desempeño igualó lo que se había logrado previamente con pruebas de ctDNA personalizadas e informadas por el tumor que requieren la secuenciación previa del tumor de cada paciente; sin embargo, el nuevo ensayo funciona solo a partir de sangre y puede aplicarse a muchos tipos de cáncer.
Qué podría significar esto para los pacientes
En términos prácticos, este estudio sugiere que una prueba sanguínea especializada puede indicar, en pocos ciclos de tratamiento, si el pembrolizumab probablemente está ayudando al cáncer de un paciente. Una caída consistente del ADN tumoral en la sangre señala una mayor probabilidad de beneficio, mientras que niveles en ascenso advierten que la enfermedad puede estar resistiendo la terapia. Debido a que el método no depende de disponer de tejido tumoral y puede repetirse con el tiempo, podría permitir a los médicos tomar decisiones antes y mejor informadas sobre continuar, cambiar o intensificar el tratamiento. Serán necesarios ensayos prospectivos más amplios, pero este trabajo aporta pruebas sólidas de que leer los patrones de metilación en el ADN tumoral presente en sangre podría convertirse en una herramienta potente y de uso generalizado para guiar la inmunoterapia.
Cita: Stutheit-Zhao, E.Y., Zhong, Y., Melton, C.A. et al. Clinical validation of a tissue-agnostic genome-wide methylome enrichment assay to monitor response to pembrolizumab. npj Precis. Onc. 10, 129 (2026). https://doi.org/10.1038/s41698-026-01327-y
Palabras clave: ADN tumoral circulante, monitorización de inmunoterapia, biopsia líquida, metilación del ADN, pembrolizumab