Clear Sky Science · es
Predicción de la deficiencia de recombinación homóloga y de las respuestas al tratamiento mediante un modelo fundacional basado en tomografía computarizada: un estudio preclínico
Por qué esto importa para pacientes y médicos
Los tratamientos contra el cáncer que dañan el ADN, como ciertas quimioterapias y nuevos fármacos dirigidos, pueden ser extraordinariamente eficaces en tumores cuyos sistemas de reparación ya son defectuosos. El reto es identificar qué tumores presentan estas debilidades ocultas sin depender de biopsias invasivas repetidas. Este estudio explora si las exploraciones de estilo médico de rutina en ratones, interpretadas por un potente modelo de inteligencia artificial, pueden revelar cuán vulnerable es un tumor y qué probabilidad tiene de responder a un fármaco experimental.
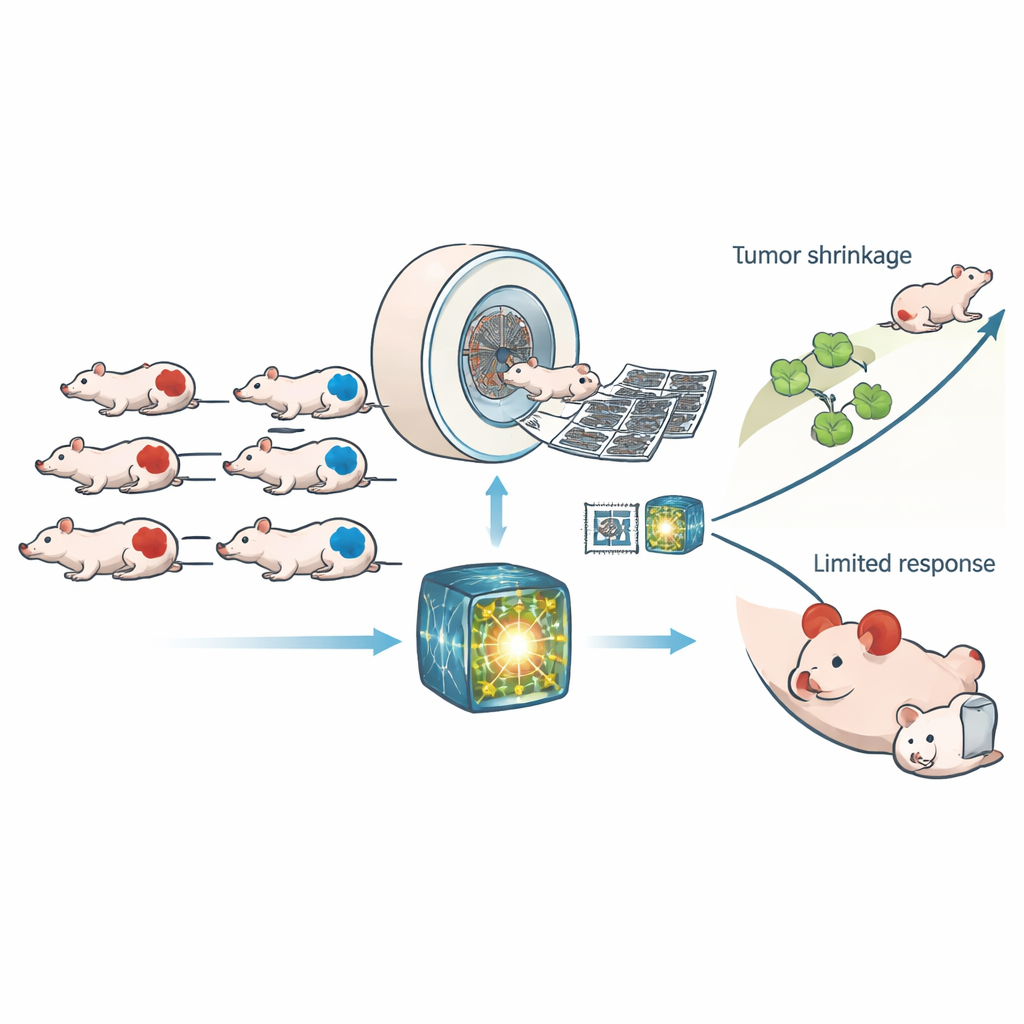
Un punto débil oculto en las células cancerosas
Muchos tumores presentan defectos en una vía clave de reparación del ADN llamada recombinación homóloga. Cuando esta vía falla, las células acumulan daños en su material genético, una condición conocida como deficiencia de recombinación homóloga, o HRD por sus siglas en inglés. La HRD puede facilitar la aparición del cáncer, pero también se convierte en un talón de Aquiles: los fármacos que dañan aún más el ADN pueden empujar a estas células ya estresadas más allá de su capacidad, matándolas con mayor eficacia que a las células sanas. Hoy en día, identificar la HRD suele depender de pruebas genéticas o ensayos de laboratorio especializados que son costosos, lentos y a menudo requieren tomar muestras del tumor. Los autores se preguntaron si la imagenología—el mismo tipo de exploraciones tridimensionales por rayos X ampliamente usadas en clínicas—podría ofrecer una ventana rápida y no invasiva hacia la HRD.
Usar exploraciones inteligentes en lugar de más biopsias
Los investigadores trabajaron con 307 ratones portadores de injertos tumorales humanos que eran o bien HRD o bien normales en su capacidad de reparación. Todos los animales se sometieron a tomografías computarizadas (TC) de alta resolución antes y después de recibir ya fuera un tratamiento control o CP‑506, un fármaco experimental que se activa en regiones tumorales con bajo oxígeno y que entrecruza las hebras de ADN. En lugar de confiar en unas pocas mediciones de imagen hechas a mano, el equipo utilizó un “modelo fundacional” moderno entrenado con grandes conjuntos de TC humanos para extraer miles de patrones sutiles de cada exploración. A continuación se entrenó un clasificador simple sobre estos patrones para decidir si un tumor presentaba HRD, y las mismas características aprendidas se reusaron para predecir cuánto daño en el ADN y cuánto retraso en el crecimiento produciría CP‑506.
Qué tan bien funcionó el modelo de imagen
El modelo fundacional superó claramente tanto a la radiómica tradicional como a una red profunda estándar entrenada desde cero. En exploraciones de prueba nuevas, distinguió tumores HRD de no-HRD con un área bajo la curva de aproximadamente 0,88, un nivel de precisión que se mantuvo a través de diferentes ajustes de energía de la TC. Cuando ambos enfoques de IA coincidían en el tipo de tumor, el rendimiento aumentaba aún más. La puntuación de HRD basada en imagen que dio el modelo se correspondió estrechamente con el estado genético real en varias líneas tumorales de próstata y colorrectales, aunque una línea con un comportamiento de reparación inusual fue más difícil de clasificar. Importante: las características de la TC asociadas a HRD no eran meros artefactos estadísticos: también predijeron cuánto daño duradero en el ADN produjo CP‑506 48 horas después del tratamiento y cuánto tiempo tardaron los tumores en volver a crecer hasta cuadruplicar su tamaño en un experimento paralelo.
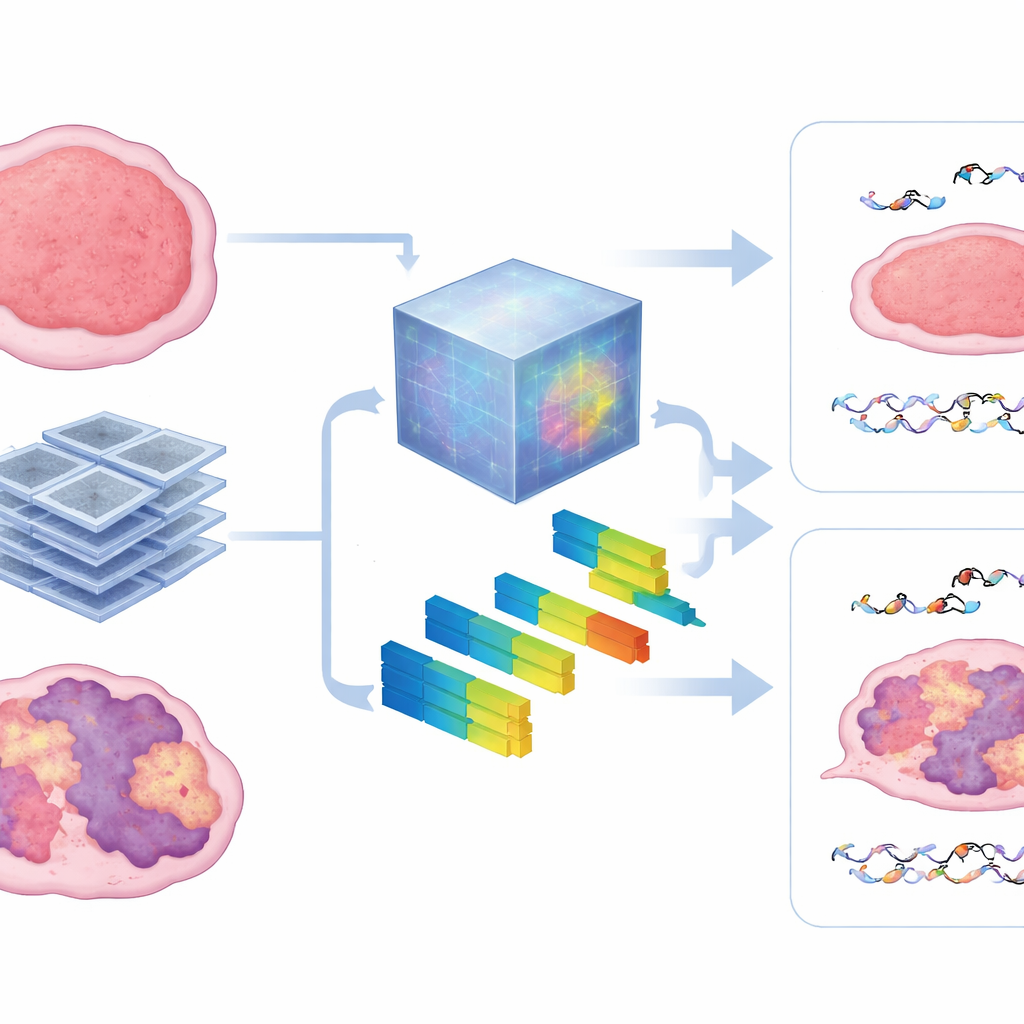
Qué revelan las exploraciones dentro del tumor
Para echar un vistazo dentro de la caja negra, los autores compararon los patrones aprendidos por el modelo fundacional con características radiómicas estándar que describen la textura y la intensidad de la imagen. Encontraron que el modelo se apoyaba en gran medida en medidas de heterogeneidad—qué tan parcheado, tosco o irregular se veía el tumor en la TC. Los tumores con firmas de HRD más fuertes tendían a mostrar texturas más desorganizadas, y esas mismas características ayudaron a predecir tanto el daño microscópico del ADN como el control macroscópico del tumor. El enfoque se mantuvo robusto cuando había menos datos de entrenamiento disponibles, lo que sugiere que tales modelos preentrenados pueden superar un obstáculo importante en estudios animales, donde recopilar grandes conjuntos de imágenes es difícil.
De experimentos en ratones a la atención futura del paciente
Este trabajo preclínico muestra que una sola TC, interpretada mediante una IA potente y preentrenada, puede captar señales de reparación defectuosa del ADN y anticipar con qué intensidad responderá un tumor a un fármaco que daña el ADN. Para un lector no especializado, la conclusión es que exploraciones de aspecto estándar podrían pronto cumplir una doble función: localizar un tumor y revelar cuán frágil es—sin procedimientos adicionales. Antes de que esto forme parte de la práctica clínica rutinaria, el método debe probarse y validarse en pacientes humanos. Si esos esfuerzos tienen éxito, las huellas digitales de HRD basadas en TC podrían ayudar a los médicos a asignar tratamientos como CP‑506 y terapias relacionadas con mayor precisión, mejorando los resultados mientras se evita exponer a otros a fármacos ineficaces y tóxicos.
Cita: Kuang, S., Schuitmaker, L., Wu, M. et al. Predicting homologous recombination deficiency and treatment responses using a computed tomography-based foundation model: a preclinical study. npj Precis. Onc. 10, 121 (2026). https://doi.org/10.1038/s41698-026-01322-3
Palabras clave: deficiencia de recombinación homóloga, imágenes oncológicas, radiómica, modelos fundacionales, terapia que daña el ADN