Clear Sky Science · es
Desarrollo y validación de un modelo basado en inteligencia artificial para diagnosticar masas anexiales benignas, borderline y malignas
Por qué esto importa para la salud de las mujeres
Las masas ováricas y otras masas anexiales son hallazgos frecuentes en la ecografía pélvica, pero decidir cuáles son inofensivas y cuáles indican un cáncer incipiente sigue siendo difícil, incluso para expertos. Este estudio presenta un nuevo sistema de inteligencia artificial (IA), llamado Clinical‑OMTA, que interpreta imágenes ecográficas y ayuda a los médicos a clasificar estas masas en tres grupos clave —benignas, borderline y malignas— para que las mujeres reciban el tratamiento adecuado evitando cirugías innecesarias.
Tres tipos de crecimientos, tres decisiones muy distintas
No todas las masas anexiales son iguales. Las lesiones benignas a menudo pueden vigilarse o extirparse con una cirugía sencilla. Los tumores malignos son cánceres potencialmente mortales que requieren cirugía especializada y quimioterapia. Los tumores borderline quedan en un término medio: pueden recurrir pero suelen afectar a mujeres más jóvenes que desean conservar la fertilidad, por lo que los cirujanos intentan resecar sólo lo necesario. Desgraciadamente, en la ecografía estas tres categorías pueden parecer muy similares. Los tumores borderline en particular pueden imitar tanto a un quiste benigno como a un cáncer agresivo, lo que hace que la toma de decisiones sea estresante para pacientes y clínicos por igual.
Convertir exploraciones complejas en respuestas más claras
La ecografía suele ser la primera y más accesible prueba para las masas anexiales, pero interpretar imágenes granuladas y muy variables exige mucha experiencia. Los sistemas de puntuación y calculadoras de riesgo existentes, como el modelo ADNEX muy utilizado, combinan características ecográficas específicas con información clínica sencilla como la edad y un marcador sanguíneo (CA125), pero siguen dependiendo de que los observadores humanos describan correctamente las imágenes. Trabajos recientes en aprendizaje profundo —una rama de la IA que aprende patrones directamente de los píxeles— ofrecen la posibilidad de sortear cierta subjetividad entrenando a los ordenadores para reconocer firmas sutiles en la imagen propias de distintos tipos tumorales.
Un asistente de IA entrenado en muchos hospitales
Partiendo de trabajos previos, los autores diseñaron Clinical‑OMTA, un modelo de IA de doble vía que primero separa las masas benignas de las no benignas y luego diferencia las borderline de las malignas. El sistema procesa imágenes ecográficas en escala de grises y también puede aceptar la edad y los valores de CA125 como entradas opcionales. Para enseñar y probar el modelo, el equipo reunió un conjunto de datos grande y diverso: 2381 mujeres de 23 hospitales en toda China, exploradas con 38 tipos de ecógrafos. La mayoría de los casos contó con confirmación quirúrgica del diagnóstico; un grupo menor de quistes claramente benignos se confirmó mediante al menos seis meses de seguimiento ecográfico. Los datos se dividieron en conjuntos de entrenamiento, pruebas internas y dos cohortes externas totalmente independientes, que incluyeron tanto imágenes fijas como barridos de vídeo cortos de los ovarios. 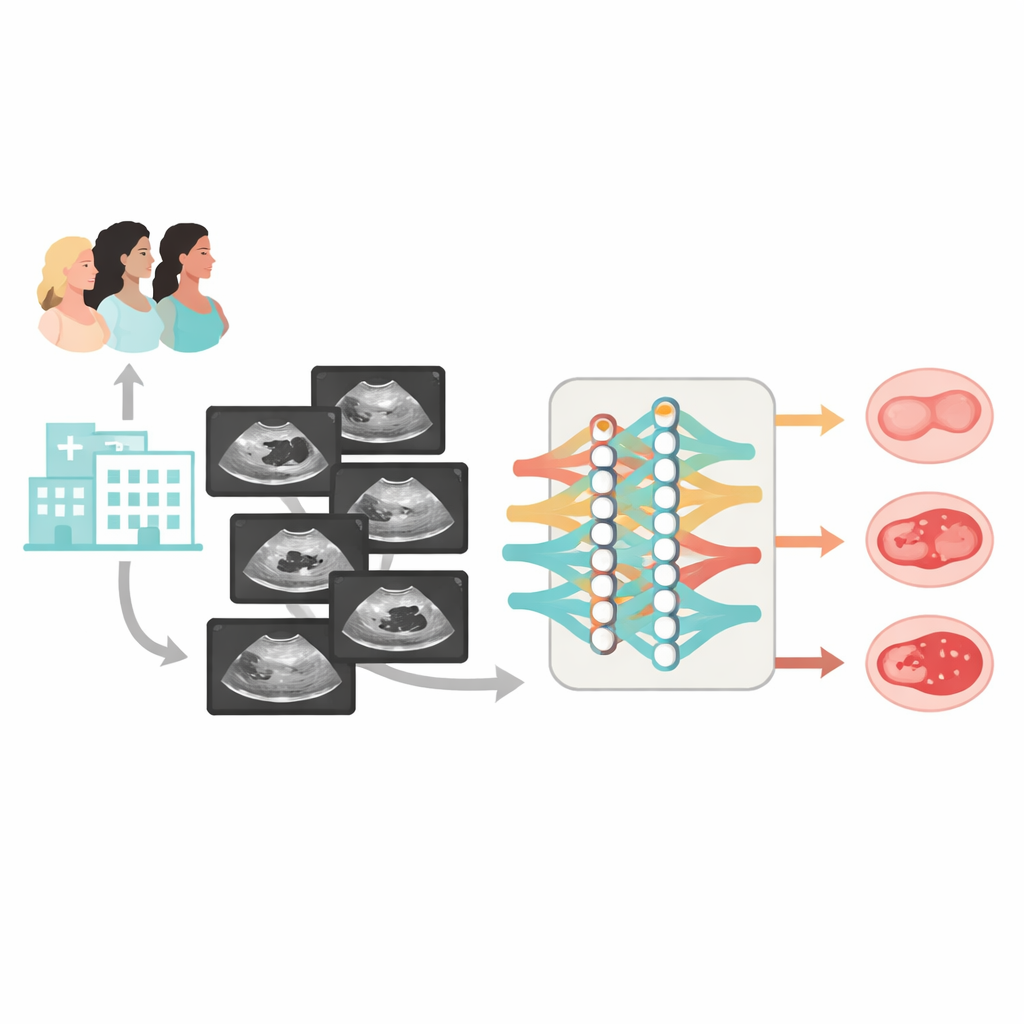
Cómo se comportó la IA en entornos reales
En las imágenes de prueba externas, Clinical‑OMTA separó correctamente las masas benignas, borderline y malignas con una precisión similar tanto al modelo ADNEX como al criterio de un examinador ecográfico experto. Su rendimiento fue estable entre distintas marcas de ecógrafos, métodos de exploración (abdominal o transvaginal) y los dos hospitales externos, lo que sugiere que el modelo no está sobreadaptado a un dispositivo o centro concreto. El sistema también funcionó bien con clips de vídeo, no solo con fotogramas fijos. Curiosamente, introducir la edad y el CA125 no mejoró sus decisiones respecto al uso exclusivo de las imágenes ecográficas, lo que coincide con estudios previos que muestran que este marcador sanguíneo aporta poco cuando existe imagen de alta calidad. 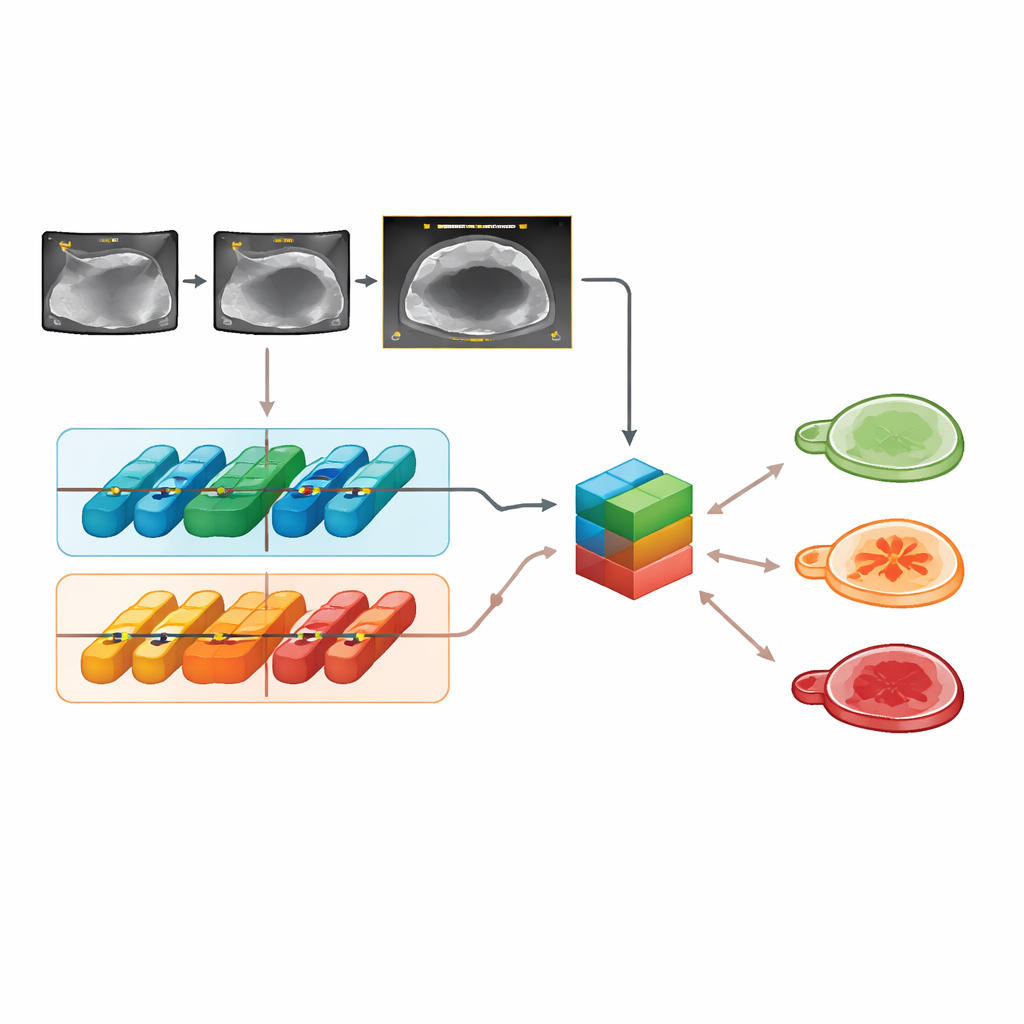
Ayudando a médicos menos experimentados, y sus límites
Los investigadores pidieron después a 11 radiólogos —junior, intermedios y muy experimentados— que clasificaran los mismos casos, primero sin ayuda y luego con la salida de la IA y mapas de calor que resaltan las regiones de la imagen que el modelo considera importantes. Con la ayuda de Clinical‑OMTA, la precisión de los médicos junior aumentó en aproximadamente 18–20 puntos porcentuales, y los lectores intermedios también mejoraron notablemente, alcanzando un rendimiento cercano al de los expertos. La concordancia entre lectores, que antes variaba de justa a moderada, se elevó a niveles muy altos cuando utilizaron la herramienta. Al mismo tiempo, el estudio señala que esa fuerte alineación puede reflejar un “sesgo de automatización”, en el que los clínicos confían en exceso en la IA, particularmente en los casos más ambiguos y borderline. Los autores insisten, por tanto, en que los mapas de calor son herramientas de investigación, no explicaciones autónomas, y que la orientación de la IA debe integrarse con cuidado en la formación clínica y la toma de decisiones.
Qué significa esto para las pacientes
En conjunto, Clinical‑OMTA demuestra que un sistema de IA entrenado con datos ecográficos diversos puede igualar el rendimiento de expertos al clasificar masas anexiales en categorías benignas, borderline y malignas, al tiempo que mejora sustancialmente las habilidades y la consistencia de radiólogos menos experimentados. Debido a que funciona en distintos aparatos y centros, el modelo podría eventualmente integrarse en escáneres o usarse como software independiente para apoyar a los médicos en clínicas con alta carga o recursos limitados. Los autores advierten que hacen falta más estudios prospectivos e internacionales antes de su uso rutinario, especialmente en entornos con equipos de gama baja o operadores no especialistas. Aun así, su trabajo apunta hacia un futuro en el que más mujeres, independientemente de dónde sean atendidas, puedan beneficiarse de una interpretación de nivel experto de las ecografías ováricas y de una atención más personalizada y oportuna.
Cita: Wu, Y., Dai, W., Li, X. et al. Development and validation of an artificial intelligence-based model for diagnosing benign, borderline, and malignant adnexal masses. npj Precis. Onc. 10, 106 (2026). https://doi.org/10.1038/s41698-026-01320-5
Palabras clave: ecografía ovárica, inteligencia artificial, masas anexiales, tumores ováricos borderline, apoyo a la decisión clínica