Clear Sky Science · es
La siguiente capa: aumentar los modelos base con aprendizaje que preserva la estructura y guía por atención para la conciencia del contexto local a global en patología computacional
Enseñar a los ordenadores a leer preparaciones de cáncer
Cuando un patólogo examina una biopsia de cáncer al microscopio, no se limita a observar células individuales: presta atención a patrones, vecindarios y a cómo se disponen en conjunto el tumor, las células inmunitarias y el tejido normal. Los sistemas de inteligencia artificial actuales para la patología digital son muy buenos detectando detalles en pequeños fragmentos de imagen, pero con frecuencia pasan por alto esta perspectiva más amplia. Este estudio presenta EAGLE-Net, un nuevo enfoque de IA que ayuda a los ordenadores a ver las preparaciones de cáncer de forma más parecida a los expertos humanos, prestando atención tanto a los detalles locales como a la disposición global del tejido en la laminilla.

Por qué importa la disposición del tejido tumoral
Un tumor es más que un conjunto de células cancerosas. Vive en un vecindario complejo lleno de vasos sanguíneos, células inmunitarias, tejido conectivo y zonas de cicatrización o muerte celular. Cómo se organizan estos elementos—sus distancias, límites y mezclas—puede indicar cuán agresivo es el cáncer y cómo podría responder el paciente al tratamiento. Los sistemas convencionales de IA en patología suelen dividir una imagen de laminilla completa en miles de pequeños mosaicos y analizarlos casi de forma aislada. Luego intentan inferir el diagnóstico o el resultado del paciente agrupando la información de todos los mosaicos. Esta estrategia suele ignorar cómo se relacionan espacialmente los mosaicos entre sí, lo que puede debilitar las predicciones y hacer que los mapas de atención de la IA parezcan dispersos o difíciles de interpretar.
Una nueva forma de capturar la perspectiva global
EAGLE-Net está diseñado para salvar esa brecha entre el detalle local y la estructura global. Parte de potentes “modelos base” que ya saben extraer características visuales ricas de pequeños parches de la laminilla. Sobre eso añade un módulo nuevo que codifica de dónde proviene cada parche en la laminilla, preservando la geometría real del tejido en lugar de forzarla en una cuadrícula distorsionada. Utilizando filtros a varias escalas, EAGLE-Net aprende patrones que abarcan desde cambios a nivel celular hasta estructuras tisulares más amplias, como los bordes del tumor y el estroma circundante. Luego emplea un mecanismo de atención—esencialmente una forma de asignar puntuaciones de importancia—para centrarse en los parches y vecindarios más relevantes para predecir el diagnóstico o la supervivencia.
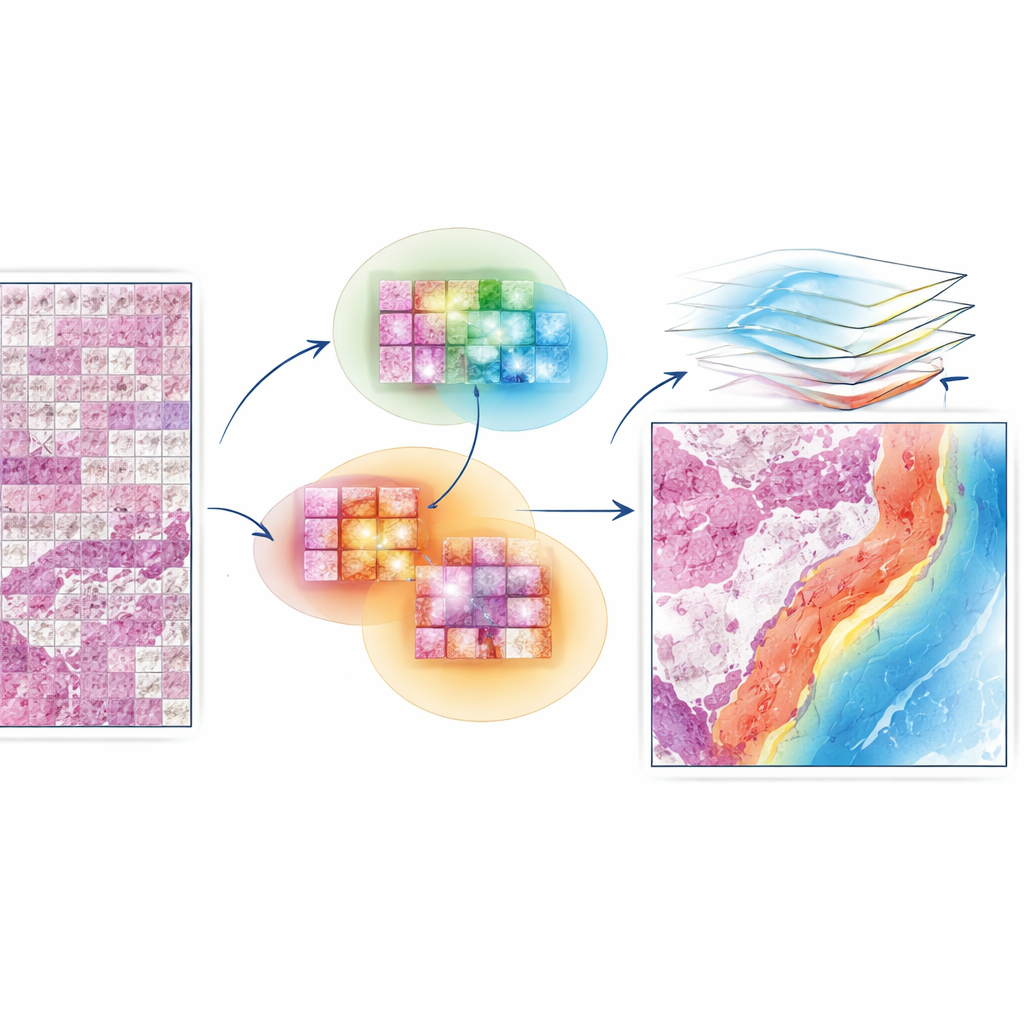
Permitir que el modelo aprenda de vecindarios, no solo de puntos
Una innovación clave de EAGLE-Net es cómo enseña a la red a valorar no solo los mosaicos más informativos sino también sus vecinos cercanos. Durante el entrenamiento, el método identifica repetidamente los mosaicos que el modelo considera más informativos y luego lo anima a considerar los mosaicos circundantes dentro de un pequeño radio como parte de la misma región significativa. Este aprendizaje “con conciencia de vecindario” empuja al modelo a formar regiones de atención suaves y contiguas que se alinean con la forma en que los patólogos ven los frentes tumorales, los cúmulos inmunitarios y otros microambientes. Al mismo tiempo, un término adicional en el proceso de entrenamiento impulsa activamente al modelo a ignorar áreas de fondo o vacías, reduciendo el riesgo de resaltar falsamente artefactos o zonas en blanco.
Demostrar su valor en muchos tipos de cáncer
Los investigadores probaron EAGLE-Net en casi 15.000 imágenes de laminillas completas que abarcan 10 tipos de cáncer diferentes, incluidos tumores de pulmón, riñón, estómago, útero, tiroides, colorrectales y de próstata. Evaluaron dos tareas principales: predecir la supervivencia de los pacientes y clasificar tipos o grados tumorales. En la mayoría de las cohortes, EAGLE-Net igualó o superó a varios métodos líderes basados en atención, mejorando a menudo las puntuaciones de predicción de supervivencia y la precisión de clasificación en varios puntos porcentuales, lo cual es significativo a escala poblacional. También mostró un buen rendimiento cuando se emparejó con tres modelos base subyacentes muy diferentes, lo que demuestra que su diseño es flexible y no depende de un único extractor de características.
Ver el razonamiento interno del modelo
Más allá de la precisión bruta, el equipo examinó con cuidado dónde “miró” EAGLE-Net en las laminillas. En comparación con otros métodos, sus mapas de atención formaron regiones más suaves y coherentes que seguían los límites tumorales y capturaban bordes invasivos, bolsillos necróticos y cúmulos de células inmunitarias. Las comparaciones cuantitativas con máscaras tumorales trazadas por expertos mostraron que las regiones resaltadas por EAGLE-Net se solapaban mejor con el tumor verdadero, hicieron menos falsos positivos sobre tejido normal y reprodujeron con mayor fidelidad formas tumorales complejas. El modelo también dedicó una mayor proporción de su atención al tumor, la necrosis y los compartimentos inmunitarios, y menos a tejido pulmonar normal o vasos sanguíneos, reflejando lo que un patólogo priorizaría al evaluar el pronóstico.
Qué significa esto para la atención del cáncer en el futuro
En términos prácticos, EAGLE-Net demuestra que añadir conciencia espacial y razonamiento por vecindarios sobre la IA patológica existente puede mejorar tanto el rendimiento como la interpretabilidad. En lugar de tratar una laminilla como una bolsa de mosaicos desconectados, el método aprende a reconocer nichos biológicamente relevantes—bordes tumorales, regiones ricas en células inmunitarias y patrones de invasión—que son importantes para los resultados de los pacientes. Dado que funciona con distintos modelos base y no requiere etiquetado a nivel de píxel que demande mucho trabajo, EAGLE-Net podría aplicarse ampliamente a grandes archivos de laminillas digitales. Con más validación e integración en los flujos de trabajo clínicos, estos sistemas podrían ayudar a los patólogos a estratificar a los pacientes con mayor precisión, descubrir nuevos biomarcadores tisulares y, en última instancia, orientar tratamientos oncológicos más personalizados.
Cita: Waqas, M., Bandyopadhyay, R., Showkatian, E. et al. The next layer: augmenting foundation models with structure-preserving and attention-guided learning for local patches to global context awareness in computational pathology. npj Precis. Onc. 10, 109 (2026). https://doi.org/10.1038/s41698-026-01312-5
Palabras clave: patología computacional, pronóstico del cáncer, IA en patología digital, microambiente tumoral, EAGLE-Net