Clear Sky Science · es
Análisis a gran escala de células individuales y perturbación in silico revelan la evolución dinámica del CHC: desde la iniciación hasta la diana terapéutica
Por qué importa la vida interna del cáncer de hígado
El carcinoma hepatocelular, la forma más frecuente de cáncer de hígado, es notoriamente difícil de tratar. Muchos pacientes no responden bien a los fármacos actuales, y los tumores con frecuencia reaparecen o hacen metástasis. Una razón importante es que cada tumor es una mezcla caótica de células distintas que evolucionan con el tiempo y mantienen una comunicación constante con su entorno. Este estudio emplea potentes tecnologías de lectura genética unicelular y espacial para observar esa evolución en acción, célula por célula, desde el crecimiento tumoral temprano hasta la enfermedad avanzada y resistente al tratamiento, y para identificar puntos débiles que podrían aprovechar nuevas terapias.
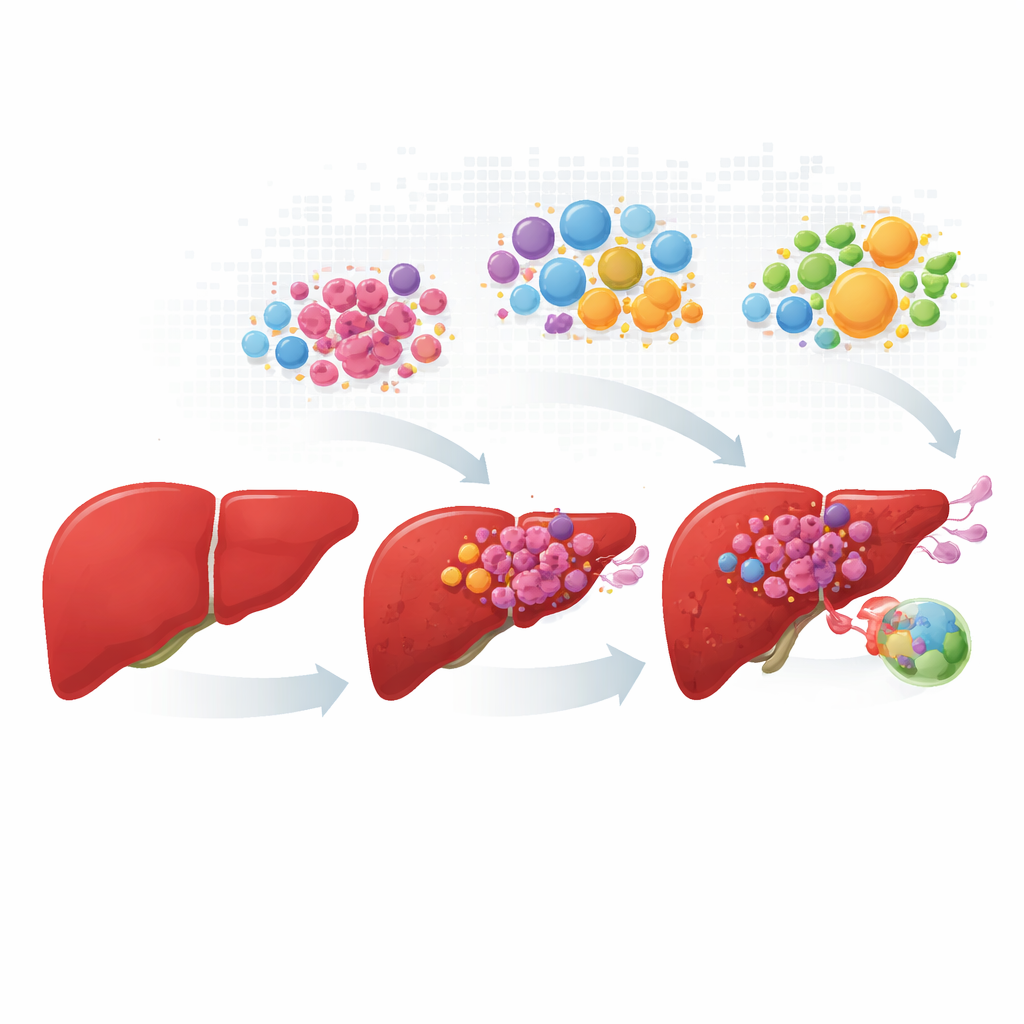
Siguiendo a las células cancerosas desde el cambio inicial hasta la diseminación
Los investigadores reunieron y armonizaron datos de más de un centenar de pacientes, abarcando hígado normal, tumores primarios, crecimientos en vasos sanguíneos y metástasis en ganglios linfáticos. En lugar de tratar cada tumor como una masa uniforme, caracterizaron cientos de miles de células individuales y luego cartografiaron dónde se ubicaban esas células en cortes de tejido reales. Las células hepáticas cancerosas se agruparon en cuatro “personalidades” recurrentes. Un grupo conservaba muchas funciones hepáticas normales y tareas metabólicas; los otros tres mostraban crecimiento impulsado por el estrés, alta actividad de la vía de crecimiento MYC, o un comportamiento invasivo vinculado a la inflamación. Estos cuatro estados aparecieron en proporciones diferentes a medida que la enfermedad progresaba, con células de crecimiento rápido e invasivas dominando en lesiones vasculares y en ganglios linfáticos.
Cuatro personalidades tumorales con distintos destinos
Los cuatro estados celulares del cáncer no fueron solo categorías académicas; se correlacionaron con el pronóstico de los pacientes. Los tumores ricos en el estado similar al hígado y metabólicamente activo se asociaron con una mejor supervivencia, mientras que los tumores dominados por los otros tres estados agresivos tendieron a tener peores resultados. Sin embargo, incluso el estado “beneficioso” tenía una vuelta de tuerca: estaba fuertemente enriquecido en pacientes que no se beneficiaron del fármaco para cáncer de hígado sorafenib, probablemente porque estas células conservan maquinaria de desintoxicación que puede inactivar medicamentos. Al reproducir cómo las células se desplazan a lo largo de trayectorias de desarrollo, el equipo mostró que las células invasivas e inflamatorias pueden ramificarse hacia estados más diferenciados o hacia estados más prolíferos, lo que sugiere que las células tumorales pueden cambiar de identidad y, potencialmente, escapar de terapias dirigidas a un único estado.
El reparto de apoyo: cómplices inmunes y estromales
Las células cancerosas no actúan solas. El estudio descubrió células inmunitarias especializadas y células de soporte que o bien combaten el tumor o bien lo ayudan en silencio. Entre los macrófagos, los recicladores y centinelas del tejido, algunos tipos produjeron señales inflamatorias que pueden favorecer la inmunidad antitumoral, mientras que otros estaban reprogramados metabólicamente, suprimían señales útiles y promovían el crecimiento vascular y la invasión. Estos macrófagos “malos” se expandieron en muestras avanzadas. De modo similar, ciertos tipos de células endoteliales que recubren los vasos y fibroblastos que forman tejido conectivo constituyeron subconjuntos ligados a un mal pronóstico. En la enfermedad avanzada, un subtipo endotelial particular y dos tipos de fibroblastos crearon nodos estrechamente conectados que remodelaron la matriz extracelular, alimentaron la formación de nuevos vasos sanguíneos y se correlacionaron con los estados celulares tumorales más agresivos.
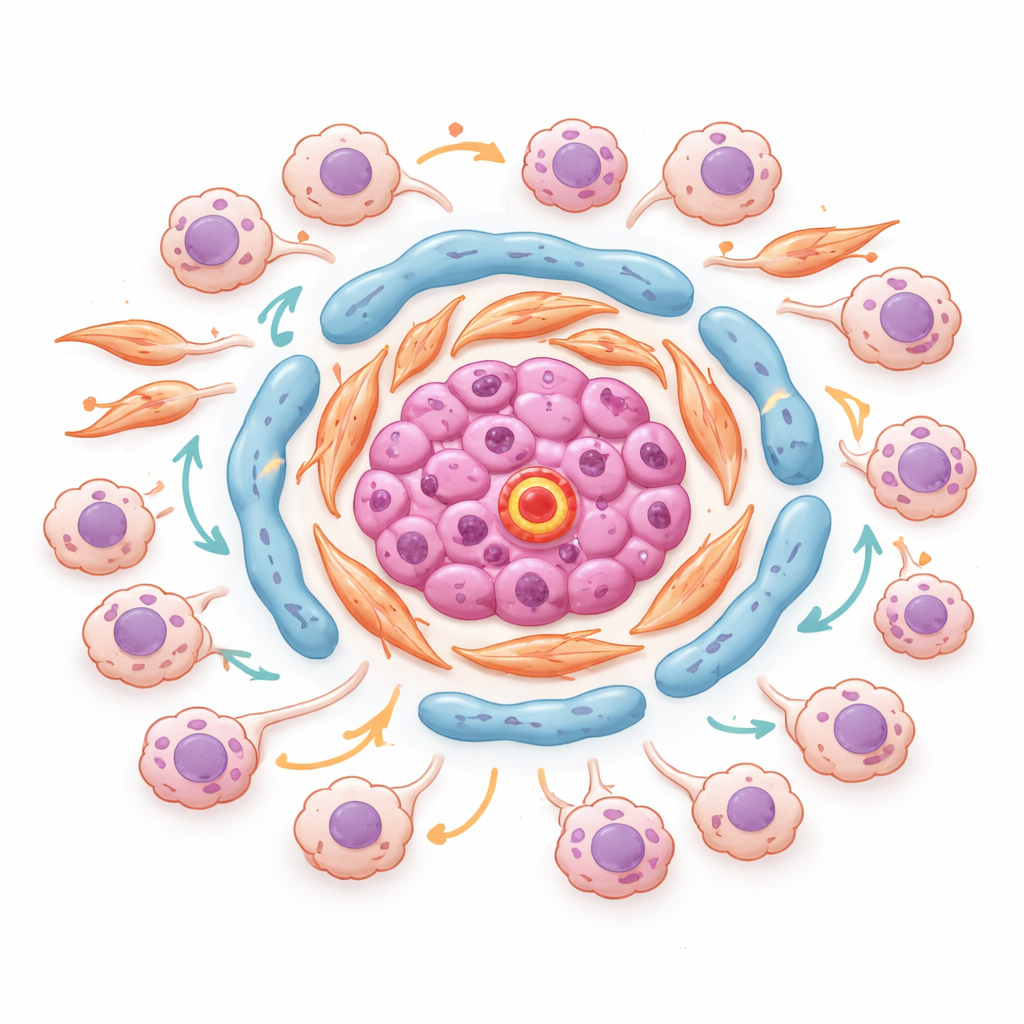
Detectando barrios peligrosos dentro de los tumores
Utilizando transcriptómica espacial, que mide la actividad génica sin perder el mapa de la ubicación de cada punto en el tejido, los autores identificaron “barrios” organizados dentro de los tumores. En un tumor representativo, las células endoteliales ricas en una molécula llamada ESM1 se agruparon con fibroblastos productores de matriz y ávidos de lípidos en el núcleo de islas estromales. Alrededor de estos núcleos se acumulaban células cancerosas impulsadas por el estrés y células invasivas, en regiones con señales fuertes de TGF‑beta y bajo oxígeno. Factores de transcripción clave que controlan cómo las células responden al estrés y a la inflamación estaban compartidos entre estos estados cancerosos y eran más activos justamente donde las células tumorales tocaban estos nodos estromales. Esto sugiere que micro-nichos específicos en los bordes tumor‑estroma fomentan activamente que las células cancerosas cambien de estado, se vuelvan más agresivas y resistan la terapia.
Encontrando un punto débil compartido para nuevas terapias
Para pasar de la descripción a la intervención, el equipo utilizó un modelo de aprendizaje automático entrenado con millones de células para simular “anulaciones virtuales” de genes y predecir qué cambios podrían empujar a las células dañinas hacia estados más saludables. Comparando macrófagos, células endoteliales y células cancerosas, encontraron un pequeño conjunto de genes cuya eliminación ayudaba a normalizar los tres tipos. Entre ellos destacó HSP90B1: las líneas celulares cancerosas dependen en gran medida de él, está sobreexpresado en tumores hepáticos, especialmente en aquellos que resisten fármacos dirigidos e inmunoterapia, y niveles altos predicen una supervivencia peor. HSP90B1 codifica una chaperona encargada del manejo del estrés en la fábrica celular de plegado de proteínas que soporta muchos receptores de superficie y vías de señalización. Dado que ya existen fármacos selectivos contra esta chaperona que también pueden remodelar el entorno inmunitario, el estudio propone a HSP90B1 como una diana prometedora para vencer la resistencia, especialmente en combinación con los tratamientos actuales para el cáncer de hígado.
Qué significa esto para pacientes y terapias
En conjunto, este trabajo demuestra que el cáncer de hígado no es una sola enfermedad sino un ecosistema dinámico de estados celulares y nichos que cambian conforme el tumor crece y se disemina. Al vincular personalidades celulares tumorales específicas, células de soporte y barrios espaciales con el resultado del paciente y la respuesta a fármacos, el estudio ofrece una hoja de ruta para tratamientos más precisos: adaptar las terapias a los estados celulares dominantes, interrumpir los nodos estromales que cultivan comportamientos agresivos y dirigir dependencias compartidas como HSP90B1 de las que dependen muchas células tumorales y del microambiente. Aunque se necesitan más pruebas en laboratorio y en ensayos clínicos, el atlas que construyó este equipo proporciona un plano detallado para convertir la complejidad interna del tumor en una oportunidad para terapias hepáticas más inteligentes y duraderas.
Cita: Xia, P., Shuang, S., Fu, D. et al. Large-scale single-cell analysis and in silico perturbation reveal dynamic evolution of HCC: from initiation to therapeutic targeting. npj Precis. Onc. 10, 100 (2026). https://doi.org/10.1038/s41698-026-01307-2
Palabras clave: carcinoma hepatocelular, análisis unicelular, microambiente tumoral, transcriptómica espacial, HSP90B1