Clear Sky Science · es
Diversidad clonotípica y especialización de los receptores de células T en cánceres del sistema digestivo
Por qué esta investigación importa para los pacientes con cáncer
La inmunoterapia contra el cáncer ha transformado el tratamiento de muchas personas, pero no funciona por igual en todos los casos. Este estudio examina en profundidad las “huellas” de las células inmunitarias—los receptores de células T—dentro de los tumores del sistema digestivo, incluidos los cánceres colorrectal y gástrico. Al leer estas huellas a gran escala, los investigadores muestran cómo el sistema inmune reconoce los tumores, cómo difiere ese reconocimiento entre tipos de cáncer y cómo cambia cuando el cáncer colorrectal hace metástasis. Estos hallazgos podrían ayudar a los médicos a predecir mejor los resultados y a diseñar inmunoterapias más precisas y personalizadas.
La huella del sistema inmune dentro de los tumores
Las células T son los defensores dirigidos del organismo, cada una con un receptor único que le permite reconocer células anómalas específicas, incluidos los cánceres. El equipo secuenció receptores de células T de 415 muestras tumorales tomadas de 145 pacientes con cáncer colorrectal, gástrico y de hígado, y combinó estos datos con información clínica detallada. Examinaron varias cadenas de receptores que definen dos familias clave de células T: las convencionales αβ, que impulsan la mayoría de las respuestas inmunitarias adaptativas, y las γδ, que actúan más como centinelas de respuesta rápida. Encontraron que las células T αβ tendían a formar clones grandes y muy variados, mientras que las γδ conformaban grupos más pequeños y especializados. Los pacientes con enfermedad más avanzada, invasión vascular o diseminación a distancia presentaron patrones de receptores de células T más complejos, lo que sugiere que la progresión tumoral empuja al sistema inmune a una contienda más amplia y complicada.
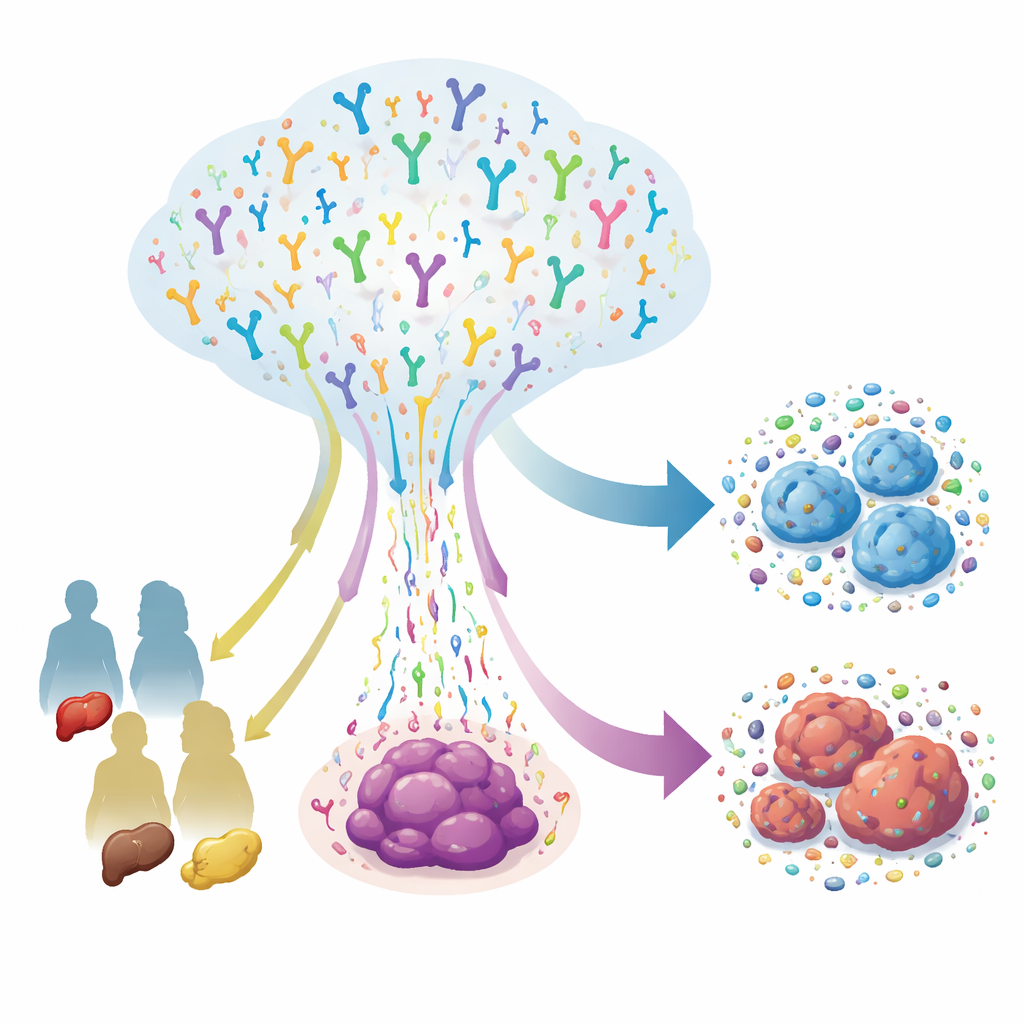
Diferentes cánceres, distintas estrategias inmunitarias
Aunque estos tumores se originan en el sistema digestivo, no atraen ni modelan las células T de la misma manera. Los cánceres colorrectales mostraron un enriquecimiento de combinaciones particulares de segmentos génicos del receptor en la cadena β clásica, lo que apunta a un papel destacado de las células T convencionales. Los cánceres gástricos, en cambio, mostraron un uso más intenso de receptores de células T γδ, lo que sugiere que estos centinelas menos estudiados pueden desempeñar un papel especial en los tumores de estómago. Cuando los investigadores se centraron en la parte más crítica del receptor—el bucle corto que contacta los objetivos—encontraron patrones de secuencia compartidos entre los tipos de cáncer, señales de que las células T están siendo guiadas por presiones selectivas comunes. No obstante, también hubo diferencias claras en la longitud, la composición aminoacídica y pequeños “motivos” recurrentes que indican que cada tipo tumoral obliga a las células T a resolver un rompecabezas de reconocimiento ligeramente distinto.
Objetivos compartidos y únicos para el ataque inmune
Usando una base de datos global de pares conocidos receptor–antígeno, los autores vincularon patrones específicos de receptores con sus probables dianas. Algunos antígenos aparecieron tanto en cáncer colorrectal como gástrico, incluidos conductores bien conocidos y proteínas relacionadas con la inmunidad como KRAS, SF3B1, BST2 y varios antígenos clásicos cancer-testis. Estos objetivos compartidos podrían respaldar estrategias “pan-cáncer” que utilicen las mismas herramientas inmunitarias en varios tipos tumorales. Al mismo tiempo, cada tipo de cáncer mostró también dianas propias. Los tumores colorrectales se asociaron con antígenos como MAGEA10, WT1 y una fusión génica encontrada solo en células cancerosas, mientras que los tumores gástricos presentaron de forma exclusiva PABPC1, una proteína implicada en el control del ARN mensajero. Tales antígenos específicos del tumor son candidatos atractivos para vacunas altamente selectivas o terapias con células T diseñadas que preserven los tejidos sanos.
Cómo cambian las firmas inmunes cuando el cáncer hace metástasis
El estudio prestó especial atención al cáncer colorrectal que ya había metastatizado, comparando tumores de pacientes con y sin diseminación a distancia. Los tumores metastásicos eran más grandes, con mayor probabilidad de invadir vasos sanguíneos y mostraban niveles séricos más altos de marcadores tumorales estándar. Sus repertorios de receptores de células T también eran más ricos y complejos, especialmente en la cadena β, coherente con una contienda inmune más dura y variada. Al rastrear clones compartidos entre entornos no metastásicos y metastásicos, los investigadores los agruparon en poblaciones estables, en reducción o en expansión. Un hallazgo notable fue que algunos clones de células T γδ, inicialmente raros en los tumores primarios, se expandieron fuertemente en la enfermedad metastásica y se volvieron más numerosos a medida que los tumores crecían. Dentro de las células T convencionales, un conjunto particularmente expandido de clones portaba un motivo de secuencia específico en la cadena β y con frecuencia apuntaba a MLANA, un antígeno asociado a tumores. La alta expresión de MLANA en tumores colorrectales se asoció con una mejor supervivencia de los pacientes, lo que sugiere que este antígeno puede marcar tumores que siguen siendo visibles para el sistema inmune y susceptibles a terapias basadas en la inmunidad.
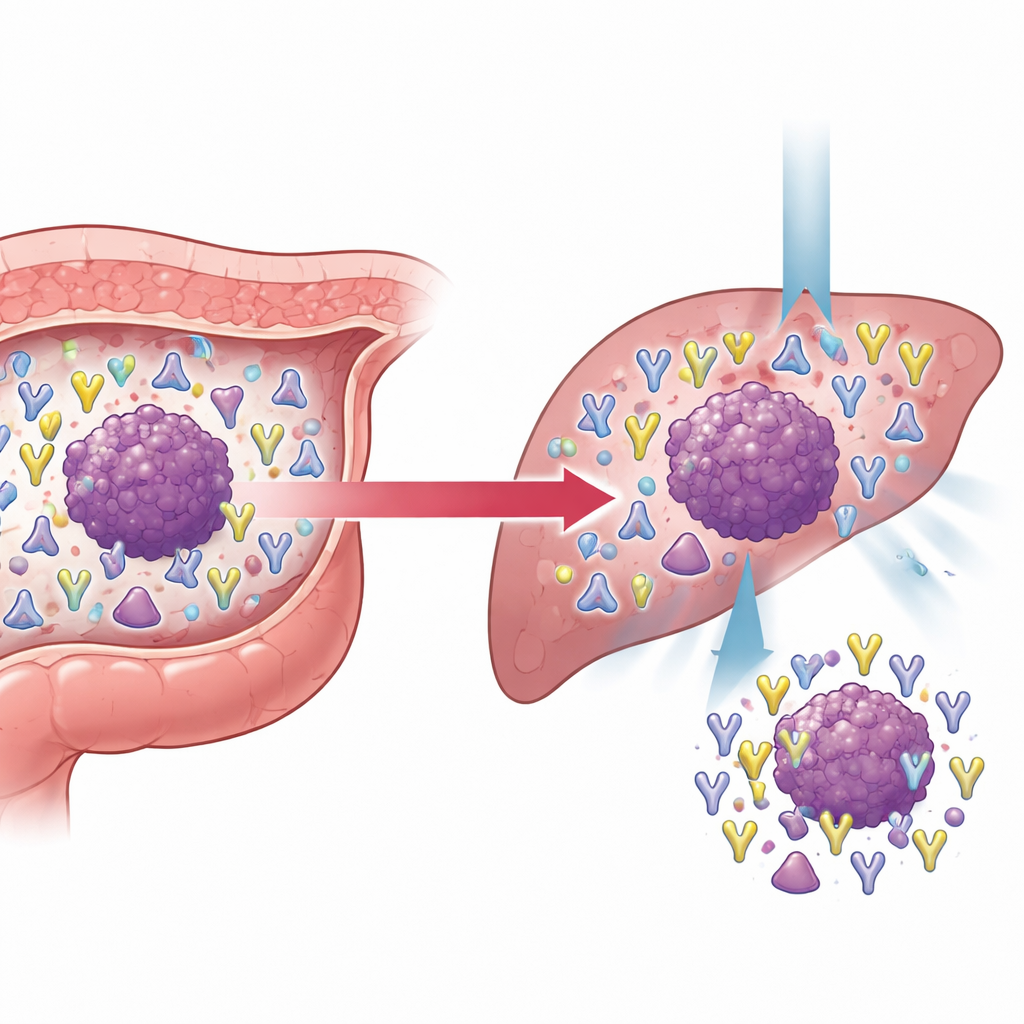
Qué significa esto para la atención oncológica futura
En conjunto, el trabajo demuestra que el paisaje inmunitario dentro de los cánceres del sistema digestivo no es aleatorio sino moldeado por el tipo de cáncer, la etapa y la diseminación. Patrones específicos de receptores de células T actúan como huellas legibles de cómo el sistema inmune se enfrenta al tumor, destacando tanto antígenos compartidos como específicos de cada cáncer. Para los pacientes, esto apunta a un futuro en el que los médicos podrían perfilar los repertorios de receptores de células T a partir de una muestra tumoral para afinar el pronóstico, elegir inmunoterapias con mayor criterio e incluso diseñar tratamientos personalizados que movilicen los clones de células T más eficaces. En el cáncer colorrectal y gástrico, las firmas de receptores y los antígenos identificados aquí ofrecen una hoja de ruta para esfuerzos de inmunoterapia de precisión.
Cita: Li, L., Li, J., Wang, F. et al. T-cell receptor clonotypic diversity and specialization in digestive system cancers. npj Precis. Onc. 10, 91 (2026). https://doi.org/10.1038/s41698-026-01294-4
Palabras clave: Receptores de células T, cáncer colorrectal, cáncer gástrico, inmunidad tumoral, biomarcadores de inmunoterapia