Clear Sky Science · es
Pérdida de microARN-29b favorece la regulación a la baja de STING mediada por DNMT3b para atenuar la inmunidad antitumoral inducida por radioterapia en el cáncer colorrectal con mutación KRAS
Por qué importa esta investigación
Para muchas personas con cáncer de recto y de colon, la radiación es una parte clave del tratamiento antes de la cirugía. Sin embargo, algunos tumores apenas se reducen y el cáncer a menudo reaparece o se disemina. Este estudio examina en detalle un cambio genético frecuente en el cáncer colorrectal —la mutación en KRAS— para explicar por qué estos tumores suelen resistir la radioterapia y las nuevas inmunoterapias, y propone una estrategia para reactivar el propio sistema inmunitario contra ellos.
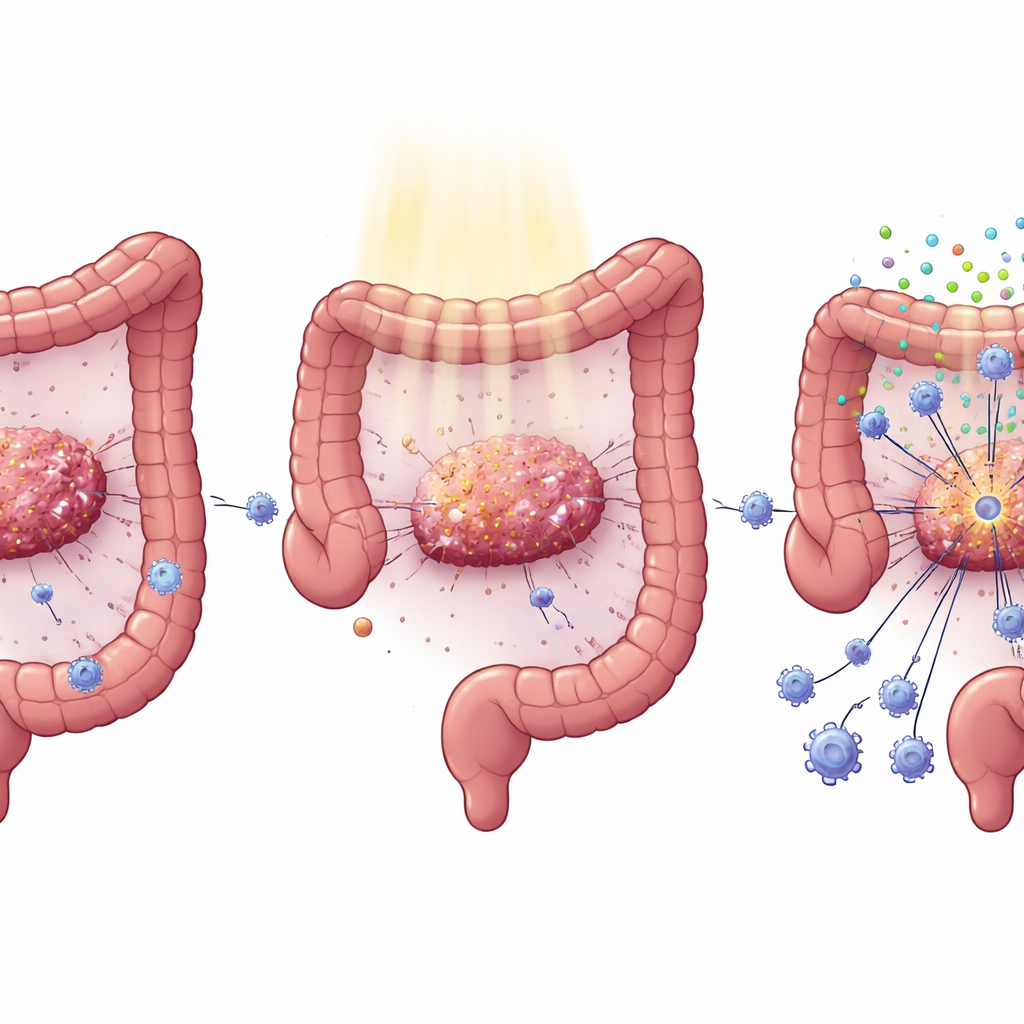
Una mutación común que esconde los tumores del ataque inmunitario
El cáncer colorrectal presenta con frecuencia mutaciones en el gen KRAS, un impulsor principal del crecimiento y la diseminación tumoral. Los clínicos ya habían observado que los tumores con KRAS mutado tienden a responder mal tanto a fármacos dirigidos como a la radioterapia. Al explorar grandes bases de datos de cáncer y analizar muestras de pacientes, los autores hallaron que los tumores con KRAS mutado muestran menos células CD8 citotóxicas y una actividad más débil de las señales interferón que estimulan la inmunidad. En pacientes que recibieron quimiorradioterapia estándar antes de la cirugía por cáncer rectal, aquellos con KRAS normal ganaron muchas más células CD8 dentro de sus tumores tras el tratamiento que los pacientes con mutaciones en KRAS, lo que ayuda a explicar sus mejores resultados.
El sistema de alarma ausente dentro de las células cancerosas
La radioterapia no solo daña el ADN tumoral; también puede actuar como una bengala que hace que las células cancerosas liberen fragmentos de ADN que activan una vía interna de alerta llamada cGAS–STING. Cuando STING está activo, las células producen interferones tipo I y otras señales que atraen y activan células inmunitarias, incluidas células T y células dendríticas. Los investigadores mostraron que en células de cáncer colorrectal modificadas para portar KRAS mutado, este sistema de alarma está atenuado: tras la radiación, estas células produjeron mucho menos interferón y moléculas relacionadas. En ratones, silenciar KRAS en los tumores restauró los niveles de STING, aumentó las señales de interferón y condujo a más células T CD4 y CD8, menos células T reguladoras y un mayor control tumoral; no solo en los tumores irradiados sino también en tumores distantes no irradiados (“abscopales”).
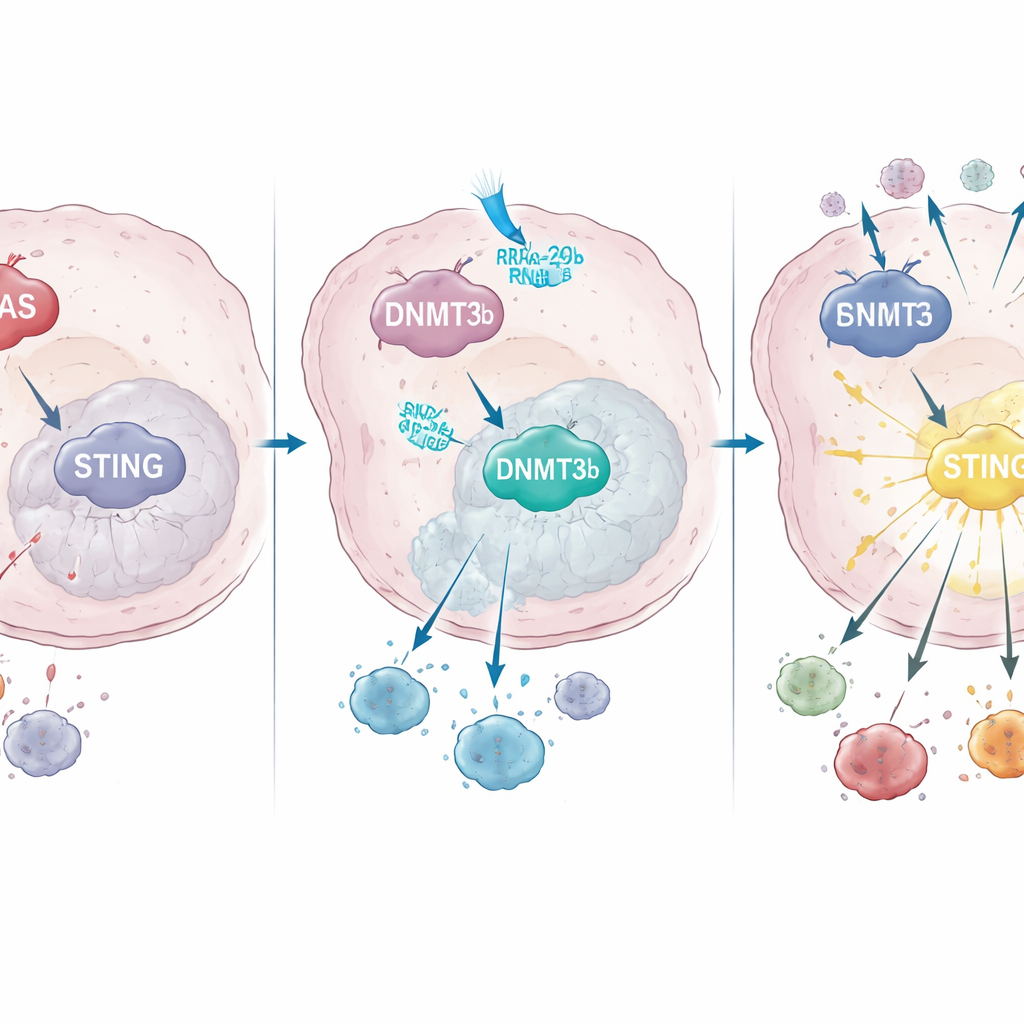
Cómo KRAS reconfigura el control génico para apagar STING
Profundizando, el equipo descubrió que KRAS mutado aumenta la actividad de una enzima modificadora del ADN llamada DNMT3b, que añade grupos metilo a ciertas regiones del ADN y silencia los genes cercanos. Tanto en líneas celulares cancerosas como en muestras de pacientes, altos niveles de DNMT3b se asociaron con bajos niveles de STING. Un tramo clave del promotor de STING —la región del ADN que actúa como interruptor de encendido— estaba fuertemente metilado en tumores con KRAS mutado, pero no en los tumores con KRAS normal. Los pacientes cuyos tumores aún podían aumentar la expresión de STING tras la quimiorradioterapia tuvieron mayor infiltración de células T CD8 y mejor supervivencia, lo que subraya la importancia de esta vía para el éxito del tratamiento.
Un pequeño ARN que puede reactivar la alarma
Los autores se preguntaron entonces qué ocasiona la abundancia de DNMT3b en el cáncer con KRAS mutado. Mediante secuenciación de microARN identificaron un pequeño ARN regulador, microARN‑29b‑3p, que normalmente mantiene a DNMT3b bajo control pero que queda fuertemente suprimido por KRAS mutado. Restaurar este microARN en células KRAS‑mutantes cultivadas redujo DNMT3b, reactivó STING y potenció la producción de interferón tras la radiación; bloquearlo produjo el efecto contrario. En muestras tumorales, los pacientes con KRAS mutado tendían a tener niveles bajos de microARN‑29b‑3p, DNMT3b altos y STING bajo, y aquellos con niveles más altos de microARN‑29b‑3p vivieron más tiempo, enlazando directamente esta cadena molecular con los resultados clínicos.
Un enfoque de entrega génica dirigida que potencia la radioterapia y la inmunoterapia
Para trasladar estos hallazgos a una posible terapia, el equipo diseñó un virus inofensivo (AAV) que entrega microARN‑29b‑3p bajo el control de un promotor activo principalmente en células de cáncer colorrectal. En modelos murinos con tumores colorrectales KRAS‑mutantes, administrar este AAV junto con radioterapia localizada redujo de forma dramática tanto los tumores irradiados como los tumores distantes que no recibieron radiación. Los tumores mostraron menos DNMT3b, más STING, más señales de interferón y una intensa infiltración de células T y otras células inmunitarias. Cuando el mismo tratamiento con microARN‑29b‑3p se combinó con un inhibidor del punto de control inmunitario dirigido a PD‑1, la supervivencia mejoró aún más, y este beneficio dependió de las células T CD8, confirmando que el sistema inmunitario era el principal responsable del efecto.
Qué podría significar esto para los pacientes
En términos sencillos, este estudio revela cómo los cánceres colorrectales con KRAS mutado “cortan el cable” de un sistema de alarma interno que la radiación normalmente activa, permitiéndoles evadir el ataque inmunitario. Al restaurar un único ARN pequeño, microARN‑29b‑3p, los investigadores pudieron reducir DNMT3b, reavivar STING y convertir tumores inmunológicamente “fríos” en “calientes”, que responden mejor tanto a la radioterapia como al bloqueo de puntos de control. Aunque este trabajo sigue en fase preclínica, apunta a tratamientos futuros que combinen radiación con terapia génica dirigida al tumor para superar la resistencia en el cáncer colorrectal con KRAS mutado, potencialmente haciendo que las terapias existentes funcionen para muchos más pacientes.
Cita: Chang, HY., Chen, JY., Ke, TW. et al. Loss of MicroRNA-29b promotes DNMT3b-mediated STING downregulation to attenuate radiotherapy-induced antitumor immunity in KRAS-mutated colorectal cancer. npj Precis. Onc. 10, 93 (2026). https://doi.org/10.1038/s41698-026-01290-8
Palabras clave: Cáncer colorrectal con mutación KRAS, resistencia a la radioterapia, vía STING, microARN-29b, inmunología tumoral