Clear Sky Science · es
Análisis comparativo de estrategias de monitorización de ctDNA en NSCLC avanzado con deleciones del exón 14 de MET tratadas con ensartinib
Por qué importa una prueba de sangre en el cáncer de pulmón
Para las personas con cáncer de pulmón avanzado, una de las mayores preguntas es si un fármaco nuevo realmente funciona —y con qué rapidez pueden saberlo los médicos. Este estudio explora un enfoque basado en sangre, que utiliza pequeños fragmentos de ADN tumoral que circulan en el torrente sanguíneo, para evaluar rápidamente cuánto ayuda un fármaco dirigido llamado ensartinib en pacientes cuyos tumores comparten una alteración genética específica. Los resultados sugieren que una simple prueba sanguínea temprana podría señalar qué pacientes probablemente obtendrán un beneficio prolongado del tratamiento y cuáles pueden necesitar un cambio de estrategia.
Poner las huellas del tumor en un tubo de sangre
Las células cancerosas liberan fragmentos de su material genético en la sangre, conocidos como ADN tumoral circulante. En este ensayo, los investigadores se centraron en personas con cáncer de pulmón no microcítico impulsado por una alteración en un gen llamado MET, específicamente un defecto conocido como deleción (saltos) del exón 14. Todos los pacientes recibieron ensartinib tras el fracaso de tratamientos previos. Se tomaron muestras de sangre justo antes de iniciar el fármaco y de nuevo a las cuatro semanas. Usando una prueba avanzada de secuenciación que explora 229 genes relacionados con el cáncer, el equipo agrupó las alteraciones detectadas en tres categorías: cambios en el propio MET, un conjunto de conductores tumorales bien establecidos y un grupo amplio que incluía cualquier mutación detectable.
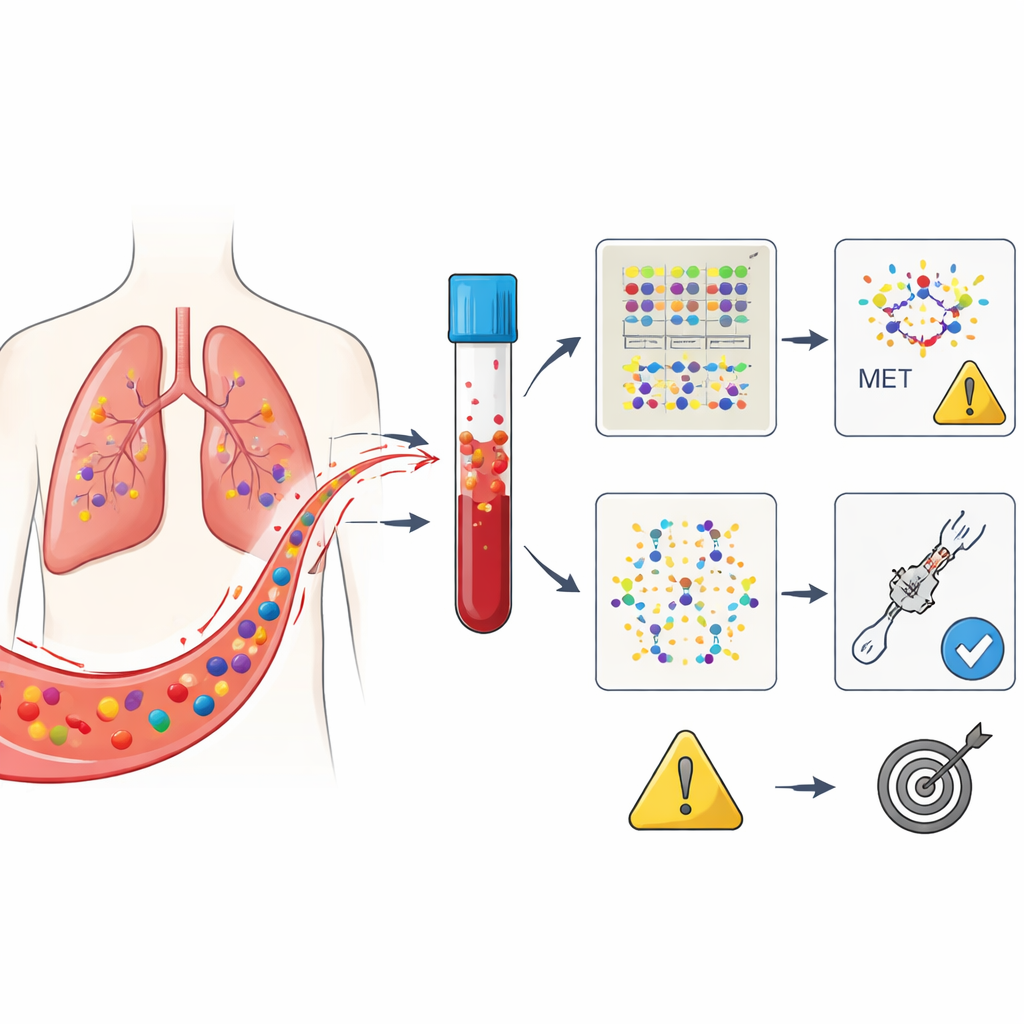
Tres maneras de leer la misma señal en sangre
La pregunta central era cuál de estas tres “vistas” sanguíneas predice mejor quién responderá al ensartinib y cuánto durará esa respuesta. Al inicio, no todos los pacientes tenían ADN tumoral detectable en sangre, a pesar de que sus tumores portaban la alteración en MET; esto refleja lo desigual que puede ser la liberación de ADN por parte de los cánceres. Temprano, el simple hecho de ser positivo o negativo para ADN tumoral en la línea de base no predijo con fuerza el resultado. Sin embargo, en la marca de las cuatro semanas surgió un patrón claro: los pacientes cuya sangre ya no mostraba cambios relacionados con MET tendían a permanecer más tiempo sin empeoramiento de la enfermedad que aquellos en quienes esas señales persistían. Esto fue cierto aun cuando las imágenes tumorales en ese momento podían seguir siendo ambiguas.
Cuando las señales de MET desaparecen, mejoran los resultados
Al observar más de cerca cómo cambiaron los resultados en sangre con el tiempo, el equipo identificó tres trayectorias. Algunos pacientes nunca tuvieron ADN de MET detectable en sangre, otros empezaron positivos y se hicieron negativos, y otros permanecieron positivos o desarrollaron nuevos cambios en MET. Aquellos que eliminaron las señales de MET a las cuatro semanas disfrutaron del intervalo más largo antes de la progresión del cáncer, alrededor de nueve meses de media, y mostraron la mayor tasa de reducción tumoral medible. Los pacientes que permanecieron positivos para ADN de MET lo hicieron mucho peor, con progresión de la enfermedad en poco más de dos meses de media. La monitorización de conjuntos más amplios de mutaciones también proporcionó información útil, pero fue menos precisa porque muchos cambios de bajo nivel o no relacionados podían enturbiar la interpretación.
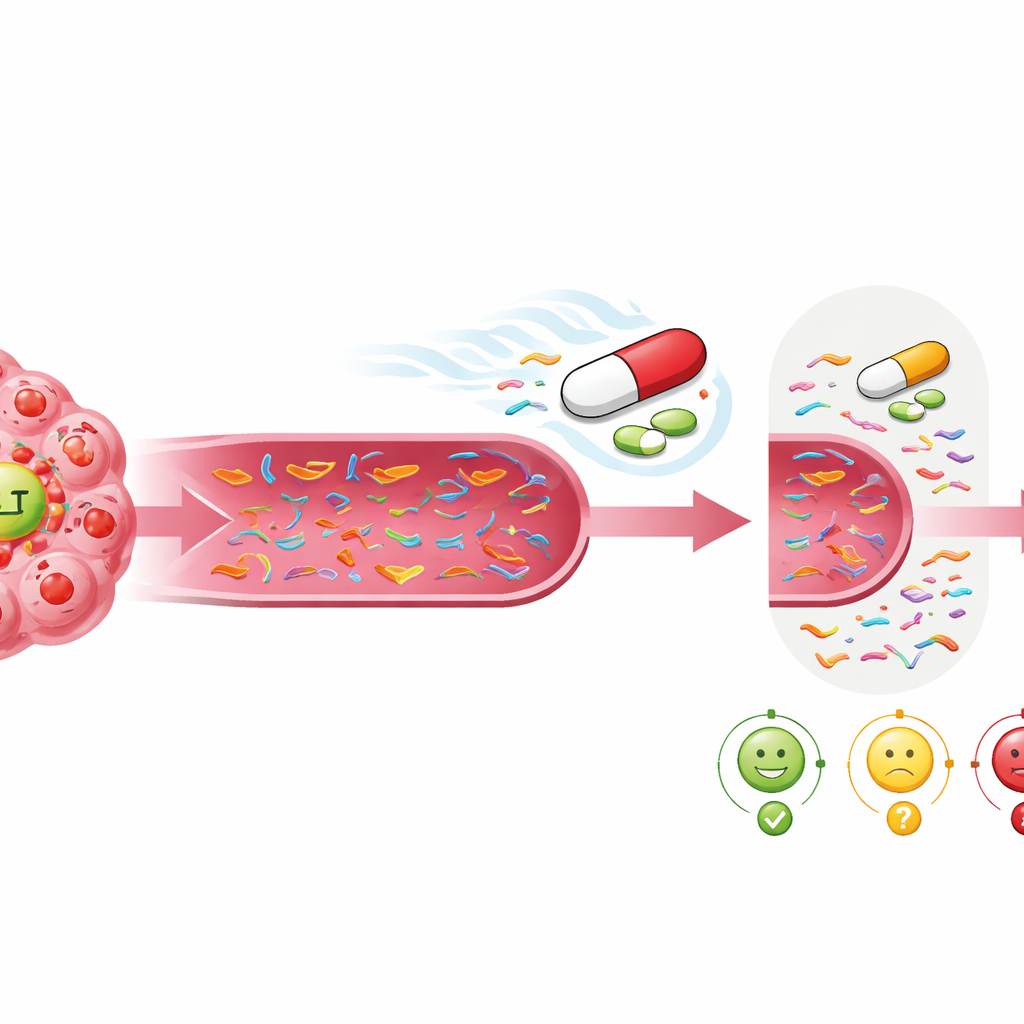
Equilibrar simplicidad y mayor visión
Usar solo el ADN relacionado con MET como guía ofreció la instantánea más clara y simple de si el ensartinib estaba ayudando. Este enfoque focalizado tuvo alta especificidad, lo que significa que cuando las señales de MET desaparecían, había una fuerte probabilidad de que el paciente evolucionara bien. Esto lo hace atractivo como herramienta práctica: las pruebas de un solo gen son más baratas, más rápidas y más fáciles de interpretar que los paneles amplios. Al mismo tiempo, escanear más genes seguía teniendo valor, porque podía revelar nuevas mutaciones que explicasen por qué un tumor dejó de responder y orientar opciones terapéuticas futuras. El estudio sugiere que combinar una visión estrecha centrada en MET para decisiones tempranas con una visión más amplia para rastrear resistencias podría ofrecer lo mejor de ambos enfoques.
Qué significa esto para los pacientes
Para un público general, el mensaje clave es que una prueba de sangre tomada solo un mes después de comenzar ensartinib ya puede sugerir el beneficio a largo plazo del fármaco. Si el ADN tumoral relacionado con MET desaparece del torrente sanguíneo, las probabilidades de un beneficio significativo y duradero son altas; si persiste, los médicos podrían necesitar vigilar más de cerca o considerar otras opciones. Aunque se trató de un estudio relativamente pequeño y de un solo brazo que requiere confirmación en series más amplias, refuerza la idea de que las “biopsias líquidas” pueden actuar como un boletín temprano sobre tratamientos dirigidos. En el futuro, esa monitorización podría ayudar a personalizar la atención, evitando que los pacientes permanezcan con fármacos ineficaces y guiándoles más rápidamente hacia terapias que funcionen.
Cita: Zhou, M., Zhu, Y., Sun, X. et al. Comparative analysis of ctDNA monitoring strategies in advanced NSCLC with MET exon 14 skipping mutations treated with ensartinib. npj Precis. Onc. 10, 110 (2026). https://doi.org/10.1038/s41698-026-01284-6
Palabras clave: ADN tumoral circulante, deleción del exón 14 de MET, ensartinib, cáncer de pulmón no microcítico, monitorización mediante biopsia líquida