Clear Sky Science · es
Un modelo interpretable de aprendizaje profundo para predecir subtipos moleculares del cáncer de endometrio a partir de láminas teñidas con H&E
Por qué importa para la salud de las mujeres
El cáncer de endometrio, que se origina en el revestimiento del útero, es uno de los cánceres más comunes en mujeres y su tasa de mortalidad está aumentando en todo el mundo. Hoy sabemos que este cáncer en realidad presenta varias “variantes” moleculares que responden de forma diferente a la cirugía, la radiación, la quimioterapia y las terapias inmunes más recientes. Actualmente, identificar esos subtipos moleculares suele requerir pruebas genéticas costosas y que consumen tiempo, que muchos hospitales no pueden ofrecer con facilidad. Este estudio explora si un sistema de inteligencia artificial (IA) bien diseñado puede leer las láminas de patología de rutina —las imágenes en rosa y púrpura del tejido que ya se toman a cada paciente— e inferir con precisión esos subtipos moleculares, lo que podría hacer que la atención de precisión esté más al alcance.
Una mirada más cercana a la diversidad tumoral
No todos los cánceres de endometrio se comportan igual. Algunos crecen despacio y se mantienen confinados al útero; otros se diseminan temprano y son más difíciles de tratar. Las guías modernas dividen estos tumores en cuatro subtipos moleculares basados en cambios del ADN y en cómo las células reparan el daño genético. Estas categorías ayudan a predecir el pronóstico y a orientar decisiones como la extensión de la cirugía o si una paciente podría beneficiarse de inmunoterapia. Sin embargo, las pruebas genéticas y las tinciones especiales requeridas son caras, dependen de la interpretación de expertos y a menudo no están disponibles en hospitales pequeños o con recursos limitados. Los patólogos han sospechado durante mucho tiempo que muchas de estas diferencias moleculares dejan pistas visuales en la apariencia de las células y el tejido de sostén al microscopio, pero esas pistas pueden ser demasiado sutiles y complejas para que el ojo humano las juzgue de forma consistente.
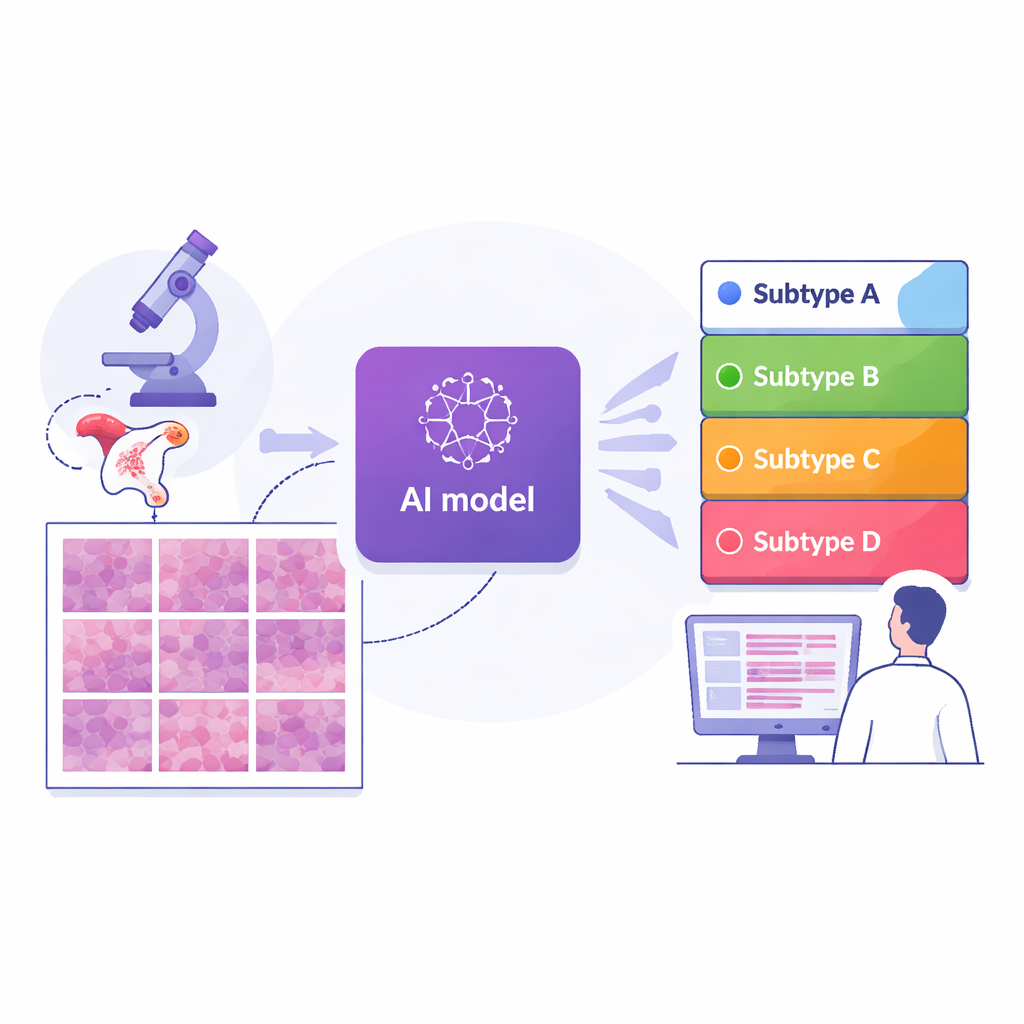
Enseñar a los ordenadores a leer láminas de patología
Los investigadores reunieron imágenes digitales de 364 láminas de tejido procedentes de 324 mujeres tratadas en un importante centro oncológico de Shanghái, junto con dos grupos de comparación independientes: 296 láminas de un conjunto de datos público internacional y 36 de otro hospital en Suzhou. Cada caso ya había sido asignado a uno de los cuatro subtipos moleculares mediante pruebas genéticas avanzadas. El equipo cortó cada imagen de la lámina completa en miles de pequeños mosaicos y entrenó un modelo de aprendizaje profundo —un tipo de IA usado en reconocimiento de imágenes— para que examinara cada mosaico y estimara la probabilidad de que perteneciera a cada subtipo. Al promediar las predicciones de los mosaicos en toda la lámina, el sistema produjo una única predicción de subtipo por paciente, reflejando de forma análoga cómo los médicos consideran el tumor en su conjunto.
Qué tan bien funcionó el sistema
En el grupo principal de Shanghái, la IA alcanzó un alto nivel de precisión: su puntuación global para distinguir entre los cuatro subtipos (medida por una estadística estándar que va de 0,5 para adivinar a 1,0 para separación perfecta) fue de aproximadamente 0,87. El rendimiento se mantuvo sólido —alrededor de 0,84— cuando se probó en los dos grupos externos procedentes de distintos hospitales y sistemas de escaneo de láminas, lo que sugiere que el enfoque es razonablemente robusto. En comparación con varias estrategias de IA líderes que usan esquemas de atención o agregación más complejos, este modelo de extremo a extremo, construido sobre una columna vertebral moderna de análisis de imágenes, generalmente rindió mejor. Es importante que los autores diseñaran el sistema para que fuera interpretable: emplearon herramientas de visualización para resaltar exactamente qué regiones de cada mosaico la IA usó para tomar sus decisiones.
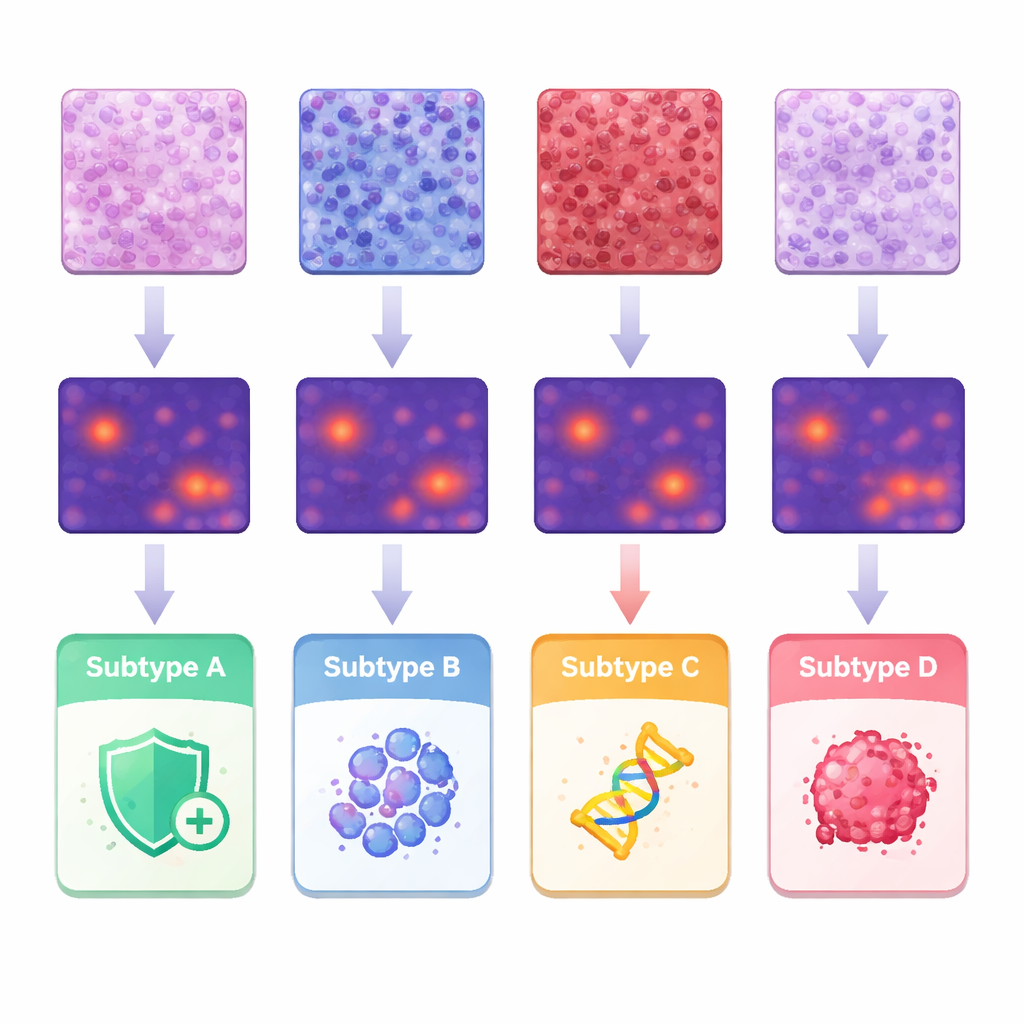
Qué “vio” la IA en el microambiente tumoral
Para entender qué características impulsaron las predicciones, el equipo vinculó los mapas de calor de la IA con observaciones patológicas clásicas y con medidas detalladas de la forma y disposición de células individuales. Los tumores de un subtipo mostraron una densa infiltración de células inmunitarias en el tejido de sostén, mientras que otro subtipo tendía a tener células estructurales muy compactas. Un tercer grupo exhibió láminas sólidas de células tumorales altamente anómalas, y el subtipo asociado a un comportamiento agresivo mostró estructuras papilares, en forma de dedos, y núcleos muy irregulares. Al segmentar y analizar aproximadamente 245 millones de células, los investigadores cuantificaron diferencias en el tamaño celular, la variación y el espaciado, y mostraron cómo ciertas combinaciones se alineaban con subtipos específicos. Estos hallazgos respaldan la idea de que las diferencias moleculares dejan una huella reconocible en la arquitectura tisular que las máquinas pueden detectar de forma sistemática.
Del proof of concept a la ayuda clínica
Este trabajo no pretende reemplazar las pruebas genéticas; en cambio, propone una herramienta de triaje “H&E primero” que usa la tinción estándar ya preparada para cada biopsia. En la práctica, un mapa de probabilidades de subtipos generado por IA podría ayudar a los patólogos a decidir qué pruebas confirmatorias solicitar primero, priorizar tejido limitado para los ensayos más informativos y acelerar las decisiones terapéuticas, especialmente en hospitales donde el perfil molecular completo es difícil de obtener. El estudio también pone de manifiesto límites actuales, como el rendimiento más débil para el subtipo más raro y la necesidad de conjuntos de datos mayores y más diversos antes de su implementación. Aun así, ofrece una demostración convincente de que las imágenes de microscopio de rutina contienen suficiente información oculta para que la IA aproxime etiquetas moleculares complejas, abriendo un camino hacia una atención más equitativa y basada en datos para las mujeres con cáncer de endometrio.
Cita: Guo, Q., Cui, H., Zhang, Y. et al. An interpretable deep learning model for predicting endometrial cancer molecular subtypes from H&E-stained slides. npj Precis. Onc. 10, 71 (2026). https://doi.org/10.1038/s41698-026-01280-w
Palabras clave: cáncer de endometrio, patología digital, aprendizaje profundo, subtipos moleculares, oncología de precisión