Clear Sky Science · es
Un atlas integrado de cáncer de pulmón a célula única revela fenotipos de fibroblastos distintos entre adenocarcinoma y carcinomas de células escamosas
Por qué importa el vecindario alrededor de un tumor
El cáncer de pulmón no está formado solo por células cancerosas. Más bien se parece a una ciudad concurrida donde las células tumorales conviven con vasos sanguíneos, células inmunitarias y células de soporte. Este estudio plantea una pregunta sorprendentemente simple con grandes implicaciones: ¿construyen las dos formas principales de cáncer de pulmón no microcítico —adenocarcinoma y carcinoma de células escamosas— “vecindarios” distintos dentro del pulmón, y podrían estas diferencias ayudar a explicar por qué algunos pacientes tienen mejor o peor evolución? Utilizando potentes herramientas de lectura de ADN a nivel de célula única, los investigadores cartografían cientos de miles de células individuales para revelar cómo un grupo clave de células de soporte, llamadas fibroblastos, se comporta de manera muy diferente en estos dos tipos de cáncer.
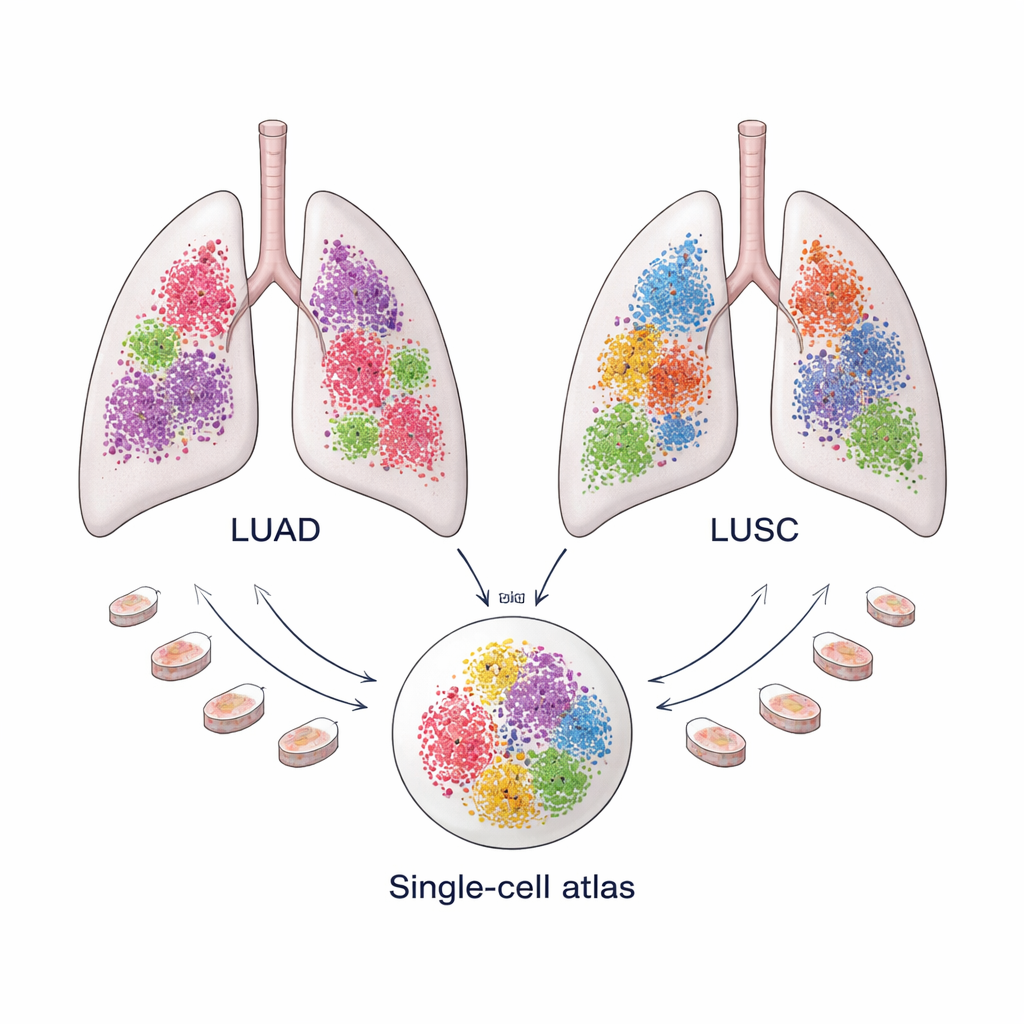
Dos cánceres pulmonares comunes, dos ecosistemas distintos
El cáncer de pulmón no microcítico constituye alrededor del 85 por ciento de los cánceres de pulmón y está dominado por dos tipos: adenocarcinoma pulmonar (LUAD), que suele surgir en las partes periféricas del pulmón, y carcinoma de células escamosas pulmonar (LUSC), que tiende a ocurrir más centralmente. Aunque hoy en día ambos se tratan bajo una misma etiqueta amplia, responden de forma diferente a las terapias y presentan resultados a largo plazo distintos. Evidencia creciente sugiere que estas diferencias no se deben solo a las células cancerosas, sino también al “microambiente tumoral”, la mezcla de células inmunitarias, vasos sanguíneos y células estructurales que rodean e interactúan con el tumor.
Construyendo un atlas de cáncer de pulmón a célula única
Para entender estos microambientes en detalle, el equipo reunió un gran “atlas” de datos de secuenciación de ARN a célula única: 366.652 células de 175 muestras de LUAD y 125.238 células de 74 muestras de LUSC, extraídas de diez conjuntos de datos públicos. El patrón de actividad génica de cada célula sirvió como una huella digital que permitió a los investigadores clasificar las células en grupos principales como células inmunitarias, células de vasos sanguíneos, células cancerosas y células estructurales o “estromales”. Métodos computacionales sofisticados eliminaron luego el ruido técnico y alinearon las muestras para que las células de distintos pacientes pudieran compararse directamente. Esta escala es crucial, porque algunos tipos celulares, en especial los fibroblastos, son raros y difíciles de aislar en números suficientes en un solo estudio.
Fibroblastos: los moldeadores del paisaje tumoral
Los fibroblastos son células de soporte que construyen y remodelan el tejido conectivo. En los tumores, se convierten en fibroblastos asociados a cáncer (CAF), que pueden restringir o promover el crecimiento tumoral según su estado. Al centrarse en más de 8.700 fibroblastos, los autores identificaron cinco subtipos principales de CAF: CAFs miofibroblásticos (mCAFs), CAFs inflamatorios (iCAFs), CAFs asociados a vasos (vCAFs), CAFs en ciclación (cCAFs) y CAFs presentadoras de antígeno (apCAFs). El equilibrio entre estos subtipos difería notablemente entre LUAD y LUSC. Los tumores LUAD tendían a albergar más iCAFs, que secretan altos niveles de moléculas inflamatorias, mientras que los tumores LUSC eran más ricos en mCAFs, que producen tejido fibroso y rígido y ayudan a formar el andamiaje físico del tumor.
Las células cancerosas enseñan a los fibroblastos sus roles
Para probar si las propias células cancerosas instruyen a los fibroblastos para adoptar estas identidades, los investigadores cultivaron fibroblastos pulmonares normales en placas junto con líneas celulares de LUAD o LUSC. Al exponerse a células LUAD, los fibroblastos activaron genes típicos de iCAFs, incluidos conocidos mediadores inflamatorios como IL-6 y ciertas quimioquinas. Cuando se emparejaron con células LUSC, esos mismos fibroblastos activaron en cambio genes mCAF implicados en contracción similar a la muscular y producción de colágeno. Los análisis de comunicación célula a célula sugirieron que las células LUAD usan citocinas como IL-1, LIF y OSM para impulsar el estado inflamatorio iCAF, mientras que las células LUSC dependen más de señales mecánicas y de la señalización WNT no canónica para empujar a los fibroblastos hacia el estado mCAF de construcción de matriz.
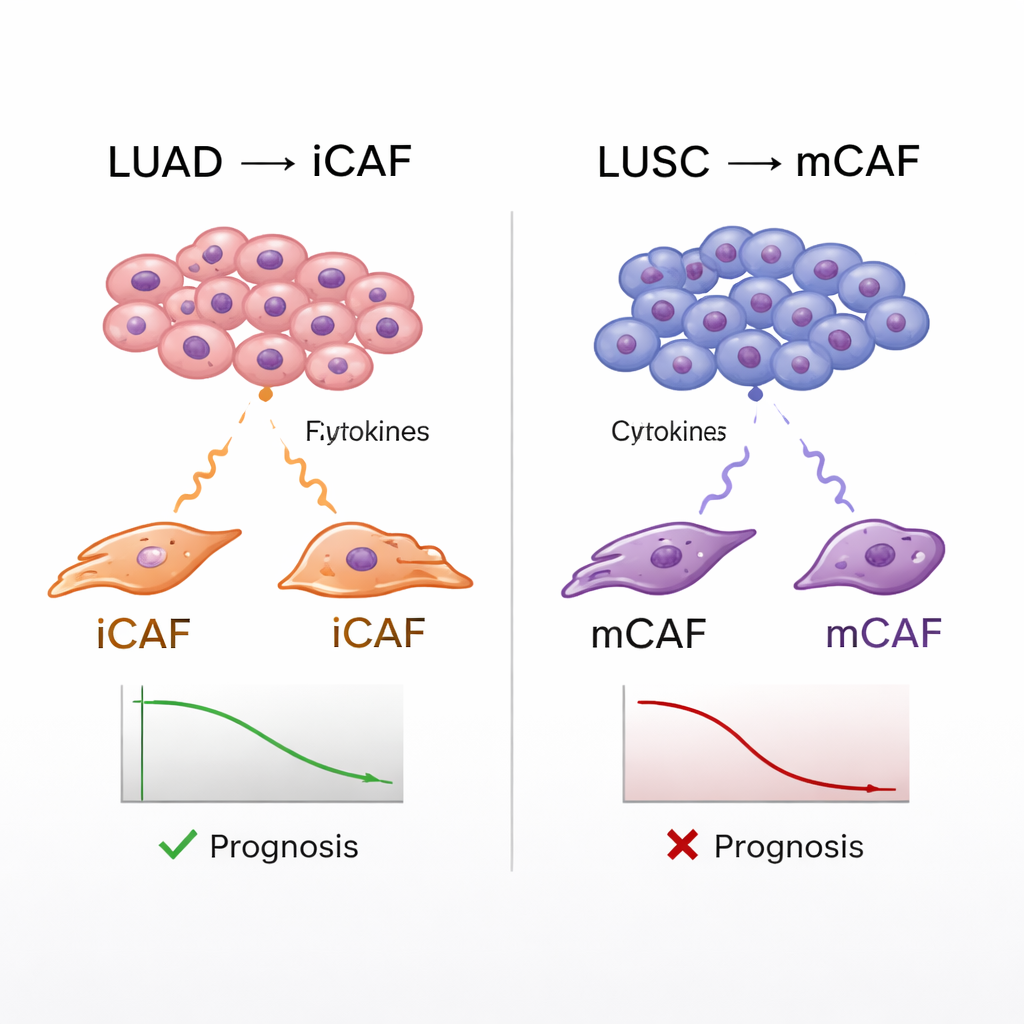
Vinculando tipos de fibroblastos con resultados en pacientes
El atlas también permitió al equipo conectar los subtipos de CAF con datos de pacientes del mundo real. Usando grandes bases de datos de cáncer, estimaron cuán fuertemente cada tumor expresaba firmas génicas de los distintos tipos de fibroblastos y luego compararon estas puntuaciones con la supervivencia. En LUAD y LUSC, los tumores enriquecidos en mCAFs se asociaron con peores resultados, consistente con la idea de que una cápsula densa y fibrosa alrededor de los tumores puede favorecer la progresión y bloquear el ataque inmunitario. Los iCAFs, sin embargo, mostraron una personalidad partida: en LUSC, altas firmas de iCAFs también predijeron peor supervivencia, mientras que en LUAD se asociaron con mejores resultados. Análisis adicionales sugirieron que en LUSC, los iCAFs ayudan a atraer neutrófilos —células inmunitarias que, en este contexto, parecen suprimir a los linfocitos T beneficiosos— creando un ambiente especialmente hostil para respuestas inmunes efectivas.
Qué significa esto para el futuro del tratamiento del cáncer de pulmón
Para un público no especialista, el mensaje clave es que no todas las células de soporte en los tumores de pulmón son iguales, y el mismo subtipo de fibroblasto puede tener significados opuestos según el contexto del cáncer. LUAD y LUSC no solo difieren en el ADN de sus células cancerosas; construyen ecosistemas microscópicos distintos que moldean cómo crecen los tumores y cómo les va a los pacientes. Al cartografiar estos ecosistemas célula por célula, este estudio identifica poblaciones específicas de fibroblastos que podrían servir como marcadores pronósticos o como dianas para futuras terapias —idealmente permitiendo que los tratamientos se adapten no solo al tipo de cáncer, sino también a la mezcla de células que lo rodean y lo sostienen.
Cita: Hirano, Y., Suzuki, H., Nakayama, J. et al. An integrated single-cell lung cancer atlas reveals distinct fibroblast phenotypes between adenocarcinoma and squamous cell carcinomas. npj Precis. Onc. 10, 72 (2026). https://doi.org/10.1038/s41698-026-01279-3
Palabras clave: cáncer de pulmón, microambiente tumoral, fibroblastos, secuenciación de ARN de célula única, pronóstico del cáncer