Clear Sky Science · es
TheraMind: un conjunto multi-LLM para acelerar el reposicionamiento de fármacos en el cáncer de pulmón mediante minería de informes de casos
Por qué esto importa para pacientes y médicos
Para las personas con cáncer de pulmón avanzado, el tiempo es precioso y las opciones de tratamiento a menudo se agotan rápidamente. Desarrollar fármacos nuevos puede llevar más de una década, pero pistas dispersas sobre terapias útiles pueden ya estar escondidas en relatos de pacientes publicados, llamados informes de casos. Este artículo presenta TheraMind, un sistema de inteligencia artificial que rastrea miles de estos informes para descubrir medicamentos existentes que podrían reutilizarse de forma segura para ayudar a personas con cáncer de pulmón de difícil tratamiento.
El desafío de encontrar nuevos usos para fármacos antiguos
El carcinoma no microcítico de pulmón es el cáncer más letal del mundo, con tasas de supervivencia que siguen siendo muy bajas una vez que la enfermedad se ha diseminado. Descubrir y testar fármacos desde cero es lento, costoso y arriesgado. En contraste, los fármacos “reposicionados” ya están aprobados para otras enfermedades, por lo que su seguridad está mucho mejor documentada. Los oncólogos se interesan por estos fármacos, especialmente para pacientes que han agotado los tratamientos estándar, pero necesitan evidencia del mundo real de que un fármaco realmente ayudó a alguien con cáncer de pulmón, no solo datos prometedores de laboratorio. Estas pistas clínicas aparecen a menudo en informes de casos individuales enterrados en la literatura médica, que son difíciles y lentos de encontrar manualmente.
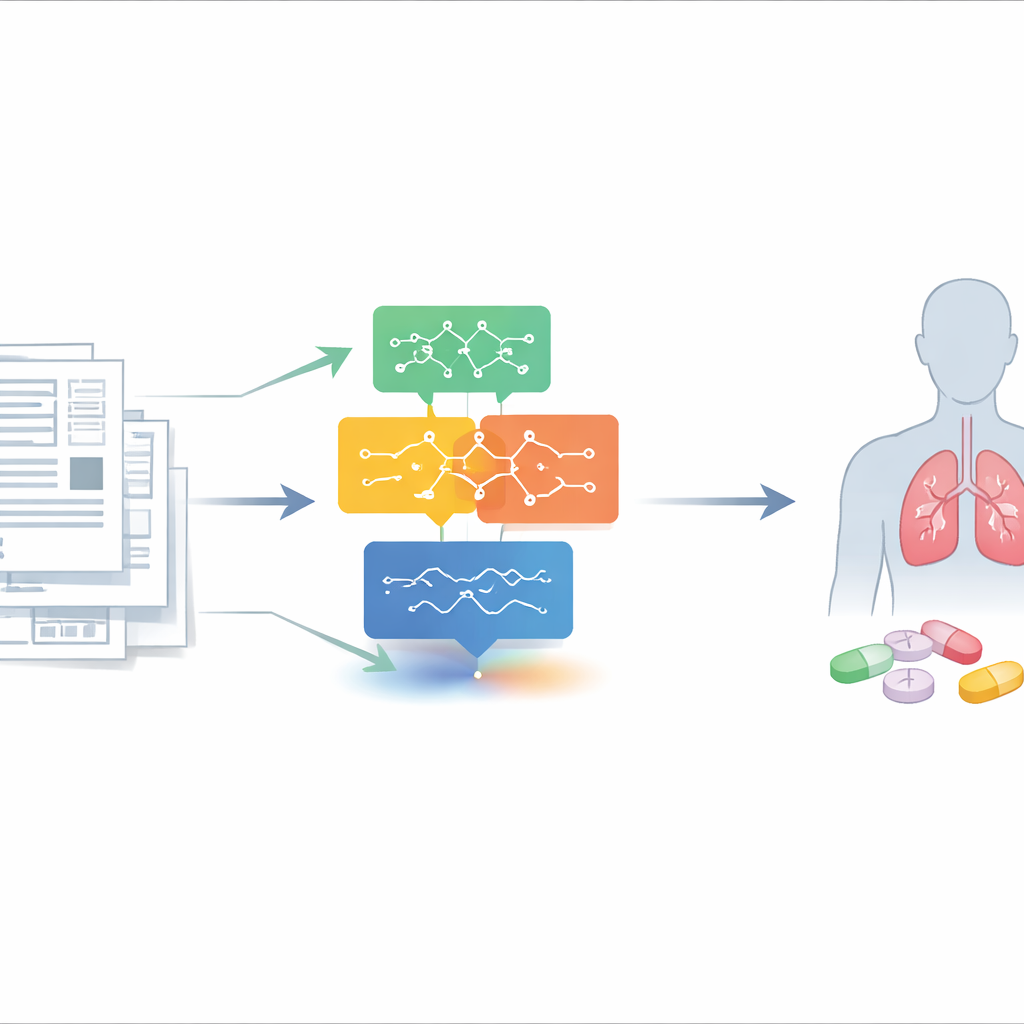
Un lector digital para miles de relatos de pacientes
Los investigadores construyeron TheraMind para actuar como un lector incansable y cuidadoso de informes de casos. Partiendo de 18 candidatos a fármacos sugeridos por estudios genómicos y de laboratorio previos, el sistema extrajo automáticamente 10.023 informes de casos de PubMed, la mayor base de datos de artículos médicos. A continuación, introdujo el texto de cada informe en tres modelos de lenguaje separados —diferentes “lectores” de IA entrenados para comprender la escritura médica. Para cada informe, estos modelos respondieron las mismas cuatro preguntas simples: ¿Se describe al paciente con carcinoma no microcítico de pulmón? ¿Se administró el fármaco del estudio específicamente para tratarlo? ¿Se interrumpió el tratamiento prematuramente? ¿Y experimentó el paciente un buen resultado clínico?
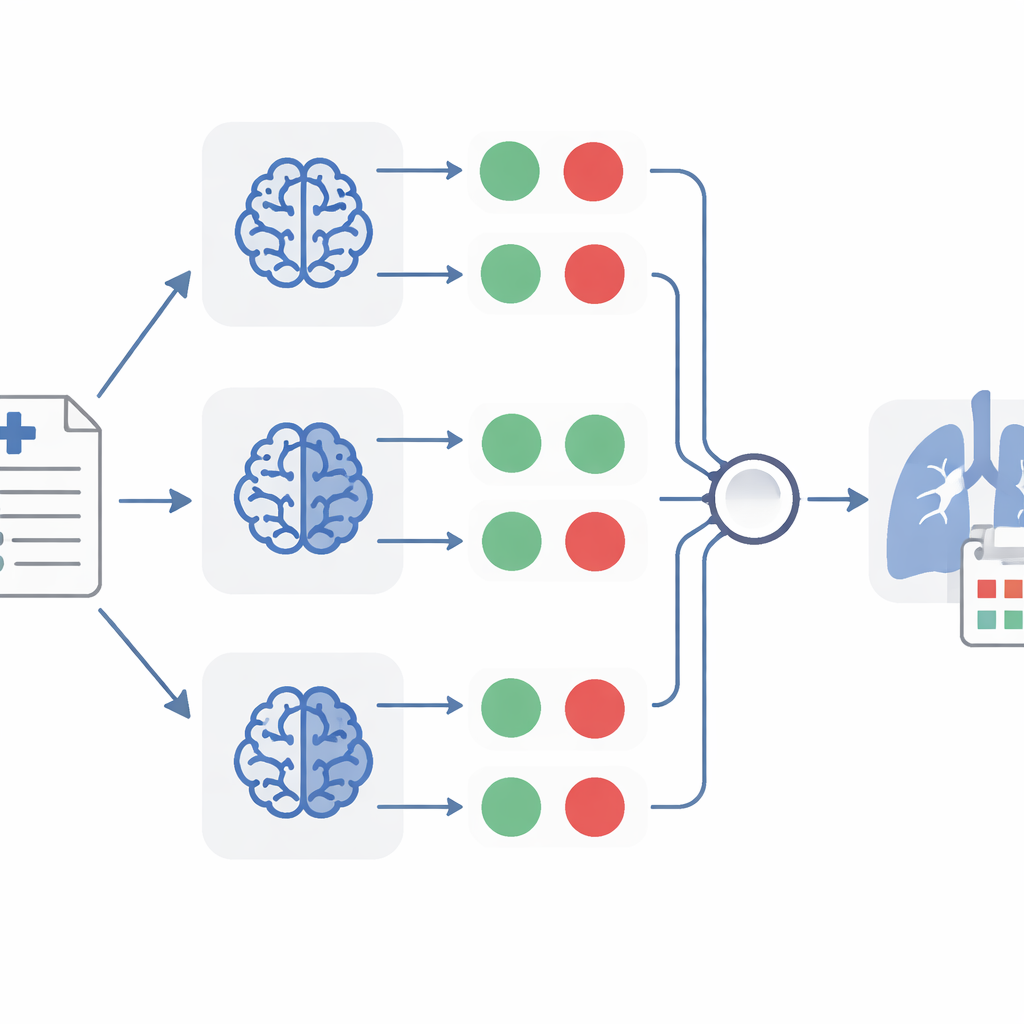
Cómo el equipo de IA llega a una decisión conjunta
Una vez que TheraMind convierte cada informe en un conjunto de respuestas sí/no, entran en juego varias capas de toma de decisiones. Un método usa un árbol de decisión diseñado manualmente que requiere que las cuatro condiciones se cumplan antes de considerar un caso relevante para el reposicionamiento. Otro permite que un único modelo valore la evidencia de forma más flexible, considerando tanto las respuestas sí/no como las breves explicaciones que produjo. El método más potente combina tres clasificadores independientes, cada uno basado en un modelo distinto, y acepta un informe solo cuando al menos dos de los tres coinciden en que es relevante. Este enfoque de “voto mayoritario” ayuda a cancelar errores individuales, de forma similar a pedir a varios médicos independientes que revisen la misma historia clínica.
Lo que TheraMind descubrió en los informes de cáncer de pulmón
Aplicado a la gran colección de informes de casos, TheraMind marcó 26 como que apoyaban firmemente el uso de diez fármacos diferentes en carcinoma no microcítico de pulmón. El método de conjunto alcanzó una sensibilidad de aproximadamente el 92 por ciento, lo que significa que capturó casi todos los informes verdaderamente relevantes, manteniendo al mismo tiempo una especificidad muy alta del 99,7 por ciento, de modo que muy pocos informes irrelevantes se filtraron. Para cada informe seleccionado, el sistema también extrajo detalles clave del paciente —como edad, sexo, antecedentes médicos, condición y el fármaco sospechoso— en un formato de datos consistente, y generó un resumen breve y claro del caso. Revisores humanos con formación en biología y en ciencias de la computación comprobaron estos resultados y confirmaron que uno de los modelos en particular produjo extracciones altamente precisas y completas.
Más allá del cáncer de pulmón y hacia la clínica
Para probar la flexibilidad del sistema, el equipo también orientó TheraMind al cáncer de mama y a varios fármacos candidatos identificados previamente por su propia investigación. En ese contexto, el sistema no reportó informes de casos coincidentes, reflejando con exactitud el registro científico actual en lugar de inventar evidencia. Los autores sostienen que este tipo de canal estructurado y transparente —combinando lógica basada en reglas con múltiples lectores de IA— puede ayudar a cerrar la brecha entre los descubrimientos de laboratorio y los tratamientos listos para ensayos clínicos. Destacan tanto la promesa de aplicar métodos similares a otros cánceres como la necesidad de manejar la privacidad del paciente con cuidado si versiones futuras se conectan directamente a registros electrónicos de salud.
Qué significa esto para tratamientos futuros
En términos sencillos, TheraMind convierte relatos de pacientes dispersos y no estructurados en evidencia organizada sobre la que médicos e investigadores pueden actuar. Al mostrar rápidamente los informes en los que fármacos existentes parecen ayudar a personas con cáncer de pulmón, puede orientar qué medicamentos reposicionados merecen un estudio más profundo en ensayos clínicos. Aunque no sustituye el juicio médico, este lector de IA multimodelo ofrece una manera de cribar montañas de textos médicos y entregar una lista breve y confiable de opciones prometedoras para pacientes que necesitan con urgencia nuevas alternativas.
Cita: More, V., Lu, L., Ding, Z. et al. TheraMind: a multi-LLM ensemble for accelerating drug repurposing in lung cancer via case report mining. npj Precis. Onc. 10, 95 (2026). https://doi.org/10.1038/s41698-025-01265-1
Palabras clave: reposicionamiento de fármacos, cáncer de pulmón, informes de casos, modelos de lenguaje grande, minería de evidencia clínica