Clear Sky Science · es
Perfilado de núcleos únicos y espacial de teratomas sacrococcígeos revela composición celular y heterogeneidad en la inactivación del cromosoma X
Por qué importan los tumores de la espalda de los bebés
Los teratomas sacrococcígeos son tumores raros que crecen en la base de la columna de un bebé, a veces incluso antes del nacimiento. Pueden contener muchos tejidos diferentes—nervioso, intestinal, piel, músculo—todos mezclados. Los médicos suelen poder extirparlos, pero algunos crecen peligrosamente rápido, y aparecen aproximadamente tres veces más en bebés con dos cromosomas X que en aquellos con uno. Este estudio utiliza herramientas genéticas de vanguardia para construir un “mapa celular” detallado de estos tumores y para preguntarse si un comportamiento inusual del cromosoma X podría ayudar a explicar cómo se forman los tumores y por qué están tan sesgados hacia las niñas.
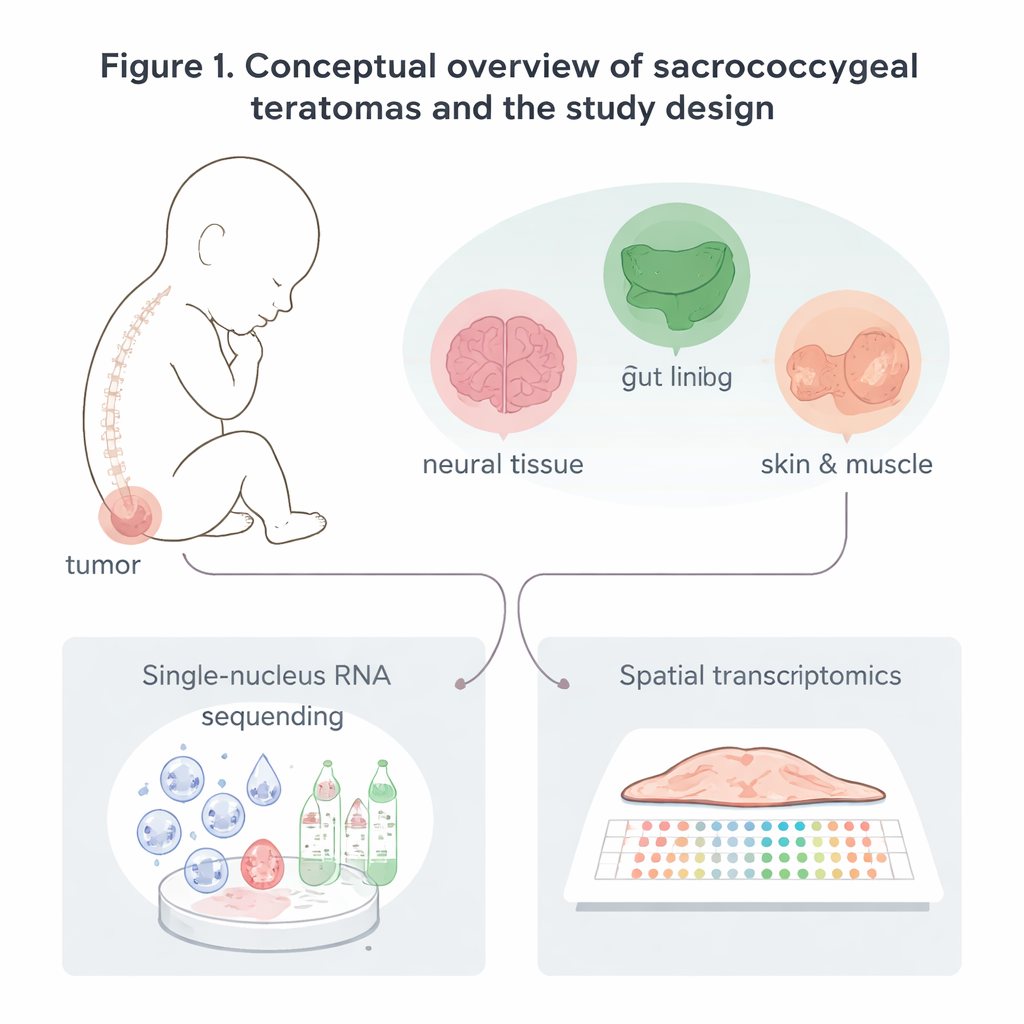
Construyendo un mapa detallado de las células tumorales
Los investigadores recogieron ocho teratomas sacrococcígeos: seis extirpados tras el nacimiento y dos extirpados antes del parto en embarazos de alto riesgo. En lugar de limitarse a observar los tumores al microscopio, leyeron qué genes estaban activos en decenas de miles de núcleos celulares individuales. También emplearon transcriptómica espacial, un método que mide la actividad génica en cortes finos de tejido preservando la posición de cada señal dentro del tumor. A partir de estos datos, identificaron cinco familias celulares principales: células relacionadas con el sistema nervioso, células de revestimiento (epiteliales), células de sostén (estromales) como músculo y cartílago, células de los vasos sanguíneos y células inmunitarias como macrófagos y linfocitos T. Cada familia contenía múltiples subtipos, revelando que estos tumores son mosaicos de muchos tejidos reconocibles, parecidos a los del cuerpo, en lugar de una masa uniforme.
Diferentes tumores, distintas mezclas de tejidos
Aunque todos los tumores contenían células semejantes a las tres capas embrionarias principales, sus mezclas variaron enormemente. Tratando todas las células de un tumor como una “voz” combinada, el equipo comparó patrones globales de expresión génica y encontró tres grandes grupos de tumores. Un grupo era rico en células epiteliales que expresaban fuertemente un gen a menudo asociado con estados embrionarios tempranos (POU5F1); otro grupo tenía menos células epiteliales pero más vasos sanguíneos y tejido parecido al cartílago; y un tercer grupo combinaba células epiteliales y relacionadas con el sistema nervioso. Estas diferencias se alinearon con programas génicos relacionados con la inflamación, el crecimiento vascular y el desarrollo del sistema nervioso. En los tumores de rápido crecimiento extirpados antes del nacimiento, el mapeo espacial mostró que células estromales y de tipo nervioso dominaban grandes regiones, con racimos de células en división activa dispersos, lo que sugiere que estos tumores de crecimiento rápido se alimentan de focos de células estromales y nerviosas en ciclo.
Poniendo en cuestión la idea de una célula madre oculta
Dado que los teratomas contienen una gran variedad de tejidos, muchos científicos han sospechado que surgen de una célula rara y potente similar a las células madre primitivas que originan óvulos y espermatozoides. El equipo buscó específicamente células que activaran a la vez genes característicos de células pluripotentes y de células germinales primordiales. Encontraron expresión dispersa de algunos de estos genes, pero nunca de un modo que identificara una población “maestra” unificada y clara. En su lugar, genes relacionados con células germinales y pluripotencia aparecieron en tipos celulares comunes del tumor, como células inmunitarias o ciertos epitelios. Esto sugiere que, al menos en los tumores estudiados aquí, cualquier fundador con cualidades de célula madre o bien desapareció o dejó solo trazas tenues en poblaciones celulares más maduras.
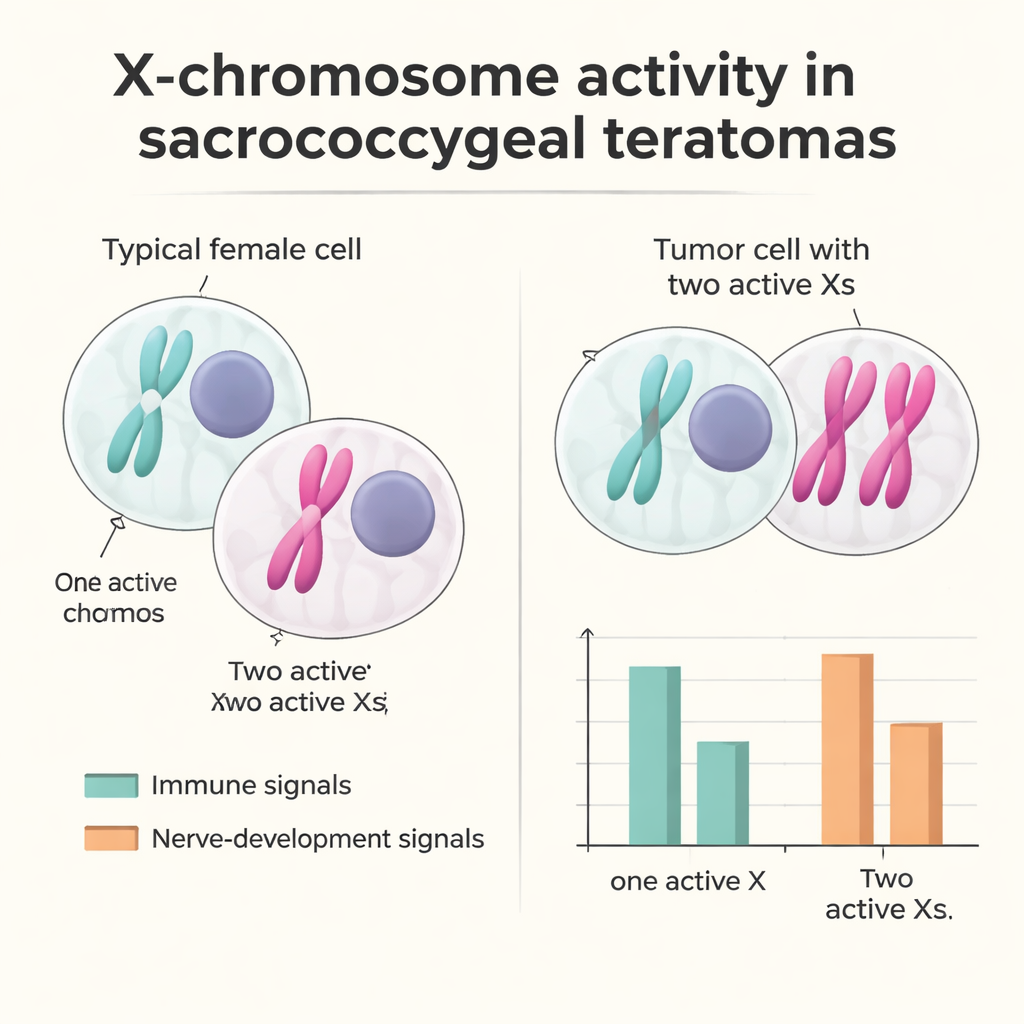
Dos cromosomas X activos y una respuesta inmune más tenue
Para explorar por qué estos tumores son mucho más comunes en bebés con dos cromosomas X, los investigadores examinaron cómo se regulaba el cromosoma X dentro de las células tumorales. En las células femeninas típicas, uno de los X se apaga para mantener el equilibrio de dosis génica con los varones; esa inactivación se marca por una molécula llamada XIST. En un tumor femenino, descubrieron un grupo sustancial de células que carecían de XIST y mostraban patrones de expresión génica coherentes con tener dos cromosomas X activos. Estas células de tipo “XaXa” aparecían con más frecuencia entre las poblaciones epiteliales, nerviosas y estromales. Mediante el seguimiento de variantes genéticas naturales, el equipo demostró que muchos genes ligados al X que deberían estar silenciados en el X inactivo ahora estaban activos en ambas copias, lo que indica una falla del sistema habitual de inactivación más que una simple duplicación de un X ya activo. Las células con dos X activos tendían a expresar más genes implicados en desarrollo temprano y formación neuronal, mientras que las que tenían un solo X activo mostraban señales inmunitarias e inflamatorias más fuertes, lo que sugiere que los cambios en la dosis de X podrían inclinar sutilmente el entorno tumoral para alejarlo del ataque inmunitario.
Qué significa esto para pacientes y familias
Para las familias que afrontan un diagnóstico de teratoma sacrococcígeo, este trabajo aún no cambia el tratamiento cotidiano, que sigue basándose en la cirugía y un seguimiento cuidadoso. Pero ofrece una imagen más clara de la composición de estos tumores y plantea nuevas ideas sobre por qué se forman y por qué son más frecuentes en bebés con dos cromosomas X. El estudio muestra que los tumores pueden agruparse según los tipos de tejidos y programas génicos que contienen, y que, al menos en un caso, las células con dos X activos obtienen ventajas del desarrollo mientras reducen las señales inmunitarias. En el futuro, mapas celulares tan detallados podrían ayudar a los médicos a predecir mejor qué tumores tienen más probabilidad de crecer agresivamente, inspirar pruebas que rastreen poblaciones celulares de riesgo y orientar la investigación hacia terapias que restauren el equilibrio normal del cromosoma X o refuercen la inmunidad antitumoral.
Cita: Rojas, E.J., Giannikou, K., Huang, B.J. et al. Single nuclei and spatial profiling of sacrococcygeal teratomas reveals cellular composition and X inactivation heterogeneity. npj Precis. Onc. 10, 87 (2026). https://doi.org/10.1038/s41698-025-01262-4
Palabras clave: teratoma sacrococcígeo, secuenciación unicelular, transcriptómica espacial, inactivación del cromosoma X, tumores fetales